Содержание
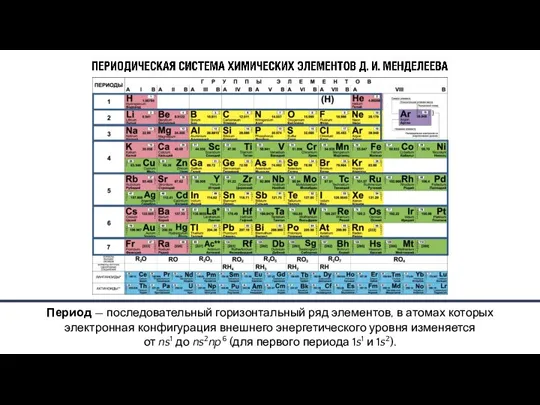
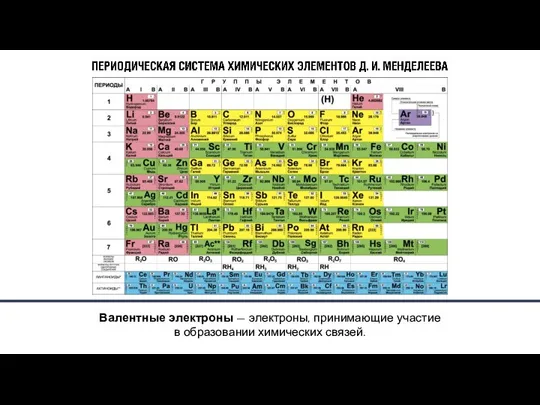
- 3. Характер изменения свойств элементов и соответствующих им соединений – металлические свойства ослабевают, следовательно, неметаллические, усиливаются; –
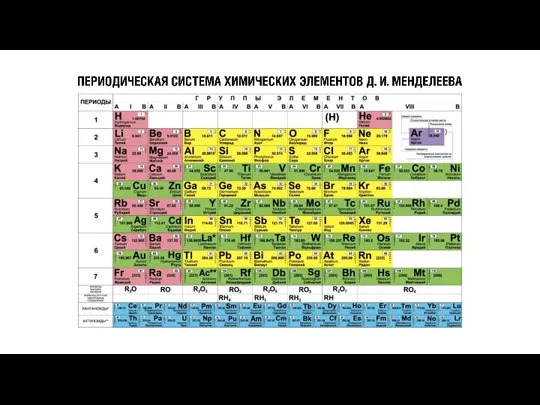
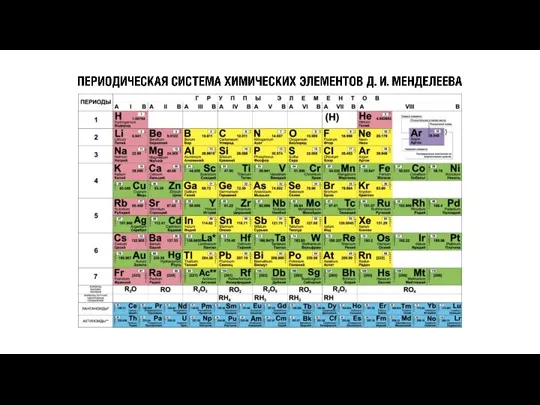
- 4. Д.И. Менделеев 1834–1907 гг. Д.И. Менделеев сделал заключение, которое получило название периодического закона: Свойства химических элементов
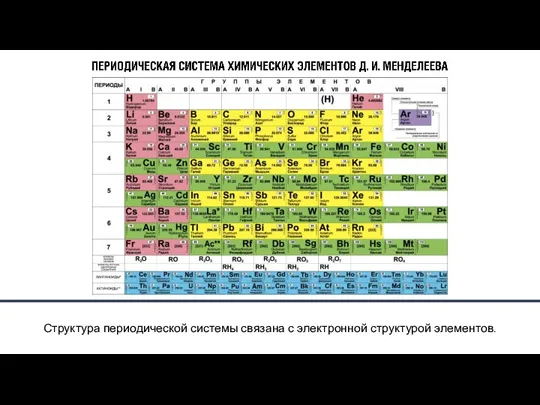
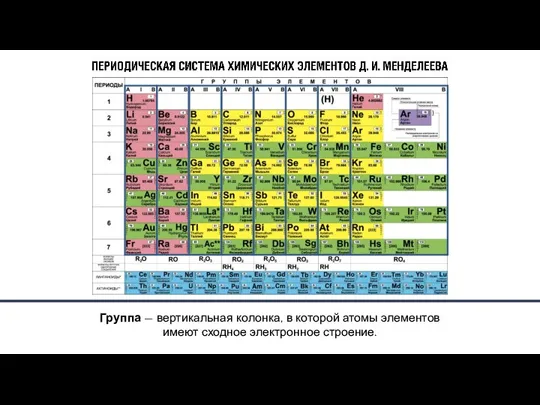
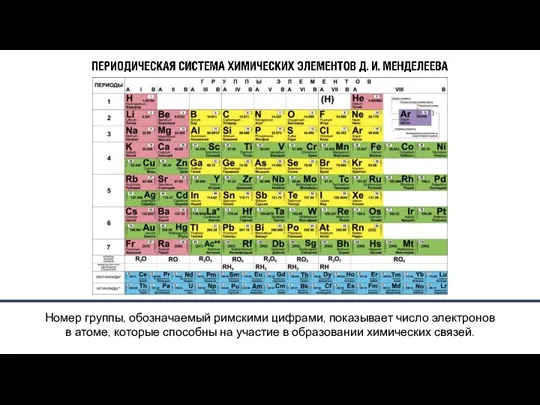
- 6. Главной характеристикой атома, согласно теории строения атома, является положительный заряд ядра, который определяет число электронов в
- 9. N — число нейтронов, А — массовое число атома, Z — атомный номер элемента. N =
- 11. От того, какой энергетический подуровень заполняется последним, различают 4 электронных семейства элементов: s, p, d и
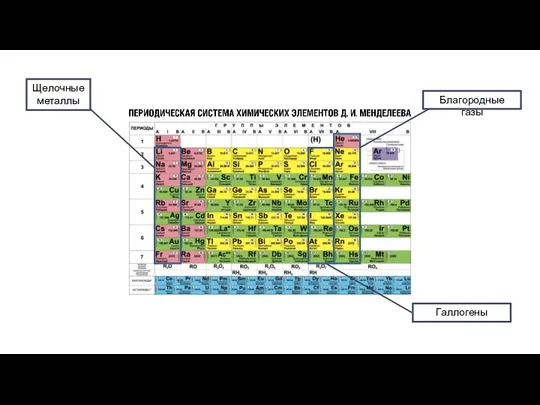
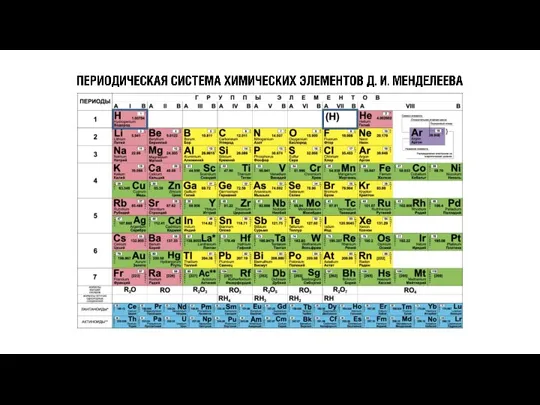
- 19. Причины изменения металлических и неметаллических свойств – заряды атомных ядер элементов и число электронов на внешнем
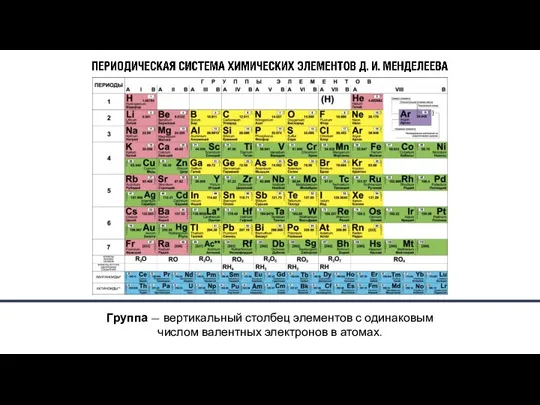
- 20. Причины изменения металлических и неметаллических свойств в пределах одной группы – увеличение зарядов атомных ядер элементов;
- 22. Атом водорода имеет на внешнем (единственном) электронном слое один электрон (относится к s-элементам), ввиду чего он
- 23. Учёные считают, что в космосе существует металлический водород с соответствующей ему металлической кристаллической решеткой и электронной
- 24. В сложных веществах в большинстве случаев водород имеет степень окисления +1, что характерно для щелочных металлов.
- 26. Скачать презентацию












 кулонометрия Дастан
кулонометрия Дастан Методы отбора проб воды. Оформление и подготовка к анализу, протокол исследования воды, определение рН
Методы отбора проб воды. Оформление и подготовка к анализу, протокол исследования воды, определение рН Кремнийорганическая гипотеза
Кремнийорганическая гипотеза Известняк. Разновидности известняка. Области применения
Известняк. Разновидности известняка. Области применения Строение атома
Строение атома Галогеноводородные кислоты
Галогеноводородные кислоты Сухой метод определения глюкозы. Глюкометры
Сухой метод определения глюкозы. Глюкометры Современные сплавы на основе циркония
Современные сплавы на основе циркония Комплексное задание по дисциплине основы материаловедения для группы 18
Комплексное задание по дисциплине основы материаловедения для группы 18 Соли
Соли Минералы и горные породы
Минералы и горные породы lektsia_6 (1)
lektsia_6 (1) Подготовка к контрольной работе химические реакции 8 класс
Подготовка к контрольной работе химические реакции 8 класс Азотосодержащие соединения: Амины. Аминокислоты. Белки
Азотосодержащие соединения: Амины. Аминокислоты. Белки Угольная кислота и её соли
Угольная кислота и её соли Комплексные соединения
Комплексные соединения Альдегиды, строение и свойства
Альдегиды, строение и свойства Презентация на тему Алкены. Строение. Изомерия. Химические свойства. Получение
Презентация на тему Алкены. Строение. Изомерия. Химические свойства. Получение  Распределение электронов в атомах
Распределение электронов в атомах Разработка системы подготовки лаборанта химического анализа
Разработка системы подготовки лаборанта химического анализа Пищевые добавки: вред и польза
Пищевые добавки: вред и польза Строение и функции нуклеиновых кислот. Лекция №3
Строение и функции нуклеиновых кислот. Лекция №3 Исследование биодеградации полимерных материалов методом АСМ
Исследование биодеградации полимерных материалов методом АСМ Коррозия металлов
Коррозия металлов Кислород. Физические и химические свойства. Получение
Кислород. Физические и химические свойства. Получение Классификация сложных неорганических веществ. Оксиды
Классификация сложных неорганических веществ. Оксиды Виготовлення водних розчинів з заданою масовою часткою розчиненої речовини
Виготовлення водних розчинів з заданою масовою часткою розчиненої речовини Стелс-материалы
Стелс-материалы