Содержание
- 2. Раствор - это сложная равновесная химическая система, образованная растворителем, растворенным веществом и продуктами их взаимодействия.
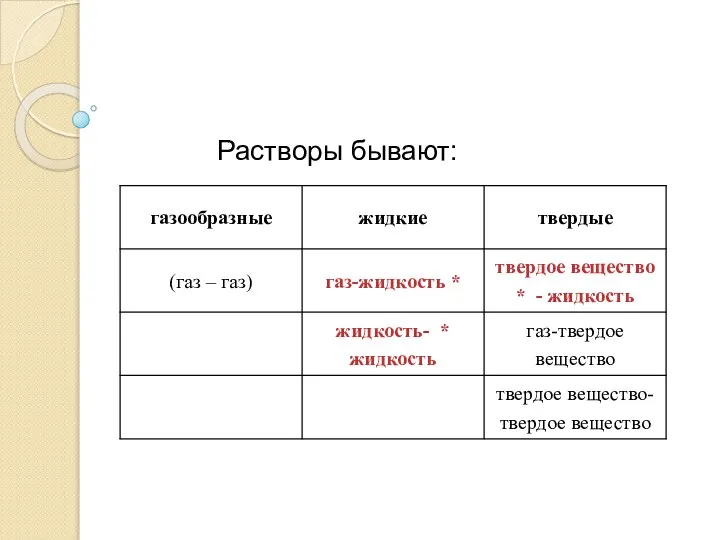
- 4. Растворы бывают:
- 5. Параметры состояния раствора - температура, давление и концентрация.
- 6. Процесс растворения состоит из: 1) фазового перехода (например, кристалл-жидкость) и 2) процесса сольватации Тогда: ΔН =
- 7. Если ΔН = 0 и ΔV = 0, такой раствор называется идеальным. Например, две жидкости, молекулы
- 8. Растворимость газов в жидкостях. ΔНф.п = 0. Следовательно ΔН
- 9. В разбавленных растворах ΔН≈0 и ΔV≈0 . Они приближаются к идеальным растворам. Частицы растворенного вещества далеко
- 10. 1.Массовая доля Отношение массы растворенного вещества к массе раствора, %
- 11. 2. Молярная концентрация Отношение количества растворенного вещества к объему раствора, моль/л
- 12. Отношение массы растворенного вещества к эквивалентной массе растворенного вещества и объему раствора, моль/л 3. Эквивалентная концентрация
- 13. Отношение количества растворенного вещества к массе растворителя, моль/кг 4. Моляльная концентрация или моляльность
- 15. Скачать презентацию











 Prezentatsia_Microsoft_PowerPoint
Prezentatsia_Microsoft_PowerPoint Карбоновые кислоты
Карбоновые кислоты Скорость химической реакции
Скорость химической реакции Межкристаллитная коррозия МКК
Межкристаллитная коррозия МКК Стерилизация технологических потоков и оборудования
Стерилизация технологических потоков и оборудования Научно-познавательное шоу Юный химик
Научно-познавательное шоу Юный химик Алканы
Алканы Основные классы неорганических соединений. Гидроксиды
Основные классы неорганических соединений. Гидроксиды Аспирин и его влияние на организм человека
Аспирин и его влияние на организм человека Алканы
Алканы Альдегиды. Строение молекул
Альдегиды. Строение молекул Техника безопасности при использовании различных видов топлива. Практическая работа № 3
Техника безопасности при использовании различных видов топлива. Практическая работа № 3 Сахароза (С12Н22О11)
Сахароза (С12Н22О11) Алюминий
Алюминий Презентация на тему Экологические риски при добыче и переработке нефти
Презентация на тему Экологические риски при добыче и переработке нефти  Дополнительный_материал_09.14_19.10.2022_b0aaa559
Дополнительный_материал_09.14_19.10.2022_b0aaa559 98675992
98675992 Классификация спиртов. Изомерия спиртов
Классификация спиртов. Изомерия спиртов Ионные уравнения реакций
Ионные уравнения реакций Презентация на тему Вопросы от …
Презентация на тему Вопросы от …  Классификация и номенклатура аминов. 11 класс
Классификация и номенклатура аминов. 11 класс Презентация на тему Оксиды
Презентация на тему Оксиды  06_Типы_химических_реакций_в_органической_химии
06_Типы_химических_реакций_в_органической_химии Гибридизация АО. Пространственное строение молекул (геометрия молекул)
Гибридизация АО. Пространственное строение молекул (геометрия молекул) Ионы кальция, как важное звено в нейроцитотоксическом действии кадмия
Ионы кальция, как важное звено в нейроцитотоксическом действии кадмия Строение электронной оболочки атома часть 2
Строение электронной оболочки атома часть 2 Основные законы и понятия химии. Основные классы неорганических соединений. Химический эквивалент. Закон эквивалентов
Основные законы и понятия химии. Основные классы неорганических соединений. Химический эквивалент. Закон эквивалентов Окислительновосстановительные процессы
Окислительновосстановительные процессы