Содержание
- 2. ЦЕЛИ И ЗАДАЧИ УРОКА: РАССМОТРЕТЬ ОСНОВНЫЕ СПОСОБЫ РЕШЕНИЯ ЗАДАЧ НА ВЫВОД ХИМИЧЕСКОЙ ФОРМУЛЫ ВЕЩЕСТВА ПОЗНАКОМИТЬ УЧАЩИХСЯ
- 3. ВЕЩЕСТВО 1 Соединение содержит 32% углерода, 6,67% водорода, 42,67% кислорода и 18,67% азота. Сочетает в себе
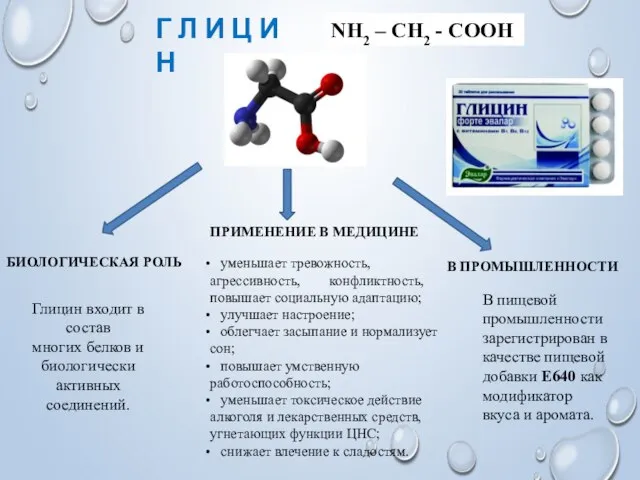
- 4. Г Л И Ц И Н NH2 – CH2 - COOH БИОЛОГИЧЕСКАЯ РОЛЬ Глицин входит в
- 5. АЛГОРИТМ НАХОЖДЕНИЯ ХИМИЧЕСКОЙ ФОРМУЛЫ ВЕЩЕСТВА ПО МАССОВЫМ ДОЛЯМ ЭЛЕМЕНТОВ Прочитайте текст задачи. Запишите условия и требования
- 6. Органическое вещество содержит – 52,17% углерода, 13,04% водорода и 34,78% кислорода. Определите молекулярную формулу вещества. В
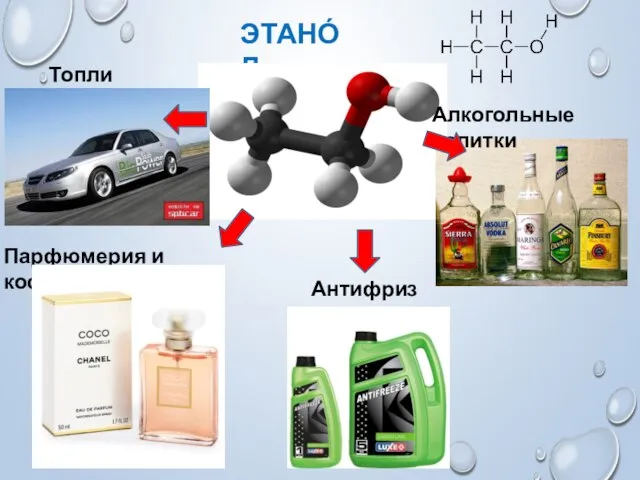
- 7. ЭТАНО́Л Топливо Алкогольные напитки Парфюмерия и косметика Антифризы
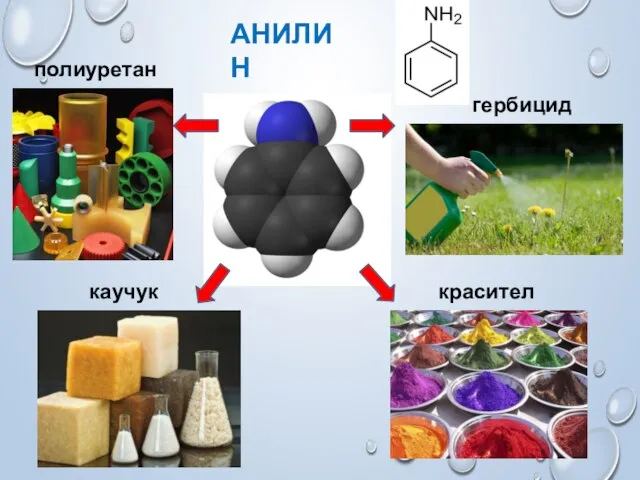
- 8. АНИЛИН полиуретаны каучуки гербициды красители
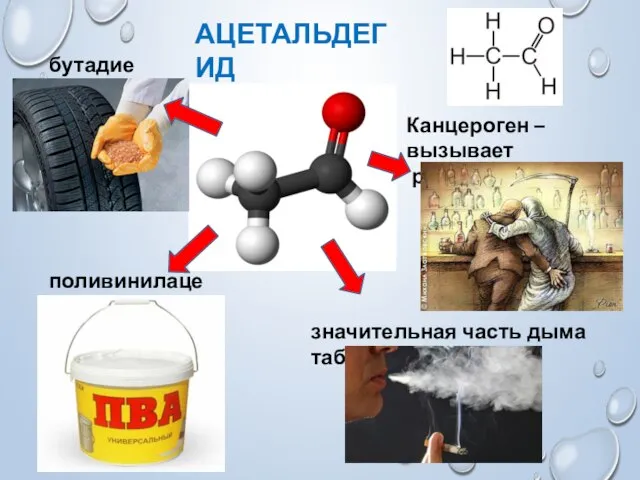
- 9. АЦЕТАЛЬДЕГИД бутадиен поливинилацетат значительная часть дыма табака Канцероген – вызывает рак печени и ЖКТ
- 10. Соединение содержит 51,43% углерода, 8,57% водорода, 40% азота. Молярная масса вещества в 4,827 раз больше молярной
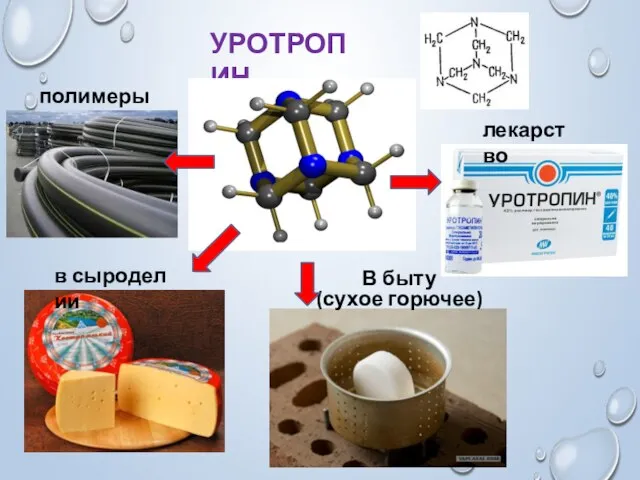
- 11. УРОТРОПИН полимеры лекарство В быту (сухое горючее) в сыроделии
- 12. АЛГОРИТМ НАХОЖДЕНИЯ ХИМИЧЕСКОЙ ФОРМУЛЫ ВЕЩЕСТВА ПО МАССОВЫМ ДОЛЯМ ЭЛЕМЕНТОВ И ЕГО ПЛОТНОСТИ Прочитайте текст задачи. Запишите
- 13. Для нахождения молярной массы вещества в условии задачи часто записывают, что: Относительная плотность паров одного газа
- 14. При полном сгорании органического вещества массой 9 г образовалось 17,6 г углекислого газа, 12,6 г воды,
- 15. Алгоритм нахождения химической формулы вещества по его плотности и продуктам сгорания Прочитайте текст задачи. Запишите условия
- 16. При сгорании органического вещества массой 18,5 г образовался углекислый газ массой 33 г и вода массой
- 17. САМОАНАЛИЗ РЕБЯТА, ЧТО НОВОГО ВЫ УЗНАЛИ СЕГОДНЯ? МОЖНО ЛИ СЧИТАТЬ, ЧТО ЦЕЛИ УРОКА ДОСТИГНУТЫ? ОЦЕНИТЕ СВОЮ
- 19. Скачать презентацию











 Понятие о химической реакции. Реакции, идущие без изменения состава веществ. 11 класс
Понятие о химической реакции. Реакции, идущие без изменения состава веществ. 11 класс Обсидиан
Обсидиан Основные классы неорганических соединений (урок - семинар)
Основные классы неорганических соединений (урок - семинар)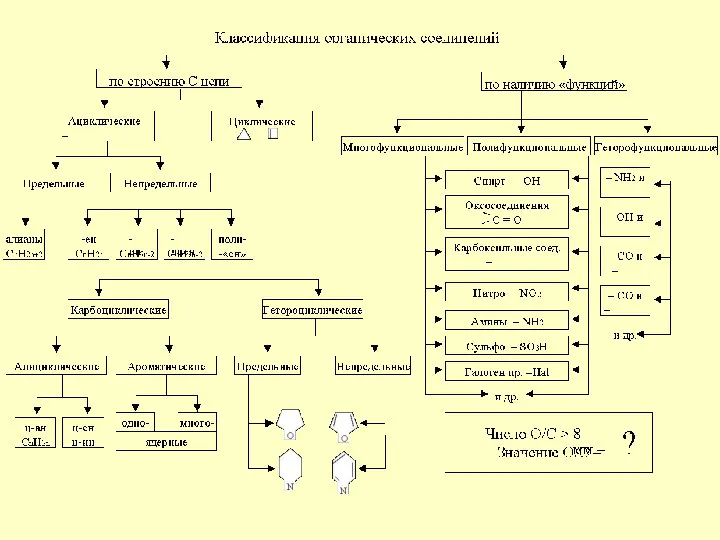 Классификация органических соединений
Классификация органических соединений Строение электронных оболочек атомов химических элементов
Строение электронных оболочек атомов химических элементов Химические процессы на кухне (урок №7)
Химические процессы на кухне (урок №7) Галогены. Элементы главной подгруппы 7 группы Периодической системы Менделеева
Галогены. Элементы главной подгруппы 7 группы Периодической системы Менделеева Применение хидких кристалов в промышленности
Применение хидких кристалов в промышленности Ministry of Education and Science of the Russian Federation
Ministry of Education and Science of the Russian Federation Презентация на тему Угарный газ
Презентация на тему Угарный газ  Prezentatsia1 (1)
Prezentatsia1 (1) Медиатехнологии на уроках химии
Медиатехнологии на уроках химии Классификация оксидов
Классификация оксидов Соли, их классификация и свойства
Соли, их классификация и свойства Соли азотной кислоты – нитраты. 9 класс
Соли азотной кислоты – нитраты. 9 класс Фракционный состав нефти. Химический состав нефти
Фракционный состав нефти. Химический состав нефти Алкадиены
Алкадиены Комплексные соединения
Комплексные соединения Анализ образцов колбасных изделий, образцов бытовой химии, напитков
Анализ образцов колбасных изделий, образцов бытовой химии, напитков Спирты. Классификация, изомерия
Спирты. Классификация, изомерия Особенности решения практикоориентированного задания №26 ГИА-11
Особенности решения практикоориентированного задания №26 ГИА-11 Учебно-познавательные задачи на уроках химии
Учебно-познавательные задачи на уроках химии Карбоновые кислоты
Карбоновые кислоты Теоретические основы органической химии
Теоретические основы органической химии относительная атомная масса
относительная атомная масса Разбор ДЗ. Титрование – общие моменты
Разбор ДЗ. Титрование – общие моменты Тест по химии
Тест по химии Презентация 1
Презентация 1