Содержание
- 2. Строение и свойства атомов
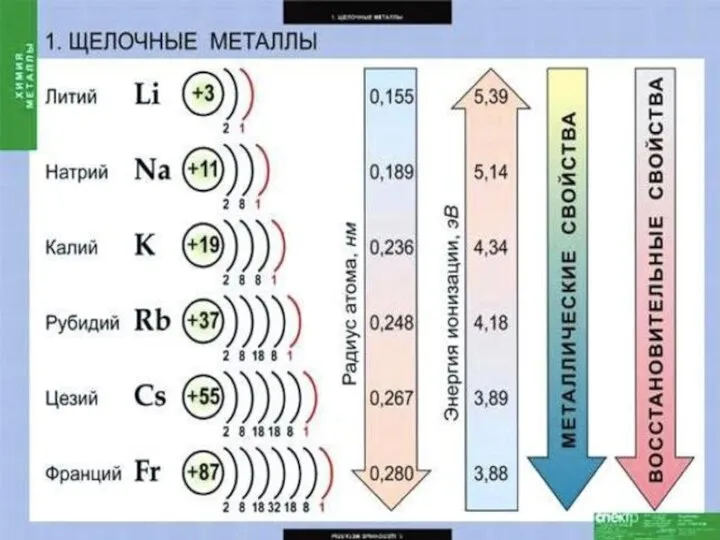
- 3. Щелочные металлы — это элементы главной подгруппы I группы : литий Li, натрий Nа, калий К,
- 5. На внешнем энергетическом уровне атомы этих элементов содержат по одному электрону, находящемуся на сравнительно большом удалении
- 6. Щелочные металлы - простые вещества
- 7. Серебристо-белые мягкие вещества (режутся ножом), с характерным блеском на свежесрезанной поверхности. Все они легкие и легкоплавкие,
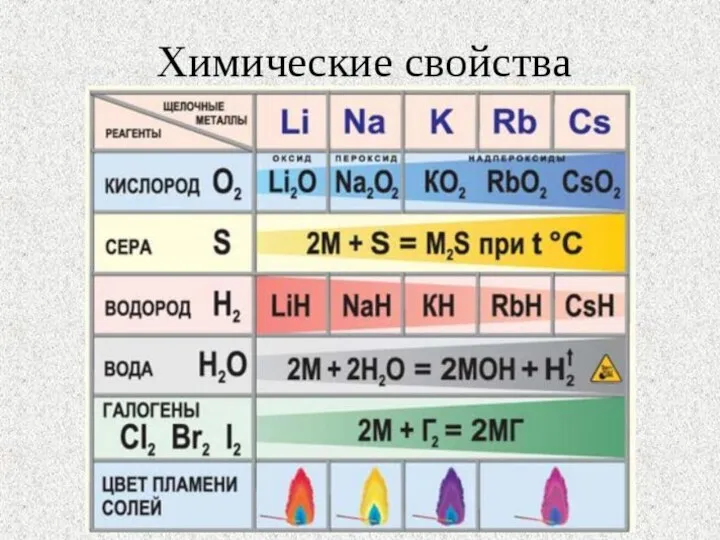
- 9. Химические свойства
- 10. Все щелочные металлы чрезвычайно активны, во всех химических реакциях проявляют восстановительные свойства, отдают свой единственный валентный
- 12. Взаимодействие с неметаллами
- 13. Щелочные металлы легко реагируют с кислородом, но каждый металл проявляет свою индивидуальность: оксид образует только литий:
- 14. Взаимодействие с водородом, серой, фосфором, углеродом, кремнием протекает при нагревании: с водородом образуются гидриды: 2Na +
- 15. С азотом легко реагирует только литий, реакция протекает при комнатной температуре с образованием нитрида лития: 6Li
- 16. Взаимодействие с водой
- 17. Все щелочные металлы реагируют с водой, литий реагирует спокойно, держась на поверхности воды, натрий часто воспламеняется,
- 18. Щелочные металлы способны реагировать с разбавленными кислотами с выделением водорода, однако реакция будет протекать неоднозначно, поскольку
- 19. Соединения щелочных металлов В свободном виде в природе щелочные металлы не встречаются из-за своей исключительно высокой
- 20. Гидроксид натрия NаОН в технике известен под названиями едкий натр, каустическая сода, каустик. Техническое название гидроксида
- 21. Соли щелочных металлов — твердые кристаллические вещества ионного строения. . Nа2СO3 — карбонат натрия, образует кристаллогидрат
- 24. Скачать презентацию



















 Кислоты. Классификация кислот
Кислоты. Классификация кислот Поликарбонат мономерлері
Поликарбонат мономерлері Технология производства органических лекарственных веществ. Препараты алифатического ряда: хлороформ, йодоформ, хлоральгидрат
Технология производства органических лекарственных веществ. Препараты алифатического ряда: хлороформ, йодоформ, хлоральгидрат Арены. Бензол. 9 класс
Арены. Бензол. 9 класс Растворы. Процесс растворения (1)
Растворы. Процесс растворения (1) Химическая промышленность. Аварии на химических предприятиях
Химическая промышленность. Аварии на химических предприятиях Химический анализ. Исследовательская деятельность (8 класс)
Химический анализ. Исследовательская деятельность (8 класс)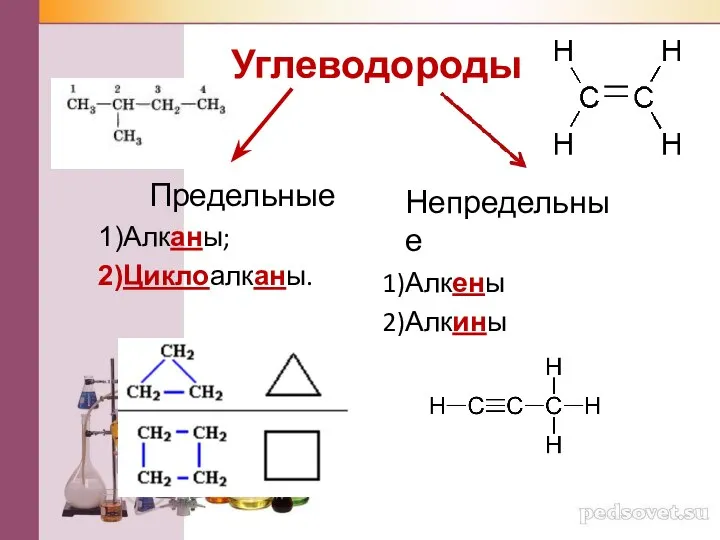 Углеводороды
Углеводороды Смеси и взвеси веществ. Простейшие операции с веществом
Смеси и взвеси веществ. Простейшие операции с веществом Предмет химии. Вещества и их свойства
Предмет химии. Вещества и их свойства Химия. Введение в предмет (8 класс)
Химия. Введение в предмет (8 класс) Презентация по Химии "Фосфор - элемент жизни и мысли"
Презентация по Химии "Фосфор - элемент жизни и мысли"  Химическая связь в молекулах. Экзаменационные вопросы
Химическая связь в молекулах. Экзаменационные вопросы Elektroliz_Gidroliz
Elektroliz_Gidroliz Концентрации растворов и эквиваленты веществ
Концентрации растворов и эквиваленты веществ Вода. Классы неорганических соединений. 8 класс
Вода. Классы неорганических соединений. 8 класс Основные понятия химической термодинамики
Основные понятия химической термодинамики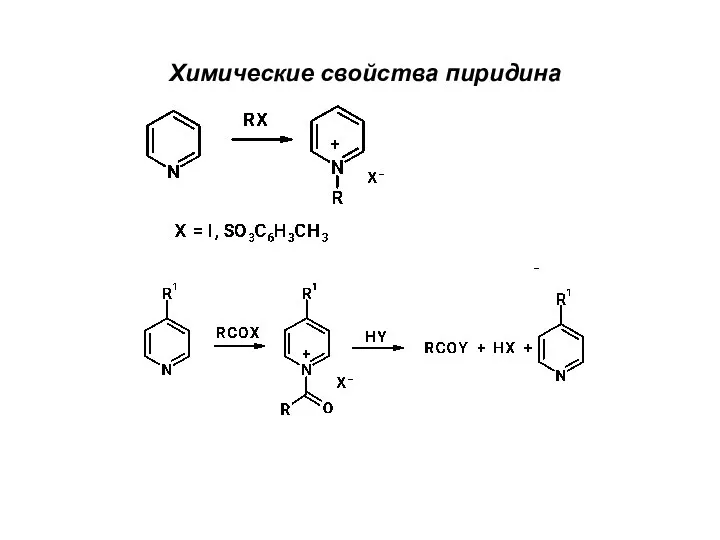 Химические свойства пиридина
Химические свойства пиридина Серная кислота H2SO4
Серная кислота H2SO4 Химические свойства оксидов
Химические свойства оксидов Исследовательский проект. Анализ состава соков разных производителей
Исследовательский проект. Анализ состава соков разных производителей Сахароза
Сахароза Элементы и атомы, В менделеевский взяты круг Сделали химию самой богатой И самой творческой из наук.
Элементы и атомы, В менделеевский взяты круг Сделали химию самой богатой И самой творческой из наук. Презентация на тему Кристаллическая решетка
Презентация на тему Кристаллическая решетка  Применение каучука
Применение каучука Сравнительный анализ Фармакопейных статей для субстанций, представленных в мировых Фармакопеях
Сравнительный анализ Фармакопейных статей для субстанций, представленных в мировых Фармакопеях Конкурс О, химия – ты муза вдохновения!
Конкурс О, химия – ты муза вдохновения! Щелочные металлы
Щелочные металлы