Содержание
- 2. Тема исследования: Скорость химической реакции и её зависимость от условий протекания.
- 3. Понятие скорости (в физике) Скорость- это отношение пройденного пути в единицу времени. V= S/t
- 4. Скорость реакции определяется изменением количества вещества в единицу времени или изменением молярной концентрации вещества за единицу
- 5. Понятие о скорости химической реакции Скорость реакции определяется изменением концентрации одного из реагирующих веществ или одного
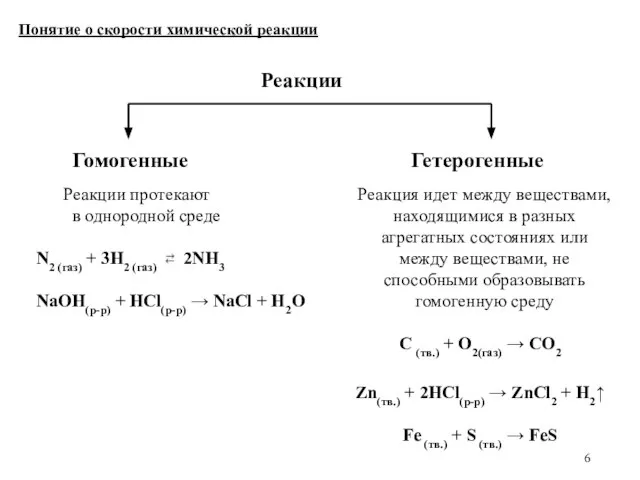
- 6. Понятие о скорости химической реакции Реакции Гомогенные Реакции протекают в однородной среде N2 (газ) + 3H2
- 7. Скорость гетерогенной реакции (υгетер.) определяется изменением количества вещества в единицу времени на единице поверхности соприкосновения веществ
- 8. Факторы, влияющие на скорость: 1.Природа реагирующих веществ HCl Mg Zn
- 9. Факторы, влияющие на скорость 2.Концентрация реагирующих веществ. Zn+CuSO4 (конц) Zn+CuSO4 (разб)
- 10. Концентрация: С повышением концентрации реагирующих веществ увеличивается скорость реакции. Факторы, влияющие на скорость химической реакции Закон
- 11. Для реакции mA + nB = C по закону действующих масс: υ = k ∙ СAm
- 12. Задача 1. Реакция идет по уравнению А +2В → С. Во сколько раз и как изменится
- 13. Факторы, влияющие на скорость 3. Поверхность соприкосновения реагирующих веществ HCl CaCO3 (кусочек) CaCO3 (порошок)
- 14. Факторы, влияющие на скорость Температура H2SO4 H2SO4 + CuO H2SO4 + CuO
- 15. Факторы, влияющие на скорость химической реакции 3. Температура: при повышении температуры на каждые 100 С, скорость
- 16. Дано: υt1 = 1 моль/л ∙ ч γ =3 t1 = 00С t2 = 300С Найти:
- 17. Факторы, влияющие на скорость 5. Наличие катализатора. MnO2 H2O2 H2O2
- 18. 4. Катализаторы – вещества, ускоряющие химические реакции. А + В → С – протекает медленно А
- 19. Скорость химической реакции- это величина, показывающая изменение молярной концентрации в единицу времени. Факторы, влияющие на скорость:
- 20. Мой кластер Скорость реакции
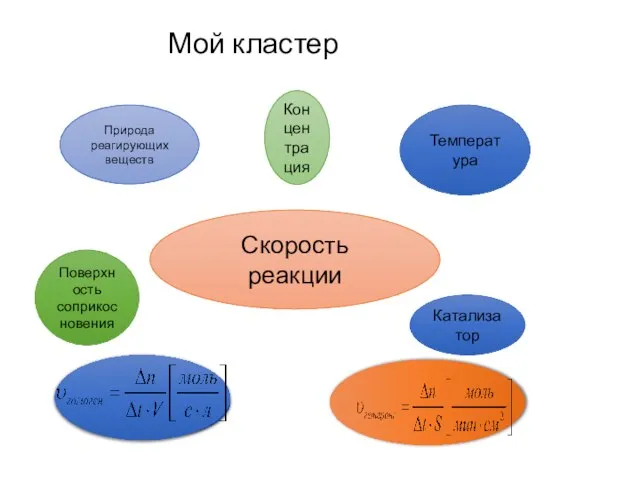
- 21. Мой кластер Скорость реакции Концентрация Природа реагирующих веществ Поверхность соприкосновения Катализатор Температура
- 23. Скачать презентацию

















 Водородная химическая связь
Водородная химическая связь Ионные реакции
Ионные реакции Периодическая система химических элементов Д.И. Менделеева
Периодическая система химических элементов Д.И. Менделеева Получение металлов
Получение металлов Презентация на тему Применение солей в быту
Презентация на тему Применение солей в быту  Полимеры. Применение
Полимеры. Применение Закономерности протеканий химических реакций
Закономерности протеканий химических реакций Строение, свойства, биологическая роль дезоксисахаров и аминосахаров
Строение, свойства, биологическая роль дезоксисахаров и аминосахаров Процессы в растворах: электролитическая диссоциация (ЭД)
Процессы в растворах: электролитическая диссоциация (ЭД) Степень окисления. Составление химических формул бинарных соединений
Степень окисления. Составление химических формул бинарных соединений Лекция 1
Лекция 1 Аминокислоты. Викторина
Аминокислоты. Викторина Презентация на тему "Азотная кислота"
Презентация на тему "Азотная кислота" Общие способы получения металлов
Общие способы получения металлов Физические и химические свойства металлов
Физические и химические свойства металлов Сложные эфиры
Сложные эфиры Примеры реакций в жизни и в быту
Примеры реакций в жизни и в быту Презентация на тему Количество вещества
Презентация на тему Количество вещества  Полисахариды. Крахмал и целлюлоза
Полисахариды. Крахмал и целлюлоза Счастливый случай
Счастливый случай Презентация на тему Знаешь ли ты классы неорганических веществ
Презентация на тему Знаешь ли ты классы неорганических веществ  Кислородосодержащие органические соединения. Cпирты (алканолы)
Кислородосодержащие органические соединения. Cпирты (алканолы) Химические формулы. Относительная молекулярная масса. 8 класс
Химические формулы. Относительная молекулярная масса. 8 класс Решение задач на смеси, растворы и сплавы
Решение задач на смеси, растворы и сплавы Лекция 3
Лекция 3 Харктеристика металлов
Харктеристика металлов Строение вещества
Строение вещества Растворы. Лекция 7
Растворы. Лекция 7