Слайд 2Домашнее задание
таблица + якласс

Слайд 3 назовите
H3С - CH 2 -CH2 - OH
CH 3 –CH -
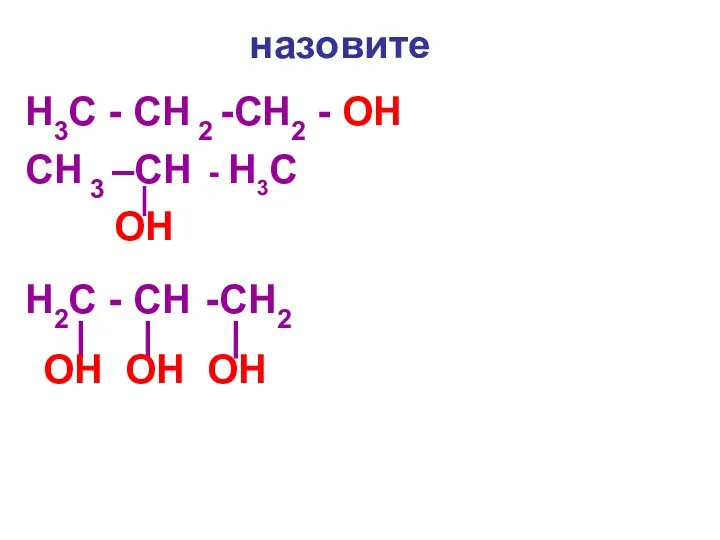
H3С
|
OH
H2С - CH -CH2
| | |
OH OH OH
Слайд 4
Номенклатура
Название углеводорода + ОЛ +
номер атома С с группой
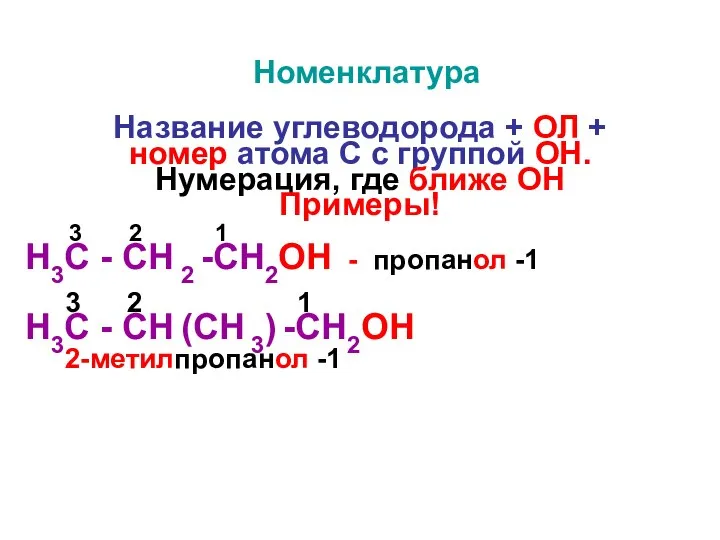
ОН.
Нумерация, где ближе ОН
Примеры!
3 2 1
H3С - CH 2 -CH2OH - пропанол -1
3 2 1
H3С - CH (CH 3) -CH2OH
2-метилпропанол -1
Слайд 5 проверьте
H3С - CH 2 -CH2 - OH - пропанол -1
CH3 –CH
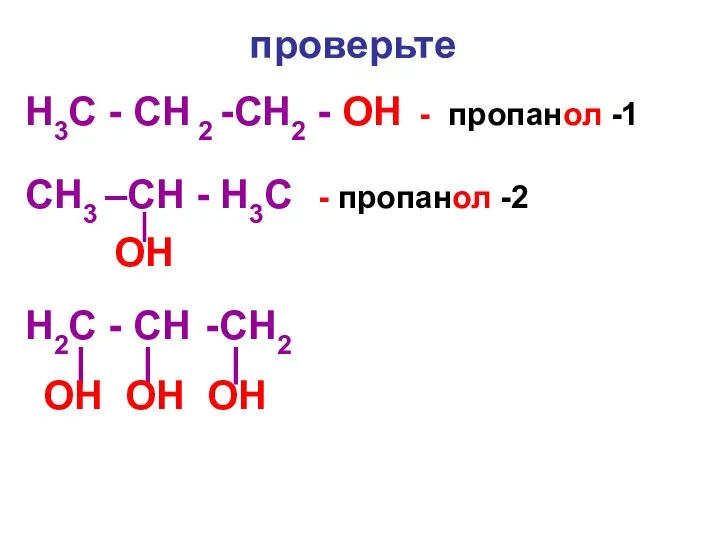
- H3С - пропанол -2
|
OH
H2С - CH -CH2
| | |
OH OH OH
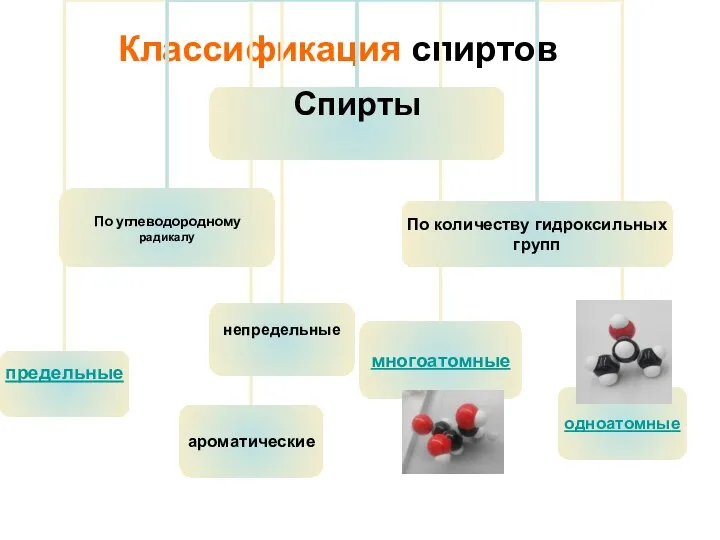
Слайд 6Классификация по …
H3С - CH 2 -CH2OH - пропанол -1
одноатомный спирт
CH
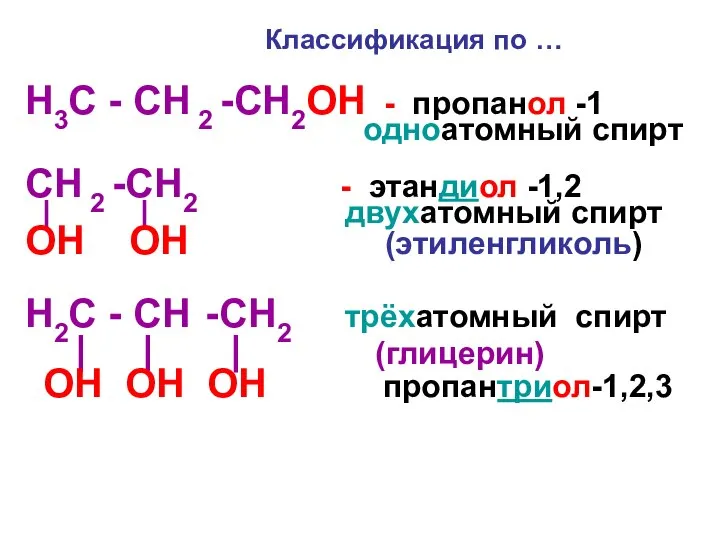
2 -CH2 - этандиол -1,2
| | двухатомный спирт
OH OH (этиленгликоль)
H2С - CH -CH2 трёхатомный спирт
| | | (глицерин)
OH OH OH пропантриол-1,2,3
Слайд 7Тема урока
«Глицерин как представитель предельных многоатомных спиртов»

Слайд 9 Влияет ли увеличение числа групп ОН на свойства спиртов?

Слайд 10Закон взаимного перехода количественных изменений в качественные
Диалектика –наука об общих законах

природы и общества
Слайд 11Физические свойства этанола
Молекулярная формула - CH 3 -CH2OH
Молярная масса – 46

г/моль
Внешний вид – жидкость с характерным запахом
Растворимость в воде – неограниченно
Температура плавления - −114,3 °C
Температура кипения - 78,4 °C
Физиологическое действие - наркотик
Родственные спирты – метанол (Яд!!!), пропанол, бутанол
Слайд 12Химические свойства
1Взаимодействует со щелочными металлами с образованием этилатов (или в общем случае

— алкоголятов) и водорода.
2C2H5OH + 2К = 2С2Н5ОК + Н2
2. Вступает в реакцию дегидратации в присутствии серной кислоты (при 120 °C) с образованием диэтилового эфира☹Серная кислота)
2CH3CH2 –O-H → CH3CH2-O-CH2CH3 + H2O
CH3CH2-OH → CH2=CH2 + H2O (t >140 °C)
3. Сгорает на воздухе и в кислороде с выделением тепла:
C2H5OH + 3O2 → 2CO2 + 3H2O +Q
4. Реагирует с карбоновыми кислотами с образованием сложных эфиров:
RCOOH + HOCH2CH3 → RCOOCH2CH3 + H2O
Слайд 13Химические свойства
5. Взаимодействует с гидридами щелочных металлов с образованием этилатов:
CH3CH2OH +

NaH → CH3CH2ONa + H2
6. Вступает в реакцию гидрогалогенирования в присутствии хлорида цинка:
CH3CH2OH + HCl → CH3CH2Cl + H2O
7.!!!!! Качественная реакция
(с медной проволокой)
Окисляется до альдегидов ( t)
CH3CH2OH + CuO → CH3 –CHO + Cu + H2O
этаналь
Слайд 14Работа в группах
Цель:
На основе экспериментальных данных изучить некоторые физические и химические

свойства глицерина в сравнении с пропанолом-2;
Проверить, «работает» ли в химии закон диалектики перехода количественных изменений в качественные
Слайд 15Докажите или опровергните утверждения о свойствах спиртов
1 группа
Глицерин и пропанол-2 –жидкости с

характерным запахом
Глицерин и пропанол-2 хорошо растворимы в воде
Растворение сопровождается разогреванием растворов
Слайд 16Докажите или опровергните утверждения о свойствах спиртов
2 группа
С увеличением молекулярной массы

температура кипения спиртов увеличивается.
Ответ подтвердите графиком зависимости температуры кипения от относительной молекулярной массы
Слайд 17Докажите или опровергните утверждения о свойствах спиртов
3 группа
Растворы глицерина и пропанола-2

не проводят электрический ток, то есть не являются электролитами
Так как в молекулах выданных веществ содержатся гидроксильные группы, следовательно их растворы имеют щелочную среду
Слайд 18Докажите или опровергните утверждения о свойствах спиртов
4 группа
Глицерин и пропанол-2 взаимодействуют

с щелочными металлами
Образующийся газ –Н2
Слайд 19Докажите или опровергните утверждения о свойствах спиртов
5 группа
Глицерин и пропанол-2 окисляются

оксидом меди (II)
Слайд 20Сравнительная характеристика
изопропилового спирта и глицерина



















 Азотная кислота
Азотная кислота Окислительно-восстановительные реакции (ОВР)
Окислительно-восстановительные реакции (ОВР) Игра Что? Где? Когда?. Химия
Игра Что? Где? Когда?. Химия Обратимость химических реакций. Химическое равновесие
Обратимость химических реакций. Химическое равновесие Индиго-краситель
Индиго-краситель Растительные источники жиров и жирных масел
Растительные источники жиров и жирных масел Макро- и микромир
Макро- и микромир Коррозия металлов
Коррозия металлов Сказка о братьях карбонатах
Сказка о братьях карбонатах Взаимодействие атомов элементов-неметаллов между собой
Взаимодействие атомов элементов-неметаллов между собой Полиамиды (ПА)
Полиамиды (ПА) Фосфориты. Добыча фосфоритов
Фосфориты. Добыча фосфоритов Способы выражения концентраций растворов
Способы выражения концентраций растворов Кислородсодержащие органические соединения
Кислородсодержащие органические соединения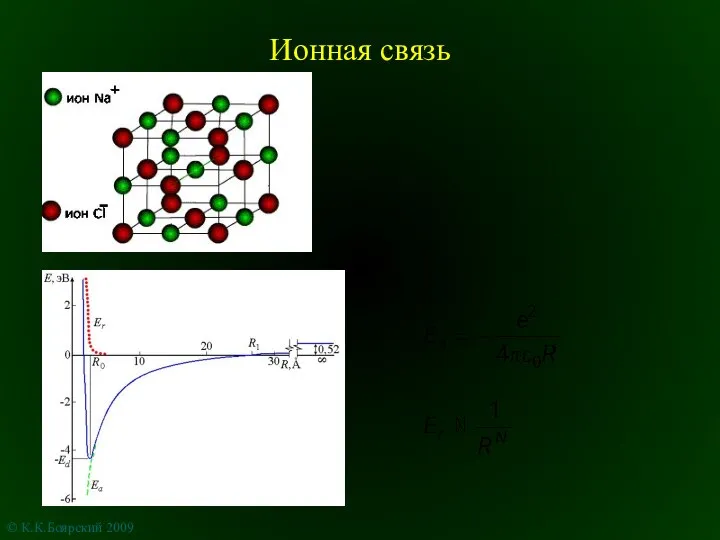 Ионная связь
Ионная связь Оңай балқитын флюстерді қолдана отырып хромкенді шекемтастар алу мүмкіндігін зерттеу
Оңай балқитын флюстерді қолдана отырып хромкенді шекемтастар алу мүмкіндігін зерттеу Карбоновые кислоты, их строение, номенклатура, получение и свойства
Карбоновые кислоты, их строение, номенклатура, получение и свойства Уравнение состояния идеального газа
Уравнение состояния идеального газа Шаблон для презентации по химии
Шаблон для презентации по химии Перициклические реакции
Перициклические реакции Оңай балқитын флюстерді қолдана отырып хромкенді шекемтастар алу мүмкіндігін зерттеу
Оңай балқитын флюстерді қолдана отырып хромкенді шекемтастар алу мүмкіндігін зерттеу Катализ в нефтепереработке
Катализ в нефтепереработке Органические галогениды. (Лекция 7)
Органические галогениды. (Лекция 7) Составление уравнений окислительно-восстановительных реакций
Составление уравнений окислительно-восстановительных реакций Жиры
Жиры Скорость химических реакций
Скорость химических реакций 1666603286718__4v20ts
1666603286718__4v20ts Основы МКТ
Основы МКТ