Содержание
- 2. Разделы лекционного курса
- 3. В V веке до нашей эры Левкипп и Демокрит первыми употребили слово «атом» для обозначения мельчайших
- 4. Изучая атмосферу и движение воздуха, Дальтон пришел к выводу, противоречащему убеждениям ведущих химиков того времени, включая
- 5. М. Фарадей установил, что ток в растворе электролита это упорядоченное движение заряженных частиц – ионов. Большую
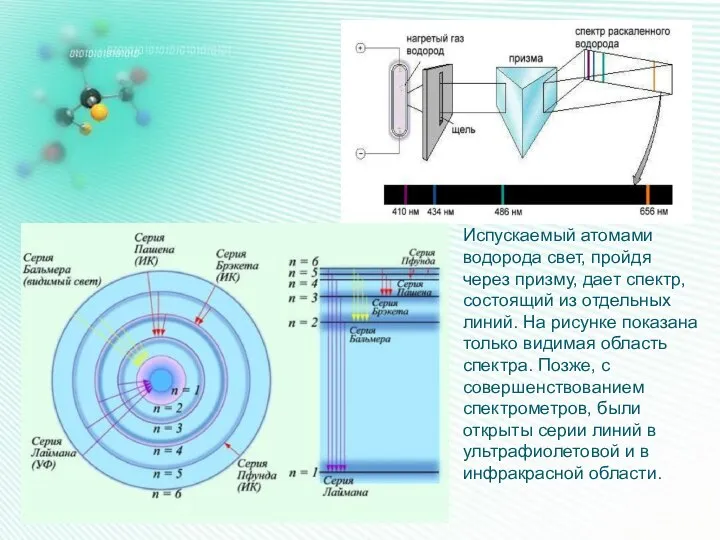
- 6. Испускаемый атомами водорода свет, пройдя через призму, дает спектр, состоящий из отдельных линий. На рисунке показана
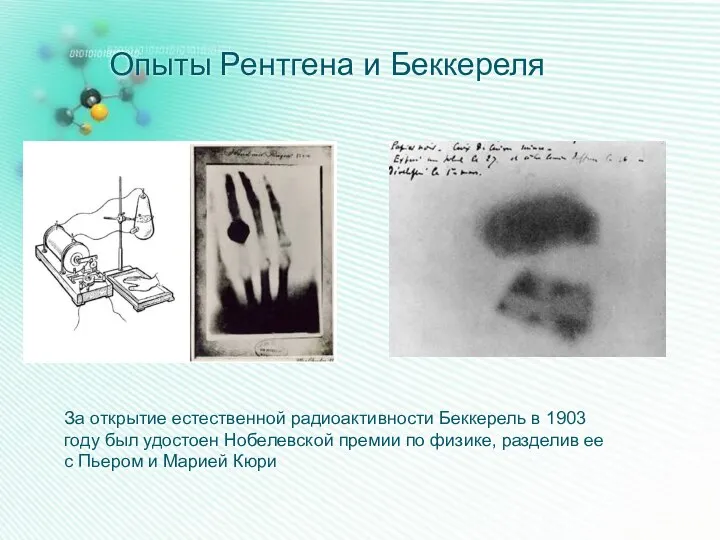
- 7. Опыты Рентгена и Беккереля За открытие естественной радиоактивности Беккерель в 1903 году был удостоен Нобелевской премии
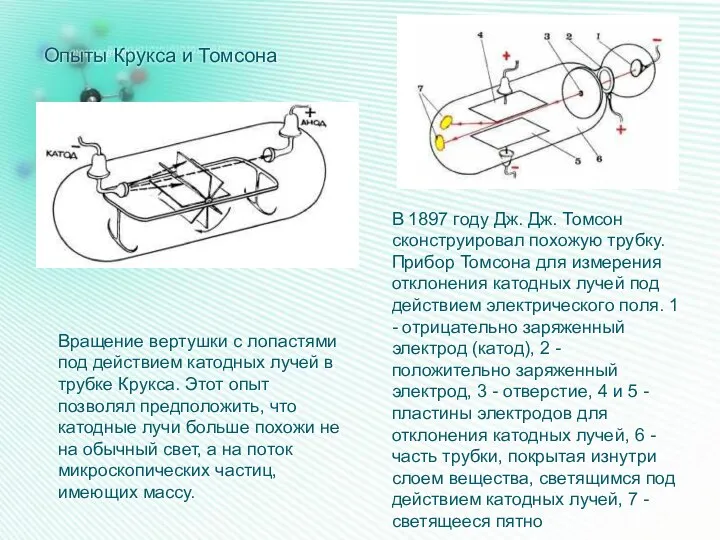
- 8. Опыты Крукса и Томсона Вращение вертушки с лопастями под действием катодных лучей в трубке Крукса. Этот
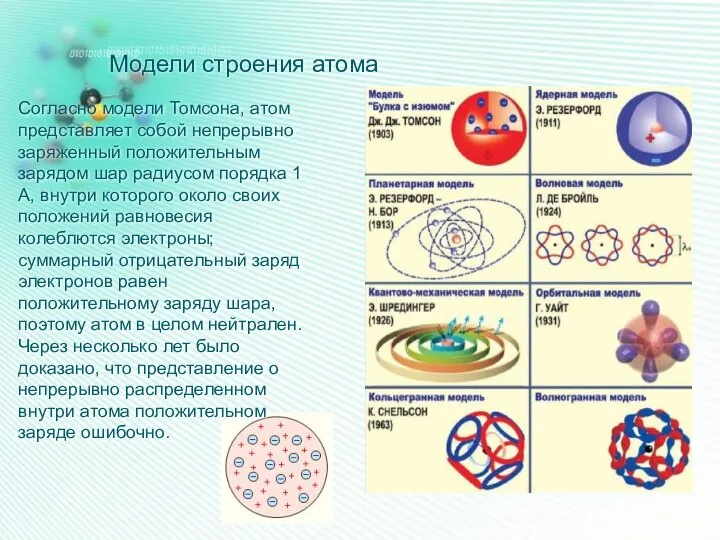
- 9. Модели строения атома Согласно модели Томсона, атом представляет собой непрерывно заряженный положительным зарядом шар радиусом порядка
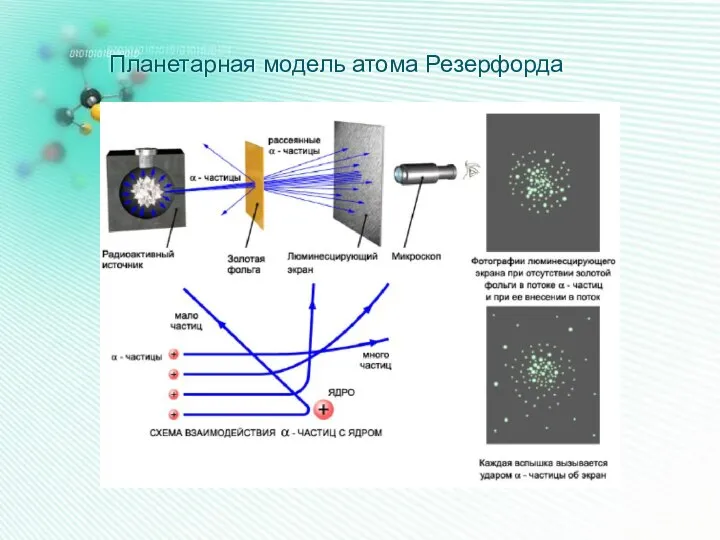
- 10. Планетарная модель атома Резерфорда
- 11. Постулаты Н. Бора
- 12. Квантово-механические принципы строения вещества
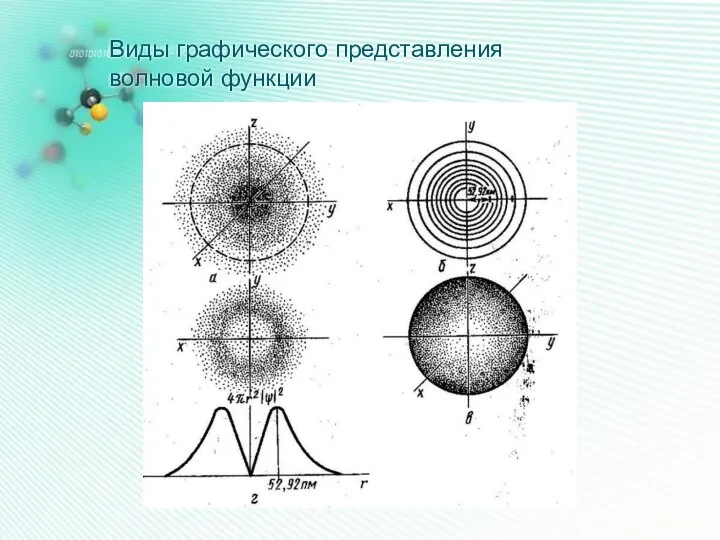
- 13. Виды графического представления волновой функции
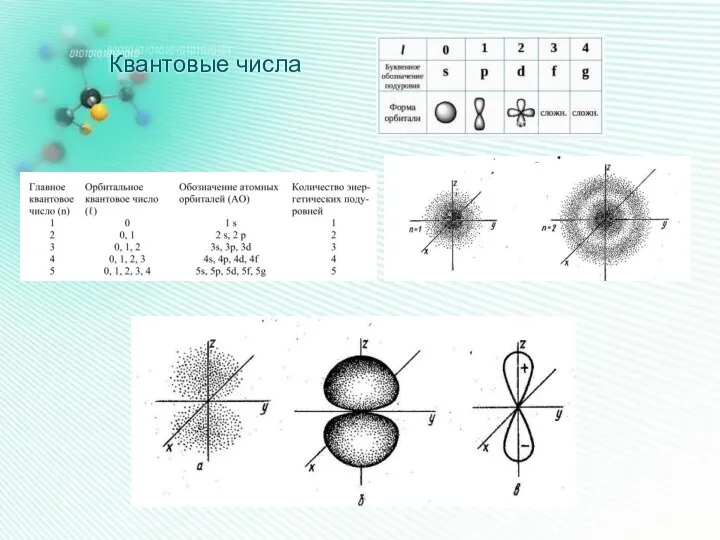
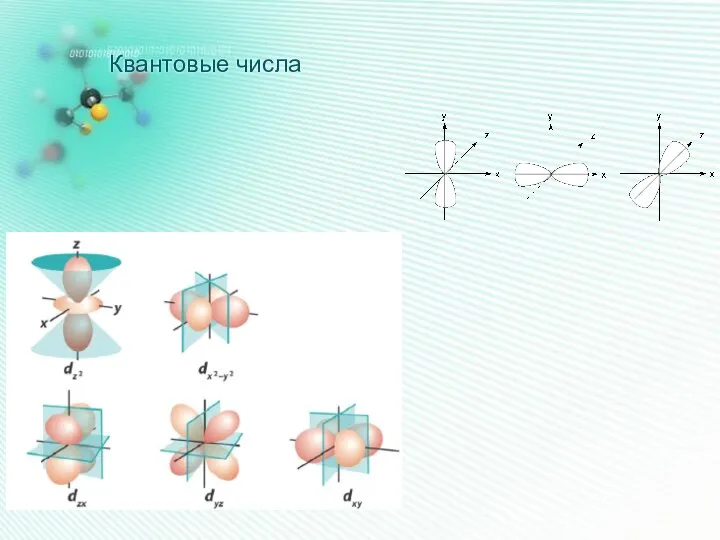
- 14. Квантовые числа
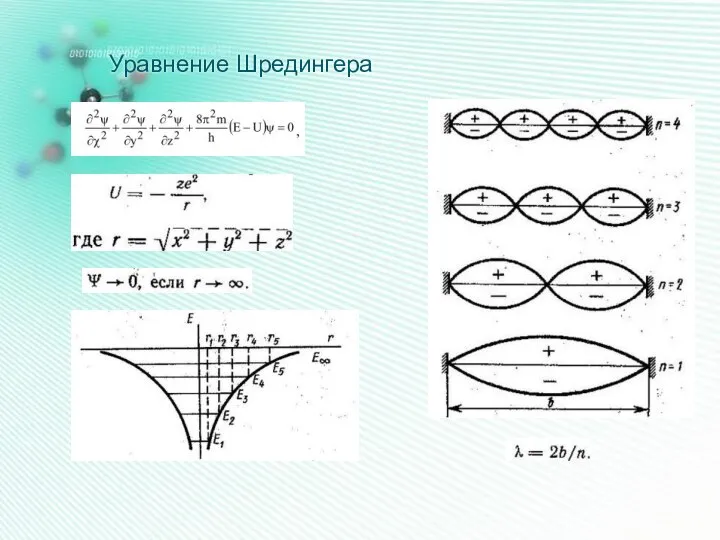
- 15. Уравнение Шредингера
- 16. Квантовые числа
- 17. Квантовые числа
- 19. Скачать презентацию







 Химическое равновесие
Химическое равновесие Химия и география. Блиц-опрос. 7 класс
Химия и география. Блиц-опрос. 7 класс Амилаза. Строение амилазы
Амилаза. Строение амилазы Моющие и чистящие средства
Моющие и чистящие средства Основные химические законы
Основные химические законы Соли: получение
Соли: получение Синтетическое моторное масло. Маркировка моторных масел
Синтетическое моторное масло. Маркировка моторных масел Khim_8
Khim_8 Химические реакции
Химические реакции Систематизация знаний по периодической системе химических элементов
Систематизация знаний по периодической системе химических элементов химия
химия Nevarne snovi
Nevarne snovi Основания. Классификация
Основания. Классификация Стелс-материалы
Стелс-материалы Тип кристаллической решетки у белого фосфора…. Тест
Тип кристаллической решетки у белого фосфора…. Тест Классификация и свойства кислот
Классификация и свойства кислот Сeквенирование нуклеиновых кислот
Сeквенирование нуклеиновых кислот Набор для выращивания монокристалла. Защита проекта
Набор для выращивания монокристалла. Защита проекта Алканы. Строение, номенклатура, изомерия, физические свойства
Алканы. Строение, номенклатура, изомерия, физические свойства Реакции разложения и соединения
Реакции разложения и соединения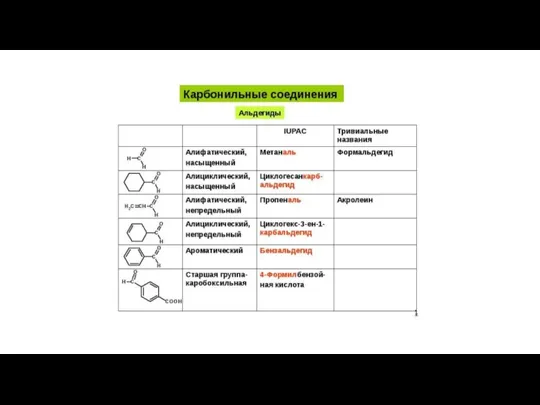 Карбонильные соединения (альдегиды)
Карбонильные соединения (альдегиды) карбоновые кислоты
карбоновые кислоты Вуглеводи. Групи
Вуглеводи. Групи Вычисление температур стеклования полимера при различных степенях отверждения смолы
Вычисление температур стеклования полимера при различных степенях отверждения смолы Сера
Сера Валенттілік. Атом-молекулалы ілім
Валенттілік. Атом-молекулалы ілім Классификация органических соединений
Классификация органических соединений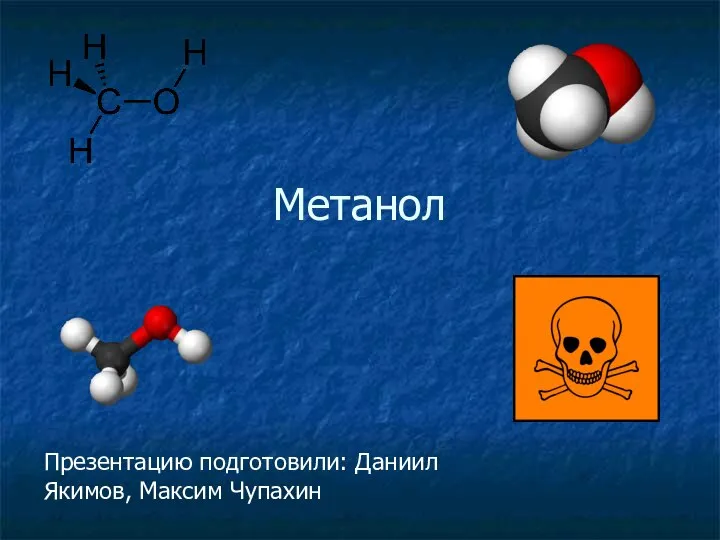 Метанол. Краткая характеристика
Метанол. Краткая характеристика