Содержание
- 2. Т1 Строение атома и ПСХЭ
- 3. А1 Строение атома 13Al +13 2,8,3 3 период 2+8+3=13 Р (е)=13 N = 27-13=14 27 K
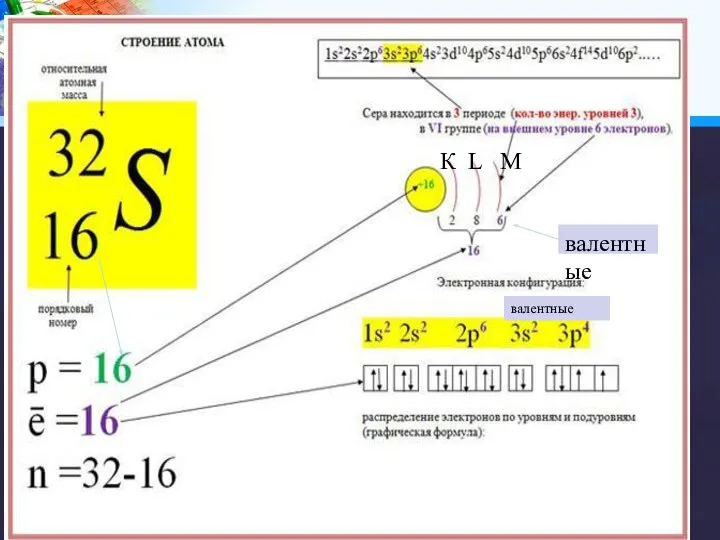
- 4. К L М валентные валентные
- 5. 4 период 6 группа главная подгруппа 34Se +34 2, 8, 18, 6 4период 7 группа побочная
- 8. №1 Ответ 1-бор Ответ -2
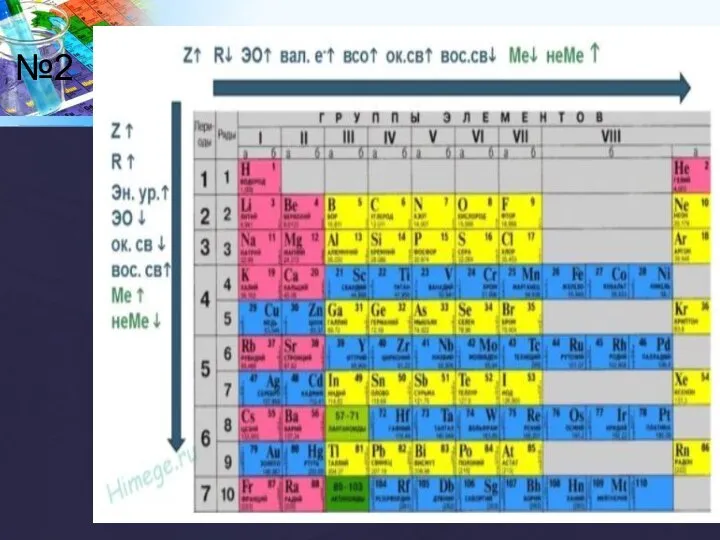
- 9. Закономерности изменения химических свойств элементов и их соединений по периодам и группам. Необходимо запомнить: Физический смысл
- 10. №2
- 11. Ответ 3 Ответ 1
- 13. Ответ 34
- 14. 1. Учебный тренажер содержит 20 заданий В-1 с кратким ответом. 2. Задание считается выполненным верно, если
- 15. 1. В ряду химических элементов О → S → Sе: уменьшается радиус атома уменьшается электроотрицательность усиливаются
- 16. 2. В ряду химических элементов Na → Al → P происходит увеличение (усиление): числа нейтронов в
- 17. 3. В ряду химических элементов Cl → Si → Al: уменьшаются заряды ядер атомов возрастают кислотные
- 18. 4. В ряду химических элементов Sе → S → О: уменьшается валентность в высших оксидах возрастают
- 19. 5. В ряду химических элементов Si → Р → S: уменьшается число протонов в ядре уменьшается
- 20. 6. В ряду химических элементов Ве → Мg → Са: уменьшается радиус атомов возрастает способность атомов
- 21. 7. В ряду химических элементов N → Р → Аs: уменьшается электроотрицательность уменьшаются радиусы атомов ослабевают
- 22. 8. В порядке ослабевания металлических свойств расположены элементы в рядах: Be → Mg → Ca Na
- 23. 9. Способность отдавать электроны возрастает у элементов следующих рядов: уменьшается число протонов в ядре уменьшается электроотрицательность
- 24. 10. В ряду химических элементов Al → Mg →Na: усиливается электроотрицательность усиливаются металлические свойства усиливается основный
- 25. 11. В ряду химических элементов N → С → В: увеличивается число протонов в ядре увеличивается
- 26. 12. В порядке уменьшения числа электронов во внешнем слое расположены элементы следующих рядов: N → O
- 27. 13. В ряду химических элементов Si → Ge → Sn: увеличивается радиус атома ослабевают металлические свойства
- 28. 14. В ряду химических элементов Cl → S → P → Si: увеличиваются неметаллические свойства уменьшается
- 29. 15. В ряду химических элементов Si → Аl → Мg: уменьшается электроотрицательность увеличиваются заряды ядер атомов
- 30. 16. В ряду химических элементов Cl → P → Si: уменьшаются заряды ядер атомов уменьшается число
- 31. 17. В ряду химических элементов I → Вr → Сl: увеличивается степень окисления в высших оксидах
- 32. 18. В ряду химических элементов F → О → N: увеличивается число электронных слоев уменьшаются заряды
- 33. 19. В ряду химических элементов Аl → Р → Сl: увеличивается электроотрицательность уменьшаются заряды ядер атомов
- 35. Скачать презентацию






























 Презентация на тему Кристаллы
Презентация на тему Кристаллы  Классификация химических реакций по различным основаниям
Классификация химических реакций по различным основаниям Сера и ее соединения
Сера и ее соединения Презентация на тему Фолиевая кислота
Презентация на тему Фолиевая кислота  Химические свойства
Химические свойства Свойства кислорода. Оксиды
Свойства кислорода. Оксиды Термореактивные пластмассы (реактопласты)
Термореактивные пластмассы (реактопласты) Диссоциация. Уравнения диссоциации
Диссоциация. Уравнения диссоциации Бирюза. Характеристики минерала
Бирюза. Характеристики минерала Применение эфиров в производстве автомобильных бензинов
Применение эфиров в производстве автомобильных бензинов Презентация по Химии "Алканолы"
Презентация по Химии "Алканолы"  ОВР - метод полуреакции
ОВР - метод полуреакции 20170625_otkrytyy_integrirovannyy_urok_himiya-geografiya
20170625_otkrytyy_integrirovannyy_urok_himiya-geografiya 175 – летию со дня рождения Дмитрия Ивановича Менделеева посвящается… АВТОР ПРЕЗЕНТАЦИИ: учитель химии МОУ СОШ №2 города Ртищево Саратовской области ПОПКОВА Е.Г.
175 – летию со дня рождения Дмитрия Ивановича Менделеева посвящается… АВТОР ПРЕЗЕНТАЦИИ: учитель химии МОУ СОШ №2 города Ртищево Саратовской области ПОПКОВА Е.Г. Изомерия
Изомерия Сера и его соединения
Сера и его соединения Алкены-2 (электрофильные реакции)
Алкены-2 (электрофильные реакции) Застосування рідких кристалів
Застосування рідких кристалів Электролиз
Электролиз Астат. Свойства астата
Астат. Свойства астата Железо как химический элемент
Железо как химический элемент Золото (Au)
Золото (Au) Распределение электронов в атоме по энергетическим уровням
Распределение электронов в атоме по энергетическим уровням Трёхкомпонентные системы. Закон распределения. Экстракция. Свойства разбавленных растворов неэлектролитов
Трёхкомпонентные системы. Закон распределения. Экстракция. Свойства разбавленных растворов неэлектролитов Металлы. Своя игра
Металлы. Своя игра Научно-познавательное шоу Юный химик
Научно-познавательное шоу Юный химик Роль М.В. Ломоносова и Дж. Дальтона в создании атомно-молекулярного учения
Роль М.В. Ломоносова и Дж. Дальтона в создании атомно-молекулярного учения Bioenergetyka syntezy glutaminy
Bioenergetyka syntezy glutaminy