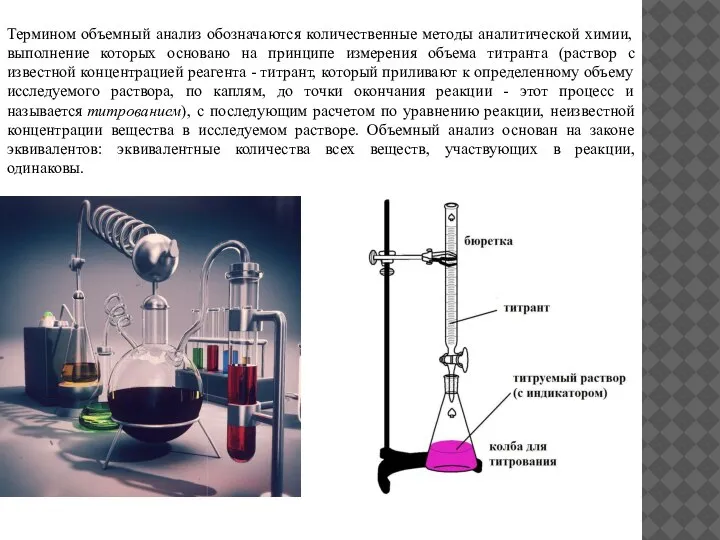
распространение получил метод кислотно-основного титрования (метод нейтрализации), в котором при анализе раствора кислоты титрантом служит раствор щелочи (ацидиметрия), а при анализе раствора щелочи титрантом служит раствор кислоты (алкалиметрия). Точка эквивалентности (конечная точка титрования) устанавливается с помощью кислотно-основных индикаторов; для сильных кислот и оснований в точке эквивалентности образуется нейтральный раствор (рН = 7). При расчетах по результатам кислотно-основного титрования исходят из того, что объемы исследуемого раствора Vp. вещества B и титранта, содержащего вещество А, в точке эквивалентности обратно пропорциональны нормальностям этих растворов N:
Используя эти соотношения, находят нормальность раствора исследуемого вещества B. Массу вещества B, растворенного в заданном объеме исследуемого раствора Vp.B, рассчитывают по уравнению:
где MeqB - эквивалентная масса вещества B, равная произведению молярной массы MB на фактор эквивалентности этого вещества feqB. Для расчета массы вещества B удобно применять соотношение, получаемое из двух предыдущих выражений:
Таким образом, по известной нормальности титранта (раствора вещества А) и использованному на титрование объему титранта находят массу растворенного вещества во взятом объеме исследуемого раствора.


 Неделя химии в МБОУ (викторина)
Неделя химии в МБОУ (викторина) Свойства основных липопротеинов (ЛП) плазмы крови
Свойства основных липопротеинов (ЛП) плазмы крови Углеводы
Углеводы Топология кристаллических структур. Топологические типы. Программы и базы данных для анализа топологии. Лекция 9
Топология кристаллических структур. Топологические типы. Программы и базы данных для анализа топологии. Лекция 9 Электролитическая диссоциация. Электролиты и неэлектролиты
Электролитическая диссоциация. Электролиты и неэлектролиты Неметаллы в ПСХЭ
Неметаллы в ПСХЭ Органическая химия. Теория строения органических веществ
Органическая химия. Теория строения органических веществ Строение атома
Строение атома Презентация 1
Презентация 1 Теория активированного комплекса
Теория активированного комплекса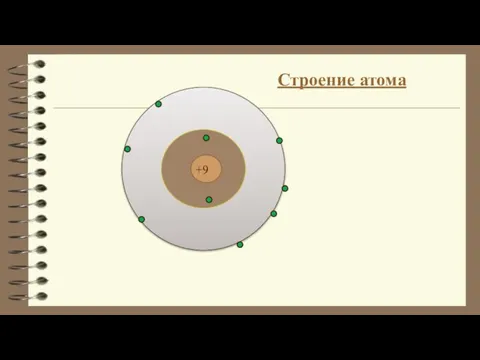 Строение атома
Строение атома Кислоты в химии
Кислоты в химии Природные источники углеводородов
Природные источники углеводородов Природные кислоты и щелочи. Индикаторы
Природные кислоты и щелочи. Индикаторы Закалка и отпуск стали. Ознакомление со структурами серого и белого чугуна. Распознавание руд железа
Закалка и отпуск стали. Ознакомление со структурами серого и белого чугуна. Распознавание руд железа Химическая технология. Структура ВКР
Химическая технология. Структура ВКР Интеллектуальная игра по химии «Металлы»
Интеллектуальная игра по химии «Металлы» Аминокислоты и их применение
Аминокислоты и их применение Углеволокно (карбон)
Углеволокно (карбон) Спирты (алканолы)
Спирты (алканолы) Дисперсные системы в пищевой промышленности
Дисперсные системы в пищевой промышленности Фосфор
Фосфор Пересчет данных анализа, выраженных в ионной форме
Пересчет данных анализа, выраженных в ионной форме Степень окисления. Составление формул бинарных соединений
Степень окисления. Составление формул бинарных соединений Металлы тоже воевали… 8 класс
Металлы тоже воевали… 8 класс Презентация на тему Серебро
Презентация на тему Серебро  Классификация химических реакций
Классификация химических реакций Sinteticheskie_Materialy_I_Ikh_Rol_1
Sinteticheskie_Materialy_I_Ikh_Rol_1