Содержание
- 2. 1. Що таке вуглеводні? 2. На які групи вони поділяються? 3. Загальна формула насичених вуглеводнів? 4.
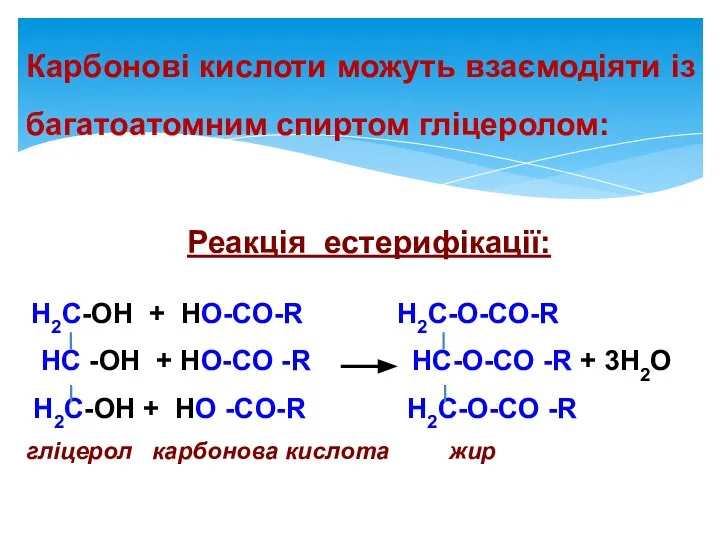
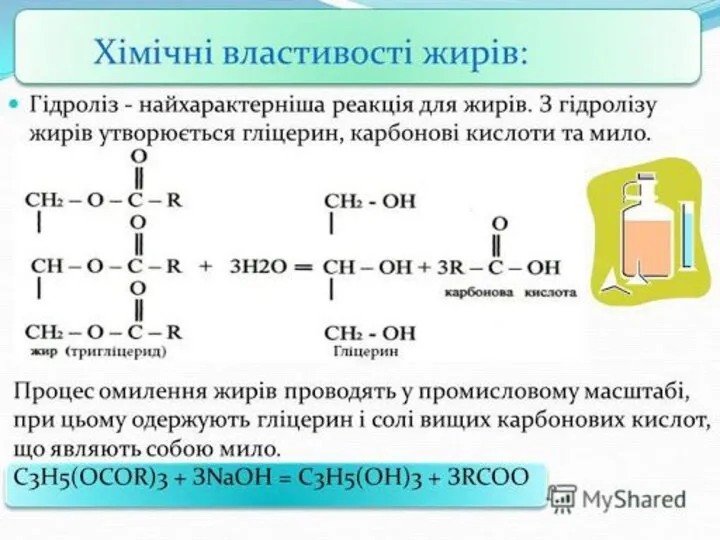
- 3. Карбонові кислоти можуть взаємодіяти із багатоатомним спиртом гліцеролом: H2C-OH + HO-CO-R H2C-O-CO-R HC -OH + HO-CO
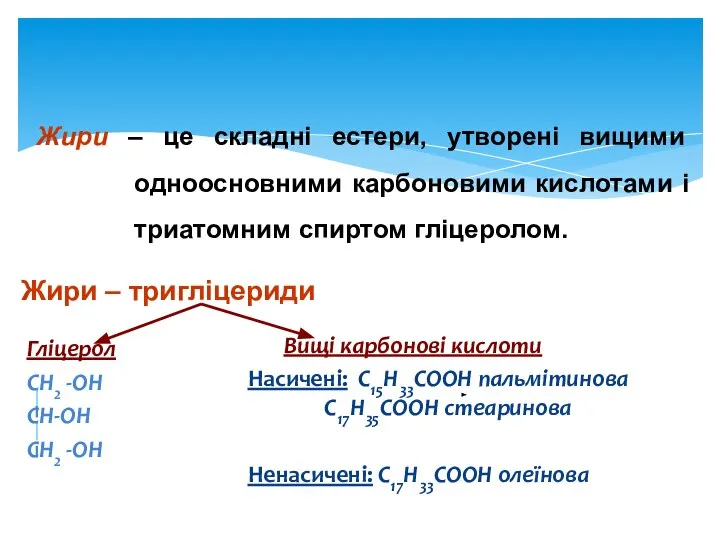
- 4. Жири – це складні естери, утворені вищими одноосновними карбоновими кислотами і триатомним спиртом гліцеролом. Гліцерол СН2
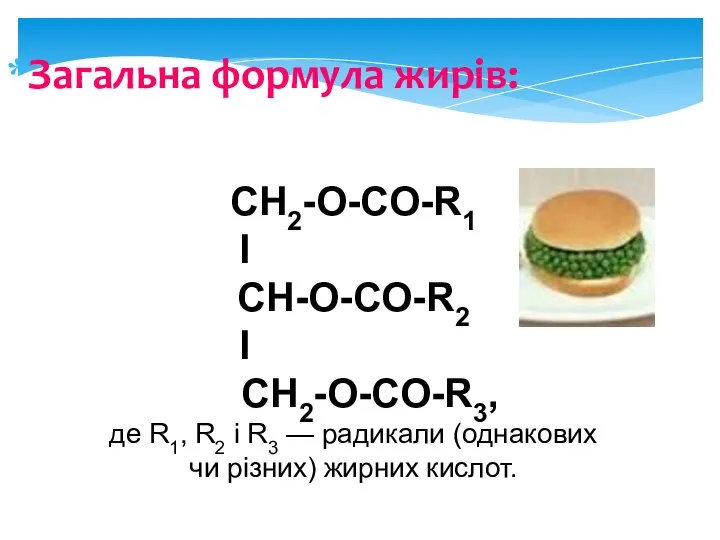
- 5. Загальна формула жирів: CH2-O-CO-R1 I CH-О-CO-R2 I CH2-O-CO-R3, де R1, R2 і R3 — радикали (однакових
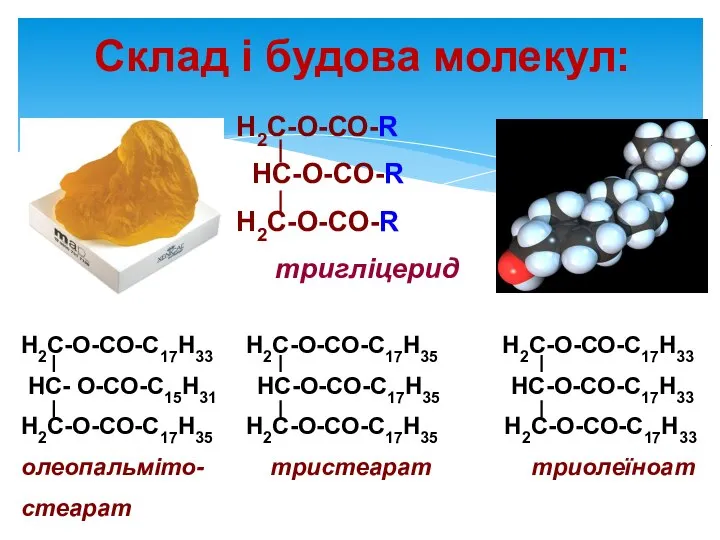
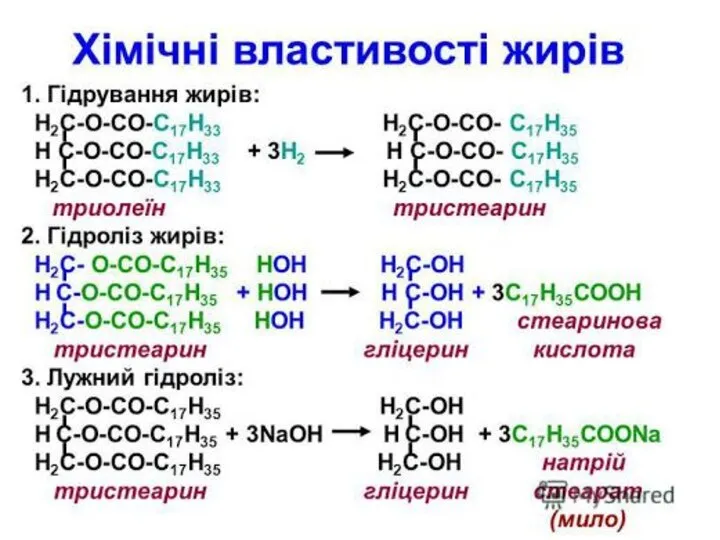
- 6. Склад і будова молекул: Н2С-О-СО-С17Н33 Н2С-О-СО-С17Н35 Н2С-О-СО-С17Н33 НС- О-СО-С15Н31 НС-О-СО-С17Н35 НС-О-СО-С17Н33 Н2С-О-СО-С17Н35 Н2С-О-СО-С17Н35 Н2С-О-СО-С17Н33 олеопальміто- тристеарат
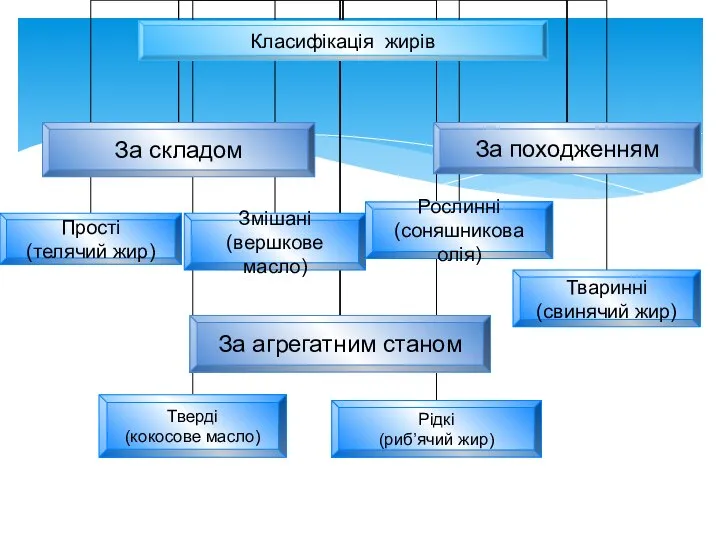
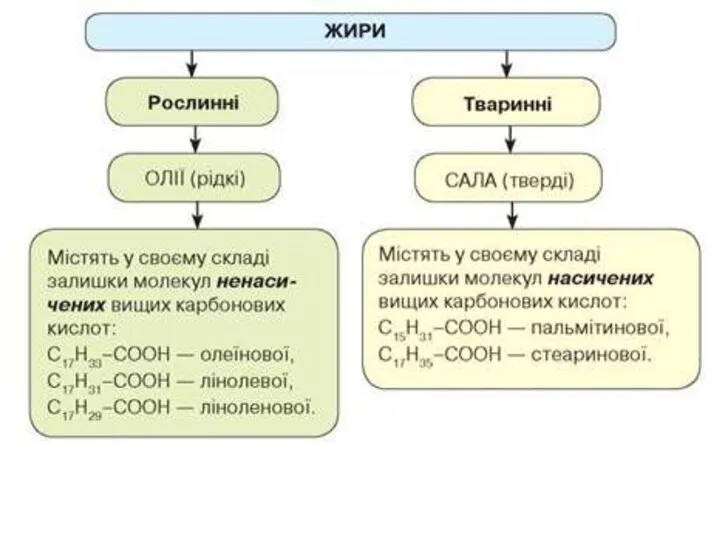
- 9. Приклади жирів: Тверді – тваринного походження (утворені насиченими карбоновими кислотами) Рідкі – рослинного походження (утворені ненасиченими
- 10. Приклади жирів: Жири тваринні: вершкове масло, свиняче сало, риб’ячий жир, баранячий лій. Рослинні жири: оливкова, соєва,
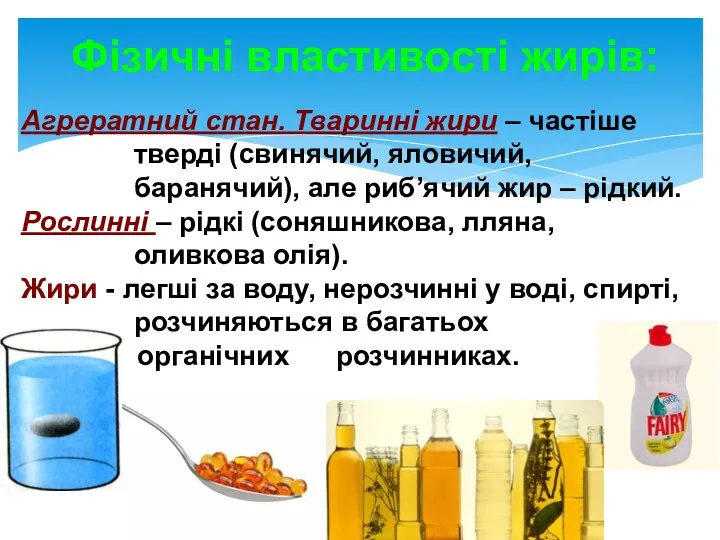
- 11. Фізичні властивості жирів: Агрератний стан. Тваринні жири – частіше тверді (свинячий, яловичий, баранячий), але риб’ячий жир
- 12. Жири не розчиняються у холодній воді. При нагріванні води розчинність зростає Жири не розчиняються у спирті.
- 15. Продукт гідрогенізації олії - твердий жир (штучне сало, саломас). Маргарин - харчовий жир, складається із суміші
- 17. Жири отримують: Витоплюванням Екстрагуванням Пресуванням Сепаруванням Гідруванням жирів в техніці.
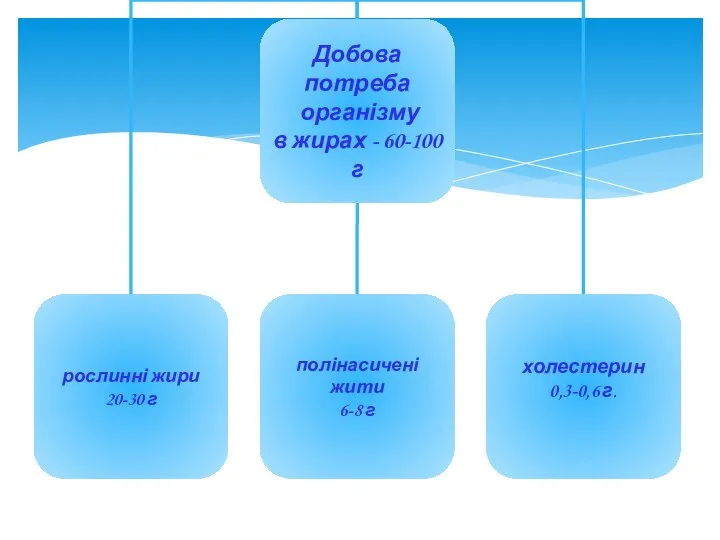
- 18. Біологічне значення жирів: Жири - джерело енергії. Жири забезпечують 25-30 % всієї енергії необ-хідної для організму
- 19. У тварин та рослин жири головним чином відіграють роль покриття, що відштовхує воду Покривають шкіру, шерсть
- 23. Біологічні функції жирів: Энергетична повне окислення 1г жиру дає 38,9 кДж енергії Будівельна Теплоізоляційна Джерело метаболічної
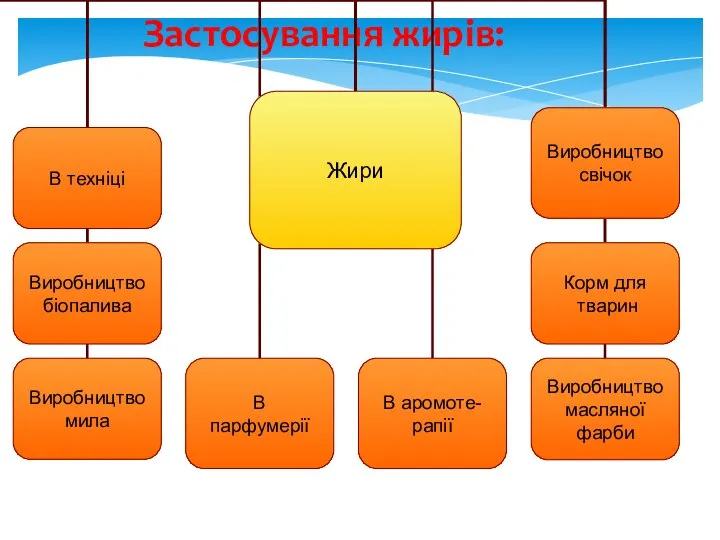
- 24. Застосування жирів:
- 26. Скачать презентацию












 Полимеры с включением атомов бора и карборановой группировки - полиборорганосилоксаны и поликарборанорганосилосксаны
Полимеры с включением атомов бора и карборановой группировки - полиборорганосилоксаны и поликарборанорганосилосксаны Химия и сельское хозяйство
Химия и сельское хозяйство Оксидтер мен негіздердің реакциялары
Оксидтер мен негіздердің реакциялары Алгоритмы при изучении химии
Алгоритмы при изучении химии Презентация на тему Витамины. Урок химии 10 класс
Презентация на тему Витамины. Урок химии 10 класс  Алкины и их свойства
Алкины и их свойства Химия и автомобиль
Химия и автомобиль Углеводороды: изомерия
Углеводороды: изомерия Амилаза. Строение амилазы
Амилаза. Строение амилазы Минеральные кислоты. Взаимодействие с простыми веществами
Минеральные кислоты. Взаимодействие с простыми веществами Энергетические уровни
Энергетические уровни Углеводороды (УВ)
Углеводороды (УВ) Олеиновая кислота
Олеиновая кислота Химия һәм сәламәт яшәү рәвеше
Химия һәм сәламәт яшәү рәвеше Презентация на тему Кальций
Презентация на тему Кальций  Арены. Бензол
Арены. Бензол Задания для подготовки к ЕГЭ по химии
Задания для подготовки к ЕГЭ по химии Окислительные свойства концентрированной серной кислоты
Окислительные свойства концентрированной серной кислоты Любовь и химия
Любовь и химия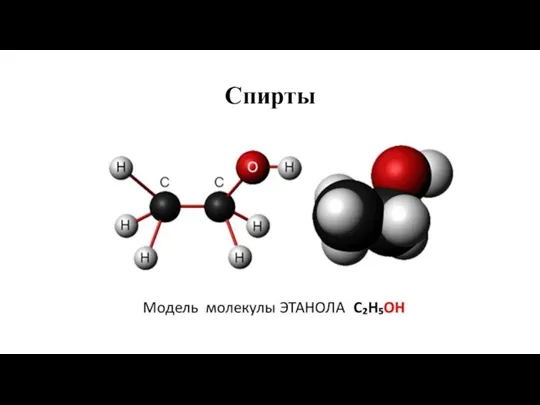 Спирты
Спирты Алкены. Этилен C2H4
Алкены. Этилен C2H4 Сравнительный анализ Фармакопейных статей для субстанций, представленных в мировых Фармакопеях
Сравнительный анализ Фармакопейных статей для субстанций, представленных в мировых Фармакопеях Окисление этанола оксидом меди
Окисление этанола оксидом меди Смачивание и не смачивание жидкости. Капилляры
Смачивание и не смачивание жидкости. Капилляры Карбоновые кислоты
Карбоновые кислоты Предмет органической химии. Урок №1
Предмет органической химии. Урок №1 Характеристика кислорода и серы
Характеристика кислорода и серы Свойства ртути
Свойства ртути