Содержание
- 2. АТОМ (от греч. atomos - неделимый), наименьшая частица хим. элемента, носитель его св-в. Каждому хим. элементу
- 3. МОЛЕКУЛА (новолат. molecula, уменьшит. от лат. moles-масса), микрочастица, образованная из двух или большего числа атомов и
- 4. 6.2. Распространенность химических элементов в природе Все доступные для исследования вещества состоят из одних и тех
- 6. 6.3. Валентность, степень окисления и строение молекул ВАЛЕНТНОСТЬ (от лат. valentia - сила), способность атома присоединять
- 7. На международном съезде химиков в Карлсруэ в 1860 году были приняты определения понятий молекулы и атома.
- 8. Центральным положением классической теории является положение о химической связи, при этом допускается наличие не только двухцентровых
- 9. 6.4. Понятие изомерии ИЗОМЕРИЯ (от изо... и греч. meros - доля, часть), существование соединений (гл. обр.
- 10. Структурная изомерия — результат различий в химическом строении. Пространственная изомерия (стереоизомерия) возникает в результате различий в
- 11. 6.5. Концепции обратимости химических реакции ОБРАТИМЫЕ РЕАКЦИИ — химические превращения, в которых продукты взаимодействия исходных веществ
- 12. При химических реакциях атомы или молекулы веществ, вступающих в реакцию, должны войти в тесное соприкосновение —
- 13. Окисление-восстановление, окислительно-восстановительные реакции, химические реакции, сопровождающиеся изменением окислительных чисел атомов. Первоначально (со времени введения в химию
- 15. Скачать презентацию
Слайд 2АТОМ (от греч. atomos - неделимый), наименьшая частица хим. элемента, носитель его
АТОМ (от греч. atomos - неделимый), наименьшая частица хим. элемента, носитель его

Слайд 3МОЛЕКУЛА (новолат. molecula, уменьшит. от лат. moles-масса), микрочастица, образованная из двух или
МОЛЕКУЛА (новолат. molecula, уменьшит. от лат. moles-масса), микрочастица, образованная из двух или

Слайд 46.2. Распространенность химических элементов в природе
Все доступные для исследования вещества состоят из
6.2. Распространенность химических элементов в природе
Все доступные для исследования вещества состоят из

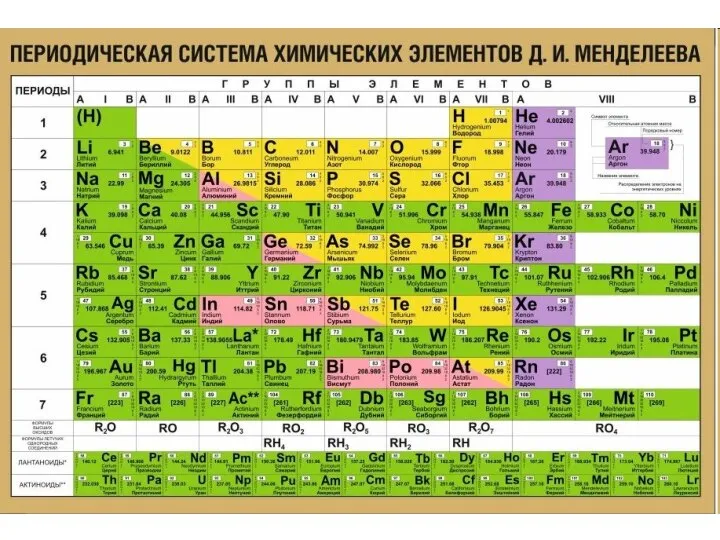
Распространенность химических элементов в природе подчиняется следующим основным эмпирическим правилам:
распространенность уменьшается с ростом заряда ядра;
зависимость распространенности элементов от заряда ядра имеет две ветви - крутую для легких элементов (до Cu, Zn) и значительно более пологую для более тяжелых;
четные химические элементы распространены больше, чем их нечетные соседи (<правило Оддо-Гаркинса>) (исключения - H, He, а также Li, Be, B);
наблюдаются отчетливые максимумы на кривой распространенности элементов группы Fe (Cr, Mn, Fe, Co, Ni), а также менее выраженные в области Xe-Ba, Pt и Pb;
наблюдается резко пониженная распространенность Li, Be, B.
Слайд 66.3. Валентность, степень окисления и строение молекул
ВАЛЕНТНОСТЬ (от лат. valentia - сила),
6.3. Валентность, степень окисления и строение молекул
ВАЛЕНТНОСТЬ (от лат. valentia - сила),

Слайд 7На международном съезде химиков в Карлсруэ в 1860 году были приняты определения
На международном съезде химиков в Карлсруэ в 1860 году были приняты определения

Классическая теория химического строения
В классической теории химического строения молекула рассматривается как наименьшая стабильная частица вещества, обладающая всеми его химическими свойствами.
Молекула данного вещества имеет постоянный состав, то есть одинаковое количество атомов, объединённых химическими связями, при этом химическая индивидуальность молекулы определяется именно совокупностью и конфигурацией химических связей, то есть валентными взаимодействиями между входящими в её состав атомами, обеспечивающими её стабильность и основные свойства в достаточно широком диапазоне внешних условий. Невалентные взаимодействия (например, водородные связи), которые зачастую могут существенно влиять на свойства молекул и вещества, образуемого ими, в качества критерия индивидуальности молекулы не учитываются.
Слайд 8 Центральным положением классической теории является положение о химической связи, при этом допускается
Центральным положением классической теории является положение о химической связи, при этом допускается

Таким образом, молекула в классической теории представляется динамической системой, в которой атомы рассматриваются как материальные точки и в которой атомы и связанные группы атомов могут совершать механические вращательные и колебательные движения относительно некоторой равновесной ядерной конфигурации, соответствующей минимуму энергии молекулы и рассматривается как система гармонических осцилляторов.
Слайд 96.4. Понятие изомерии
ИЗОМЕРИЯ (от изо... и греч. meros - доля, часть), существование
6.4. Понятие изомерии
ИЗОМЕРИЯ (от изо... и греч. meros - доля, часть), существование

Слайд 10Структурная изомерия — результат различий в химическом строении.
Пространственная изомерия (стереоизомерия) возникает в
Структурная изомерия — результат различий в химическом строении.
Пространственная изомерия (стереоизомерия) возникает в

Химические превращения, в результате которых структурные изомеры превращаются друг в друга, называется изомеризацией. Такие процессы имеют важное значение в промышленности. Так, например, проводят изомеризацию нормальных алканов в изоалканы для повышения октанового числа моторных топлив; изомеризуют пентан в изопентан для последующего дегидрирования в изопрен. Изомеризацией являются и внутримолекулярные перегруппировки, из которых большое значение имеет, например, перегруппировка Бекмана — превращение циклогексаноноксима в капролактам (сырьё для производства капрона).
Слайд 116.5. Концепции обратимости химических реакции
ОБРАТИМЫЕ РЕАКЦИИ — химические превращения, в которых продукты
6.5. Концепции обратимости химических реакции
ОБРАТИМЫЕ РЕАКЦИИ — химические превращения, в которых продукты

Слайд 12 При химических реакциях атомы или молекулы веществ, вступающих в реакцию, должны войти
При химических реакциях атомы или молекулы веществ, вступающих в реакцию, должны войти

Слайд 13Окисление-восстановление, окислительно-восстановительные реакции, химические реакции, сопровождающиеся изменением окислительных чисел атомов. Первоначально (со
Окисление-восстановление, окислительно-восстановительные реакции, химические реакции, сопровождающиеся изменением окислительных чисел атомов. Первоначально (со

Восстановлением называется присоединение электронов атомом, молекулой или ионом: Cl2 + 2e = 2Cl–
Окислителями называется нейтральный атом, молекула или ион, принимающие электроны (во втором примере молекула хлора Cl2), восстановителями — нейтральный атом, молекула или ион, отдающие электроны (в первом примере — атом Zn). Окисление и восстановление — взаимосвязанные процессы, которые всегда протекают одновременно. Когда одно вещество окисляется, то другое восстанавливается, и наоборот. Так, приведённые выше частные реакции окисления и восстановления составляют единый процесс окисления-восстановления: Zn + Cl2 = ZnCl2.
 Ситалл – искусственный поликристаллический материал
Ситалл – искусственный поликристаллический материал Использование катионных красителей в экстракционно-флуориметрическом анализе
Использование катионных красителей в экстракционно-флуориметрическом анализе Аналитическая химия. Гомогенные растворы
Аналитическая химия. Гомогенные растворы Галогены. Положение галогенов в ПСХЭ
Галогены. Положение галогенов в ПСХЭ Арены. Химические свойства
Арены. Химические свойства Индикаторная бумага
Индикаторная бумага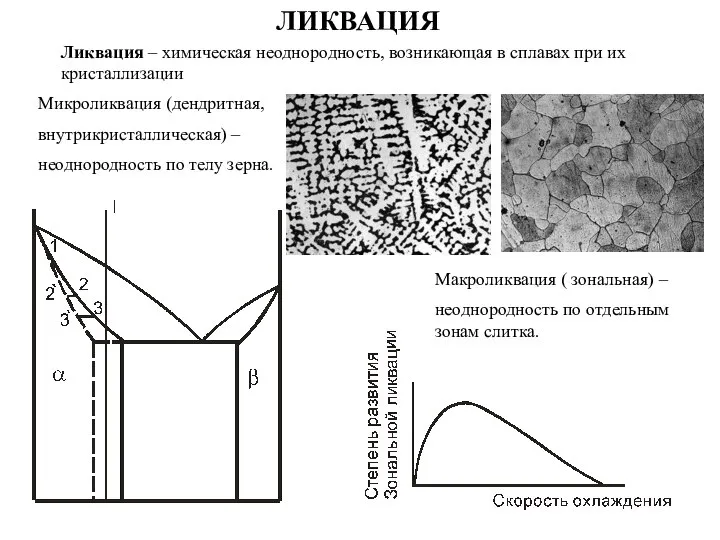 Ликвация. Микроликвация
Ликвация. Микроликвация Получение и примененипе радиоактивные изотопы
Получение и примененипе радиоактивные изотопы Химия и сельское хозяйство
Химия и сельское хозяйство Исследование влияния изменения технических параметров на производительность установки замедленного коксования
Исследование влияния изменения технических параметров на производительность установки замедленного коксования Непредельные углеводороды
Непредельные углеводороды Пластмассы
Пластмассы Тайна алмазов
Тайна алмазов Красители для волос. Первая группа
Красители для волос. Первая группа ОГЭ №1, вопрос 1-16
ОГЭ №1, вопрос 1-16 Интегративный подход к обучению на уроках химии
Интегративный подход к обучению на уроках химии Обобщение знаний об основных классах неорганических соединений
Обобщение знаний об основных классах неорганических соединений Презентация на тему Металлическая связь
Презентация на тему Металлическая связь  металлы
металлы Распределение электронов в атоме по энергетическим уровням
Распределение электронов в атоме по энергетическим уровням Строение атома. Распределение электронов
Строение атома. Распределение электронов Презентация на тему Алюминий(Al)
Презентация на тему Алюминий(Al)  Наркотики и прекурсоры
Наркотики и прекурсоры Получение галогеноалканов
Получение галогеноалканов Презентация на тему Гидролиз
Презентация на тему Гидролиз  Склероглюкан
Склероглюкан Курсовая работа: синтез 3,5-диметилпиразола
Курсовая работа: синтез 3,5-диметилпиразола Кремнийорганические каучуки
Кремнийорганические каучуки