Блокаторы периферического анионного сайта ацетилхолинэстеразы на основе пиримидина в качестве средства симптоматической терапии
Содержание
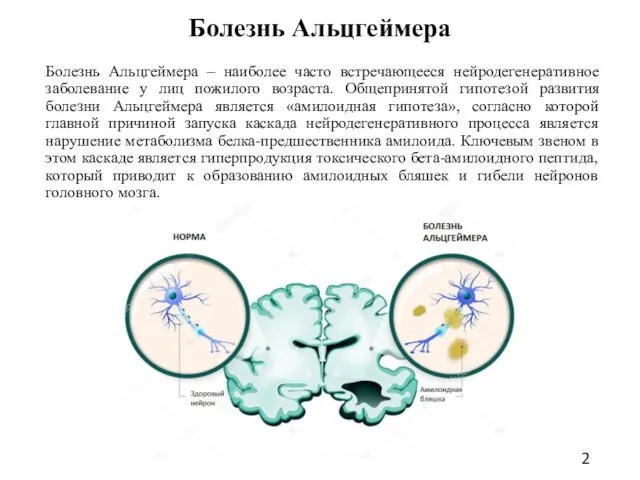
- 2. Болезнь Альцгеймера Болезнь Альцгеймера – наиболее часто встречающееся нейродегенеративное заболевание у лиц пожилого возраста. Общепринятой гипотезой
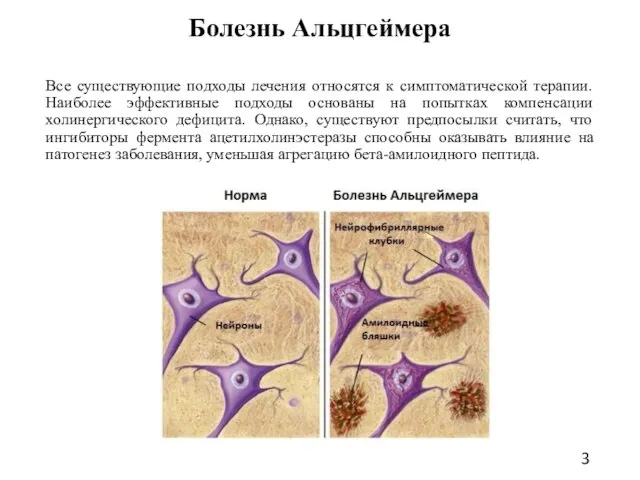
- 3. Болезнь Альцгеймера Все существующие подходы лечения относятся к симптоматической терапии. Наиболее эффективные подходы основаны на попытках
- 4. Цель работы: Исследовать эффективность соединений-лидеров, синтезированных в Институте органической и физической химии им. А.Е. Арбузова ФИЦ
- 5. Проверка острой токсичности Поведенческие тесты ( Т-тест, УРПИ ) Оценка острой токсичности соединений проводилась согласно «Методическим
- 6. Моделирование Болезни Альцгеймера Фармакологическая модель болезни Альцгеймера – основана на создании холинергического дефицита в результате инъекции
- 7. Приготовление срезов головного мозга и окрашивание амилоидных депозитов флуоресцентным красителем Криостат Microm HM 525 Конфокальный сканирующий
- 8. Результаты исследования Ингибиторная активность соединений
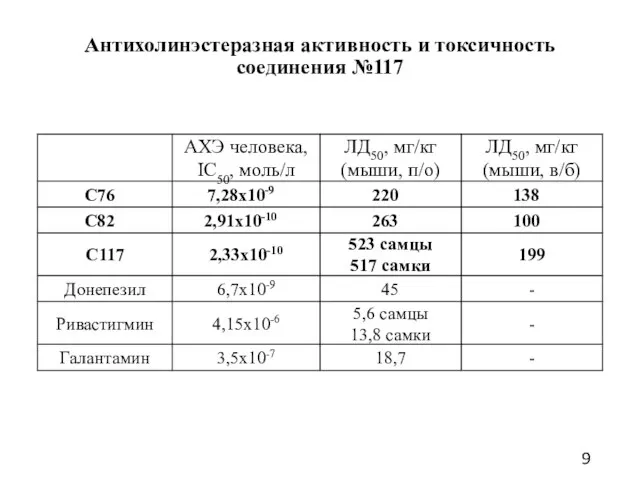
- 9. Антихолинэстеразная активность и токсичность соединения №117
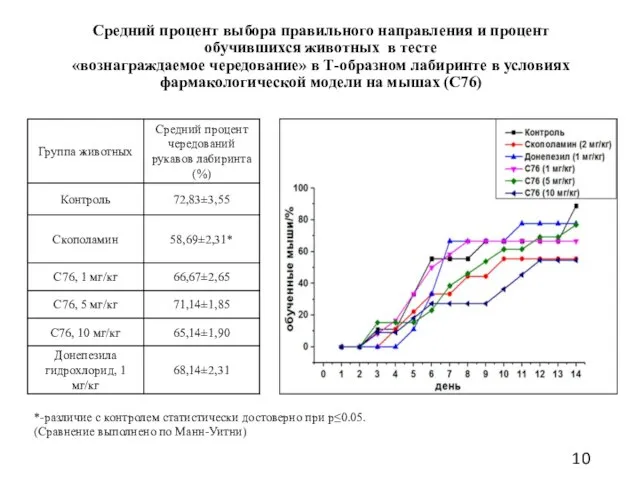
- 10. Средний процент выбора правильного направления и процент обучившихся животных в тесте «вознаграждаемое чередование» в Т-образном лабиринте
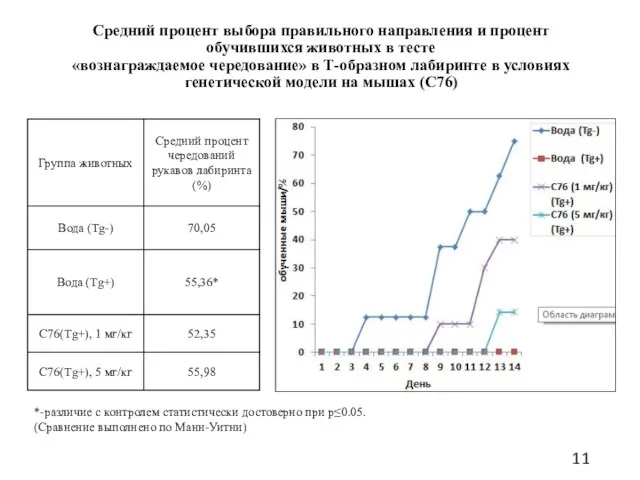
- 11. Средний процент выбора правильного направления и процент обучившихся животных в тесте «вознаграждаемое чередование» в Т-образном лабиринте
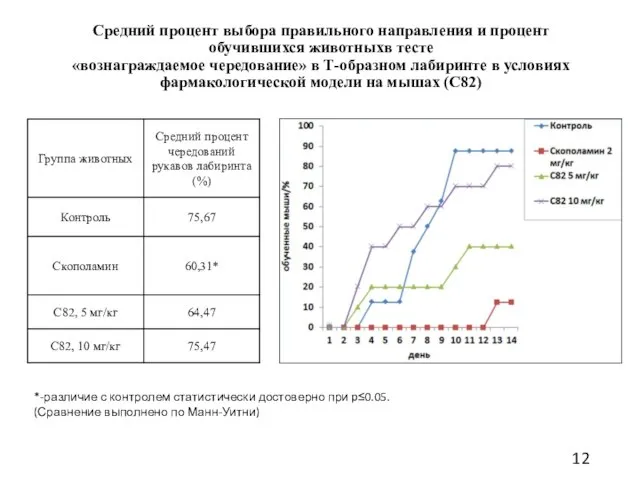
- 12. Средний процент выбора правильного направления и процент обучившихся животныхв тесте «вознаграждаемое чередование» в Т-образном лабиринте в
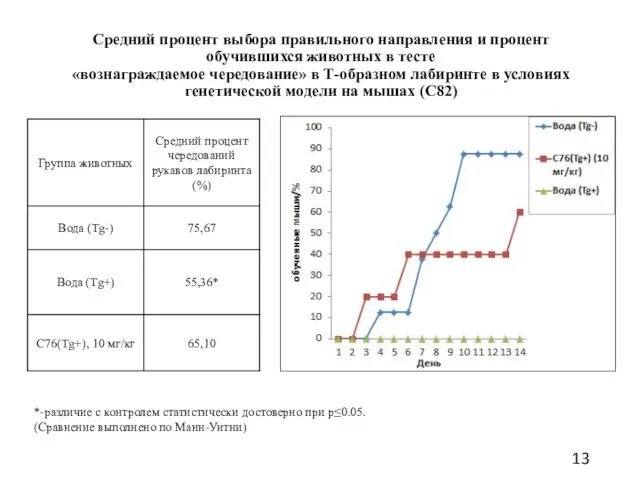
- 13. Средний процент выбора правильного направления и процент обучившихся животных в тесте «вознаграждаемое чередование» в Т-образном лабиринте
- 14. Средний процент выбора правильного направления в тесте «вознаграждаемое чередование» в Т-образном лабиринте в условиях фармакологической модели
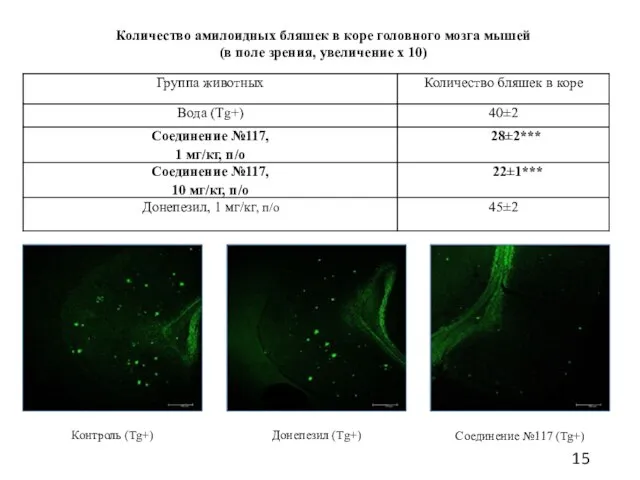
- 15. Количество амилоидных бляшек в коре головного мозга мышей (в поле зрения, увеличение х 10) Контроль (Tg+)
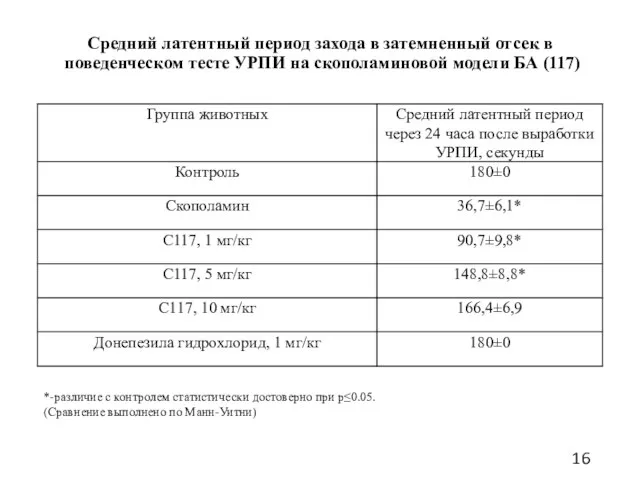
- 16. Средний латентный период захода в затемненный отсек в поведенческом тесте УРПИ на скополаминовой модели БА (117)
- 17. Выводы 1. Исследуемые соединения с лабораторными С76, С82 и С117 показали способность угнетать активность АХЭ в
- 18. Исследования были поддержаны грантами РНФ 14-50-00014 и РНФ 19-15-00344. Подана заявка на поддержку доклинических испытаний в
- 20. Скачать презентацию








 Задачи и основы организации единой государственной системы предупреждения и ликвидации чрезвычайных ситуаций (РСЧС)
Задачи и основы организации единой государственной системы предупреждения и ликвидации чрезвычайных ситуаций (РСЧС) Гипопитуитаризм
Гипопитуитаризм Рак шейки матки. Лекция 20
Рак шейки матки. Лекция 20 Отбор патологического материала для диагностики бешенства
Отбор патологического материала для диагностики бешенства Особенности диетотерапии после трансплантации почки Особенности диетотерапии после трансплантации почки
Особенности диетотерапии после трансплантации почки Особенности диетотерапии после трансплантации почки Медицинская помощь населению в чрезвычайных ситуациях
Медицинская помощь населению в чрезвычайных ситуациях Бронхиальная астма
Бронхиальная астма Макролиды и азалиды. Классификация, тип и механизм действия
Макролиды и азалиды. Классификация, тип и механизм действия Послеродовый период
Послеродовый период Гемостаз. Коагулограмма. Тэг. РоТЭМ
Гемостаз. Коагулограмма. Тэг. РоТЭМ Қызылша
Қызылша Астенічний синдром
Астенічний синдром Профессия – операционная медицинская сестра
Профессия – операционная медицинская сестра Отравление угарным газом
Отравление угарным газом Онтофилогенетические пороки развития скелета
Онтофилогенетические пороки развития скелета Мышечная дистрофия Дюшенна
Мышечная дистрофия Дюшенна Ситуация в области остеопороза в республике Молдова
Ситуация в области остеопороза в республике Молдова Вариации п-образных швов для сшивания кожи и сосудов
Вариации п-образных швов для сшивания кожи и сосудов Психопатология памяти (2 часа) (Лекция 4)
Психопатология памяти (2 часа) (Лекция 4) Женская консультация в г. Санкт-Петербург. Итоги финансово-экономической и хозяйственной деятельности
Женская консультация в г. Санкт-Петербург. Итоги финансово-экономической и хозяйственной деятельности Лихорадочные реакции
Лихорадочные реакции ЧУДО-Доктор, ковид и вакцинация 2023
ЧУДО-Доктор, ковид и вакцинация 2023 Основы косметических средств фармокологии
Основы косметических средств фармокологии Международная классификация функционирования, ограничений жизнедеятельности и здоровья. Версия для детей и подростков (МКФ-ДП)
Международная классификация функционирования, ограничений жизнедеятельности и здоровья. Версия для детей и подростков (МКФ-ДП) 111111111АНАТОМИЯ_Осанка,_её_значение_и_формирование_в_онтогенезе
111111111АНАТОМИЯ_Осанка,_её_значение_и_формирование_в_онтогенезе Синдром Брилла-Симмерса
Синдром Брилла-Симмерса Неотложные состояния в хирургии Острый живот
Неотложные состояния в хирургии Острый живот Аллергические реакции у детей
Аллергические реакции у детей