Содержание
- 2. Паркинсони́зм — неврологический синдром, который характеризуется рядом симптомов: тремором, мышечной ригидностью, постуральной неустойчивостью, брадикинезией и др.
- 3. ФИЗИОЛОГИЯ ДВИЖЕНИЯ ПИРАМИДНАЯ СИСТЕМА обеспечивает произвольное сокращение той или иной мышцы, приводя к тому или иному
- 4. ФИЗИОЛОГИЯ ДВИЖЕНИЯ Стриатум (стриарная система: хвостатое ядро, скорпула) более «молодая», созревает с возрастом и доминирует во
- 5. ЭТИОЛОГИЧЕСКАЯ СТРУКТУРА ПАРКИНСОНИЗМА 1. Первичный паркинсонизм Болезнь Паркинсона Ювенильный паркинсонизм 2. Вторичный (симптоматический) паркинсонизм Сосудистый паркинсонизм
- 6. 3. Паркинсонизм при мультисистемных нейродегенеративных заболеваниях ЦНС (паркинсонизм "плюс") 3.1. Преимущественно спорадические формы мультисистемная атрофия прогрессирующий
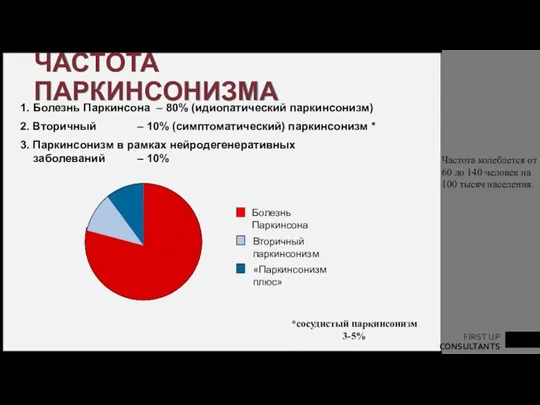
- 7. ЧАСТОТА ПАРКИНСОНИЗМА 1. Болезнь Паркинсона – 80% (идиопатический паркинсонизм) 2. Вторичный – 10% (симптоматический) паркинсонизм *
- 8. 11 Боле́знь Паркинсо́на (синонимы: идиопатический синдром паркинсонизма, дрожательный паралич) — медленно прогрессирующее хроническое нейродегенеративное заболевание центральной
- 9. ДЖЕЙМС ПАРКИНСОН ВПЕРВЫЕ ОПИСАЛ КЛИНИЧЕСКУЮ КАРТИНУ В 1817 ГОДУ 12
- 10. 13
- 11. ПРИЧИНЫ Истинная этиология остается неизвестной В качестве причин рассматривается несколько факторов: генетические причины (наследственная предрасположенность,мутации) неблагоприятные
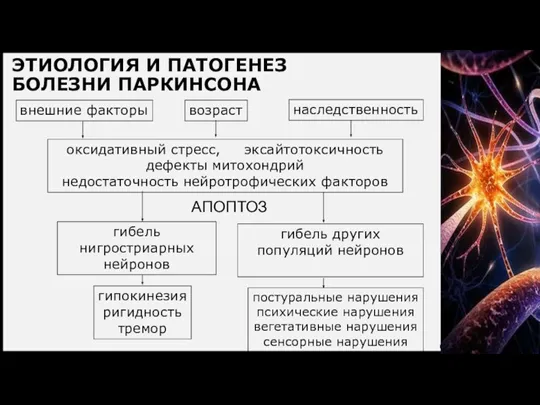
- 12. ЭТИОЛОГИЯ И ПАТОГЕНЕЗ БОЛЕЗНИ ПАРКИНСОНА внешние факторы возраст наследственность оксидативный стресс, эксайтотоксичность дефекты митохондрий недостаточность нейротрофических
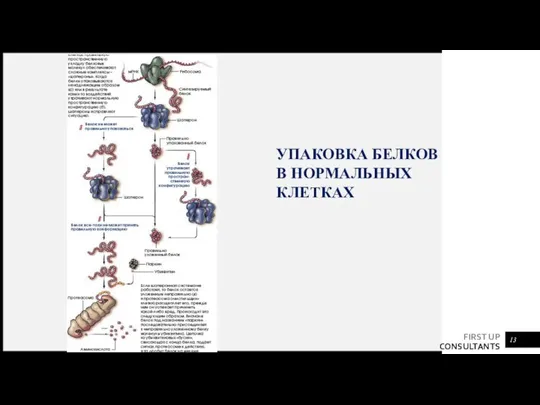
- 13. УПАКОВКА БЕЛКОВ В НОРМАЛЬНЫХ КЛЕТКАХ
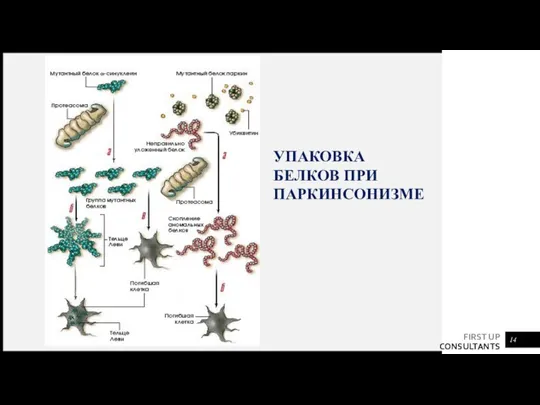
- 14. УПАКОВКА БЕЛКОВ ПРИ ПАРКИНСОНИЗМЕ
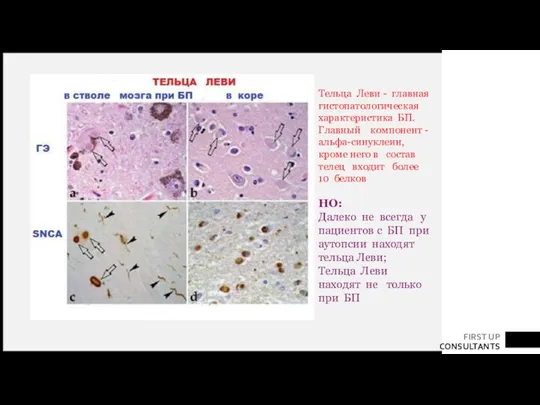
- 15. Тельца Леви - главная гистопатологическая характеристика БП. Главный компонент - альфа-синуклеин, кроме него в состав телец
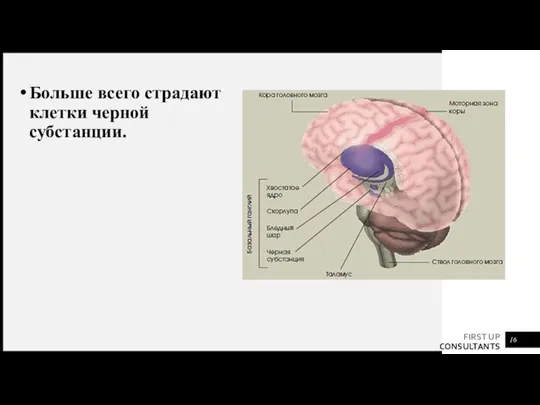
- 16. Больше всего страдают клетки черной субстанции.
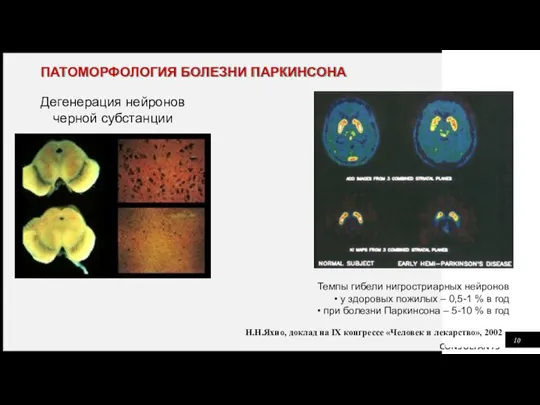
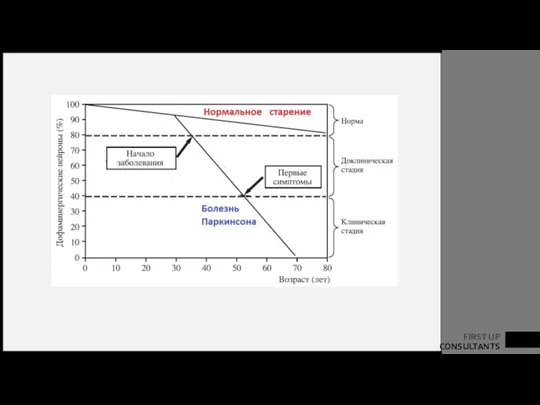
- 17. ПАТОМОРФОЛОГИЯ БОЛЕЗНИ ПАРКИНСОНА Темпы гибели нигростриарных нейронов у здоровых пожилых – 0,5-1 % в год при
- 18. Дофамин - играет роль стимулирующего нейромедиатора, способствующего повышению двигательной активности, уменьшению двигательной заторможенности и скованности, снижению
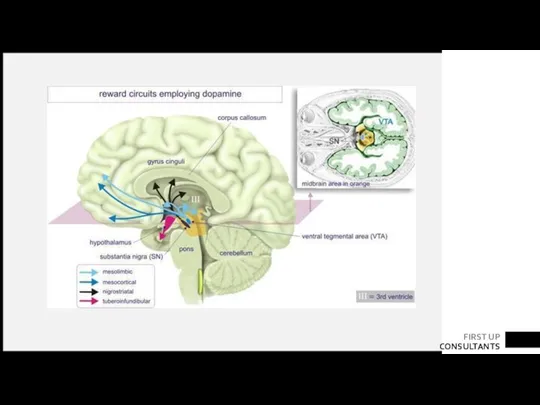
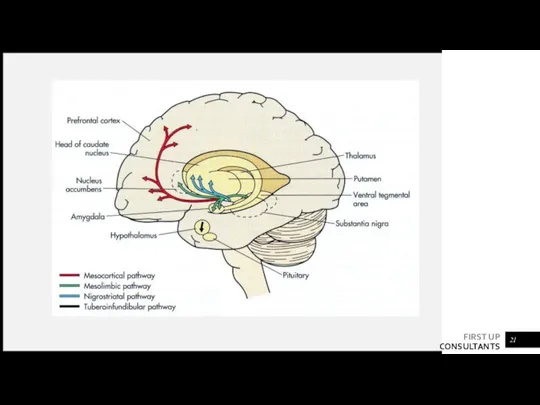
- 19. ПУТИ ПЕРЕДАЧИ ИМПУЛЬСОВ Восходящие дофаминергические пути: 1. нигростриарный путь - играет важную роль в координации; 2.
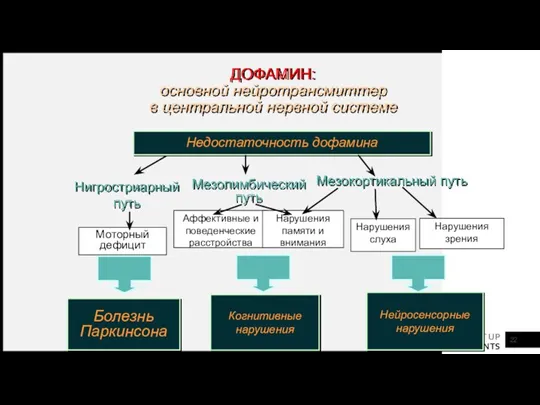
- 22. Нигростриарный путь Мезолимбический путь Мезокортикальный путь Моторный дефицит Аффективные и поведенческие расстройства Нарушения памяти и внимания
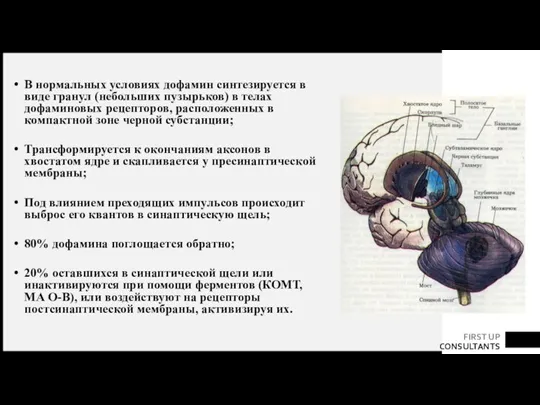
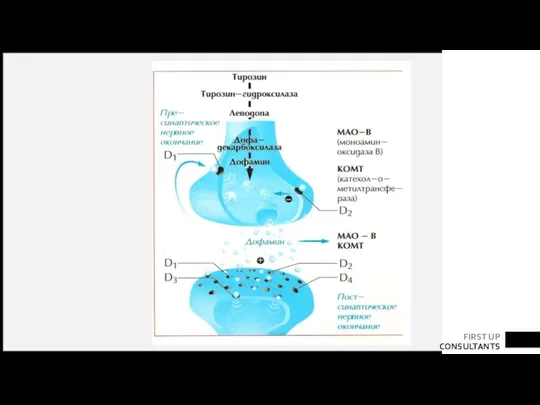
- 23. В нормальных условиях дофамин синтезируется в виде гранул (небольших пузырьков) в телах дофаминовых рецепторов, расположенных в
- 25. Так как базальные ганглии соединены между собой и с корой головного мозга, то дофамин, уменьшая активность
- 26. Соединение базальных ганглиев между собой представляет сложную систему. В ней принято выделять два основных круга: прямой
- 27. При Б.Паркинсона могут возникать дефекты в любом звене описанных взаимоотношений - снижение активности дофамин-продуцирующих нейронов черной
- 28. . Вначале последствия гибели нейронов в черной субстанции компенсируют другие нейроны, но когда доля утраченных клеток
- 30. Средний возраст начала болезни Паркинсона - 55 лет. В то же время у 10% больных заболевание
- 31. ДИАГНОСТИКА ПАРКИНСОНИЗМА состоит из 2-х этапов: 1. Синдромальная диагностика паркинсонизма; 2. Установление нозологического д-за.
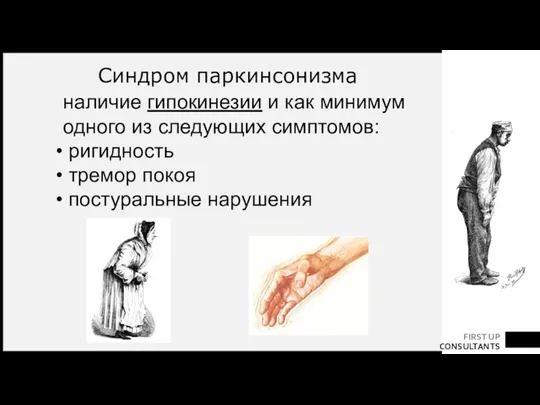
- 32. наличие гипокинезии и как минимум одного из следующих симптомов: ригидность тремор покоя постуральные нарушения Синдром паркинсонизма
- 33. КРИТЕРИИ ДИАГНОЗА БОЛЕЗНИ ПАРКИНСОНА (HUGES, 1992) 1) наличие гипокинезии и как минимум одного из следующих симптомов:
- 34. Клинико-диагностические критерии болезни Паркинсона Мозговой банк Общества болезни Паркинсона, Великобритания W.R.G. Gibbs, A.J. Lees, 1988 Критерии,
- 36. ВОЗРАСТНЫЕ ИЗМЕНЕНИЯ КОГНИТИВНЫХ ФУНКЦИЙ Уменьшается быстрота реакции ⇒ брадифрения Становится трудно длительно концентрировать внимание ⇒ быстрая
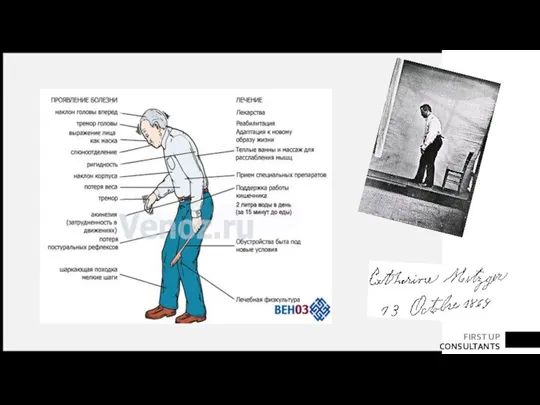
- 37. ГИПОКИНЕЗИЯ (акинезия) проявляется не только замедлением всех движений (брадикинезия), но и затруднением инициативы к действию, обеднением
- 38. РИГИДНОСТЬ – пластическое повышение мышечного тонуса – проявляется сопротивлением при пассивных движениях по типу «восковой куклы»
- 39. ДИФФЕРЕНЦИАЛЬНЫЙ ДИАГНОЗ ДРОЖАТЕЛЬНОЙ ФОРМЫ БП И ЭССЕНЦИАЛЬНОГО ТРЕМОРА
- 40. ПОСТУРАЛЬНАЯ НЕУСТОЙЧИВОСТЬ трудность поддержания центра тяжести и равновесия, т.е. нарушение позы. Самый устойчивый к лечению с-м.
- 41. СТАДИИ БОЛЕЗНИ ПАРКИНСОНА(ПО ХЕН И ЯРУ) I - односторонние нарушения, не ограничивающие обычную активность (гемипаркинсонизм); II
- 42. Классификация болезни Паркинсона (паркинсонизма) по клинической форме Дрожательная. Дрожательно - ригидная. Акинетико - ригидная форма. Акинетическая.
- 43. ТЕЧЕНИЕ БП Темпы прогрессирования: Быстрый темп прогрессирования - стадии заболевания меняются в течение 2-х лет. Умеренный
- 44. РАННИЕ НЕМОТОРНЫЕ НАРУШЕНИЯ: Эмоциональная угнетённость Повышенная раздражительность Быстрая утомляемость Ощущение постоянной усталости Расстройство потоотделения (например, профузное
- 45. ПОЗДНИЕ «немоторные» СИМТОМЫ БОЛЕЗНИ Нарушения сна (дневная сонливость, бессонница) Снижение мотивации, ангедония, хроническая депрессия (разрушение дофаминовых
- 46. ВТОРИЧНЫЙ ПАРКИНСОНИЗМ СИМПТОМАТИЧЕСКИЙ (10%) Лекарственный Токсический Сосудистый Постэнцефалитический Посттравматический При объемных процессах При гидроцефалии
- 47. ТОКСИЧЕСКИЙ ПАРКИНСОНИЗМ марганец окись углерода цианиды свинец метанол синтетический героин
- 48. ТОКСИЧЕСКИЙ ПАРКИНСОНИЗМ встречается менее чем в 1% П. Развивается постепенно, но достаточно быстро (1-3 года) и
- 49. НЕЙРОЛЕПТИЧЕСКИЙ (ЛЕКАРСТВЕННЫЙ) ПАРКИНСОНИЗМ Подострое развитие Симметричность симптомов Сочетание с лекарственными дискинезиями Сочетание с сердечно-сосудистыми и вегетативными
- 50. СОСУДИСТЫЙ ПАРКИНСОНИЗМ 1. Острое или подострое развитие после ОНМК 2. В неврологическом статусе имеются признаки поражения
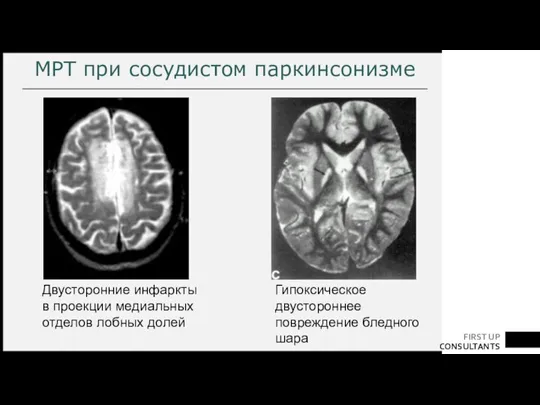
- 51. МРТ при сосудистом паркинсонизме Гипоксическое двустороннее повреждение бледного шара Двусторонние инфаркты в проекции медиальных отделов лобных
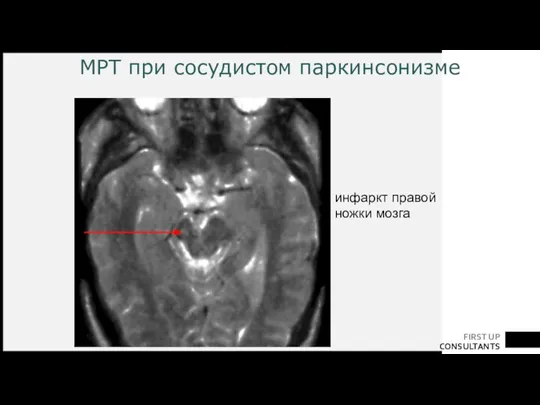
- 52. МРТ при сосудистом паркинсонизме инфаркт правой ножки мозга
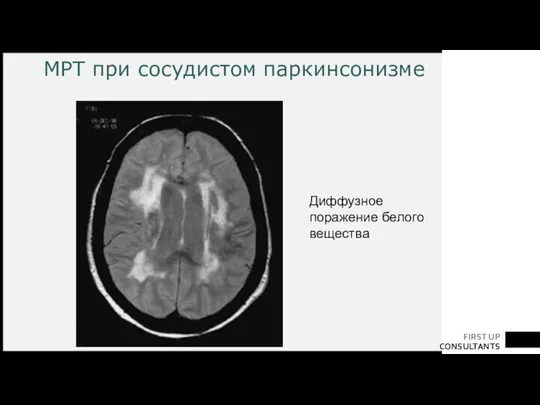
- 53. МРТ при сосудистом паркинсонизме Диффузное поражение белого вещества
- 54. ДРУГИЕ ВИДЫ ПАРКИНСОНИЗМА Постэнцефалитический П. ставится на основе анамнеза на перенесённое заболевание с выраженной сонливостью, двоением
- 55. ДРУГИЕ ВИДЫ ПАРКИНСОНИЗМА Посттравматический П. также встречается менее чем у 1% от числа б-х П. Имеется
- 56. СИНДРОМ «ПАРКИНСОНИЗМ ПЛЮС». ПРИЗНАКИ: Отсутствие ответа на леводопу/агонистов дофаминовых рецепторов на ранних стадиях заболевания раннее развитие
- 57. НЕЙРОДЕГЕНЕРАТИВНЫЕ ЗАБОЛЕВАНИЯ синуклеинопатии таупатии Альфа-синуклеин в норме присутствует в пресинаптических терминалях головного мозга. При НДЗ данный
- 58. ПРОГРЕССИРУЮЩИЙ НАДЪЯДЕРНЫЙ ПАРАЛИЧ БОЛЕЗНЬ СТИЛА-РИЧАРДСОНА-ОЛЬШЕВСКОГО: Дегенеративное заболевание головного мозга, нейропатологически характеризующееся скоплением тау-белка в астроцитах, нейрональных
- 59. Одним из самых важных диагностических признаков прогрессирующего надъядерного паралича является паралич взора по вертикали, который может
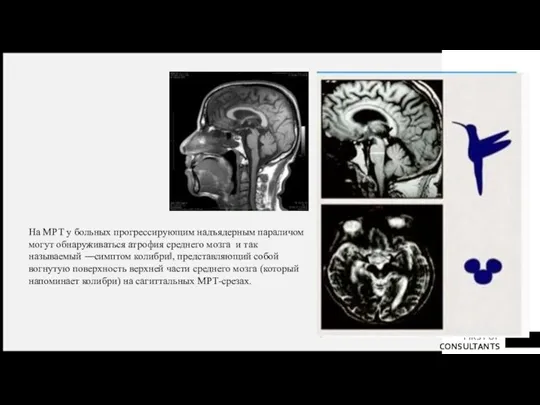
- 60. На МРТ у больных прогрессирующим надъядерным параличом могут обнаруживаться атрофия среднего мозга и так называемый ―симптом
- 61. ПОДТВЕРЖДАЮЩИЕ КРИТЕРИИ ДЛЯ ПРОГРЕССИРУЮЩЕГО НАДЪЯДЕРНОГО ПАРАЛИЧА: симметричная акинезия или ригидность, более выраженная в проксимальных отделах, чем
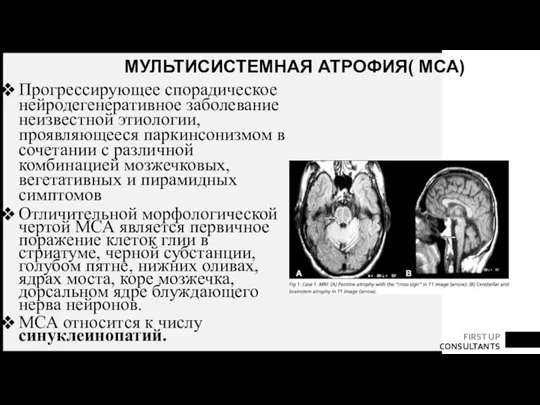
- 62. МУЛЬТИСИСТЕМНАЯ АТРОФИЯ( МСА) Прогрессирующее спорадическое нейродегенеративное заболевание неизвестной этиологии, проявляющееся паркинсонизмом в сочетании с различной комбинацией
- 63. КЛИНИЧЕСКИЕ ВАРИАНТЫ МСА Стриатонигральныя дегенерация (паркинсоническая форма) Оливопонтоцеребеллярная атрофия Синдром Шая-Дрейджера
- 64. Признаки не характерные для мультисистемной атрофии: классический тремор покоя по типу скатывания пилюль; клинически значимая нейропатия;
- 65. КОРТИКОБАЗАЛЬНАЯ ДЕГЕНЕРАЦИЯ (КБД) Нейродегенеративное заболевание, характеризующееся атрофией, глиозом и тау-иммунореактивными патологическими изменениями. Патоморфологически при КБД поражаются
- 66. Специфическим проявлением кортикобазальной дегенерации является синдром ―чужой руки‖ (alien hand phenomenon), который наблюдается в 60% случаев
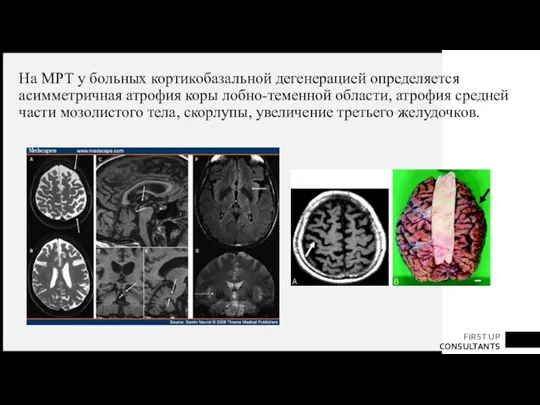
- 67. На МРТ у больных кортикобазальной дегенерацией определяется асимметричная атрофия коры лобно-теменной области, атрофия средней части мозолистого
- 68. ДЕМЕНЦИЯ С ТЕЛЬЦАМИ ЛЕВИ (ДТЛ) Морфологические признаки ДТЛ — преобладающие в коре лобной и височной долей
- 69. Экстрапирамидный синдром при ДТЛ не имеет асимметрии, в отличие от болезни Паркинсона, и проявляется изолированной акинезией,
- 70. Последовательность развития симптомов Диагноз деменции с тельцами Леви следует устанавливать, когда деменция развилась до паркинсонизма, одновременно
- 71. СИНДРОМ ПАРКИНСОНИЗМ-БАС-ДЕМЕНЦИЯ, БОЛЕЗНЬ ОСТРОВА ГУАМ Впервые описана у жителей острова Гуам в Тихоокеанском бассейне, относится к
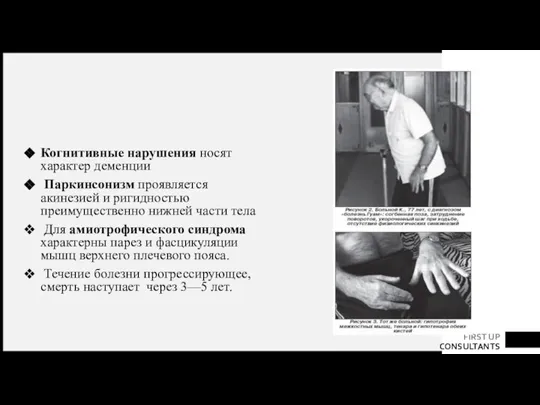
- 72. Когнитивные нарушения носят характер деменции Паркинсонизм проявляется акинезией и ригидностью преимущественно нижней части тела Для амиотрофического
- 73. 1. Центральные холинолитики 2. Препараты амантадина 3. ДОФА-содержащие средства (бенсеразид, карбидопа) 4. Агонисты дофаминовых рецепторов (бромокриптин,
- 74. ПРОТИВОПАРКИНСОНИЧЕСКИЕ ПРЕПАРАТЫ. ВЛИЯНИЕ НА КОГНИТИВНЫЕ ФУНКЦИИ. Холинолитики ускоряют деменцию Все остальные препараты снижают проявления деменции При
- 75. ПОДХОДЫ К ЛЕЧЕНИЮ БОЛЕЗНИ ПАРКИНСОНА: Начало лечения – монотерапия Подбор индивидуальной «субэффективной» дозы При прогрессировании заболевания
- 76. ЛЕВОДОПА – ЗОЛОТОЙ СТАНДАРТ ЛЕЧЕНИЯ. Благоприятный эффект на выживаемость проявляется лишь в первые 8-9 лет болезни
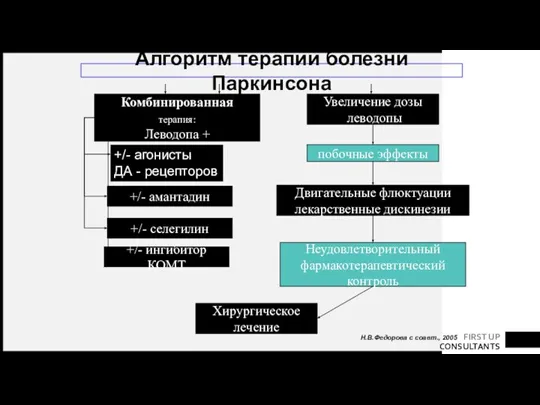
- 77. Комбинированная терапия: Леводопа + Увеличение дозы леводопы Двигательные флюктуации лекарственные дискинезии Неудовлетворительный фармакотерапевтический контроль побочные эффекты
- 78. АГОНИСТЫ ДОФАМИНЕРГИЧЕСКИХ РЕЦЕПТОРОВ АДР подразделяют на два класса – эрголиновые (бромокриптин, перголид, лизурид, каберголин) и неэрголиновые
- 79. АГОНИСТЫ ДОФАМИНЕРГИЧЕСКИХ РЕЦЕПТОРОВ Способны непосредственно стимулировать дофаминовые рецепторы на стриарных нейронах в обход дегенерирующих нигростриарных клеток,
- 80. ПРИЕМУЩЕСТВА АГОНИСТОВ ДОФАМИНЕРГИЧЕСКИХ РЕЦЕПТОРОВ Селективное воздействие на различные подгруппы дофаминовых рецепторов Прямая стимуляция постсинаптических рецепторов Не
- 81. ПРАМИПЕКСОЛ – СЕЛЕКТИВНЫЙ АГОНИСТ D2/D3 ДОФАМИНОВЫХ РЕЦЕПТОРОВ D3-рецепторы дофаминергической системы вовлечены в формирование настроения и поведения.
- 82. ПРАМИПЕКСОЛ Эффективен на всех стадиях заболевания Быстрое развитие клинического эффекта Позволяет отсрочить назначение леводопы, снизить дозу
- 83. МИРАПЕКС ПД Форма прамипексола, предполагающая однократный приём в течение дня, что может существенно повышать приверженность пациентов
- 84. ПРЕПАРАТЫ АМАНТАДИНА Оказывают умеренное положительное действие на все проявления болезни и относительно хорошо переносятся Механизм действия
- 85. Акатинол Мемантин- NMDA-антагонист специфическая нейропротекция и эффективная коррекция когнитивных расстройств различной этиологии нейродегенеративные заболевания (включая болезнь
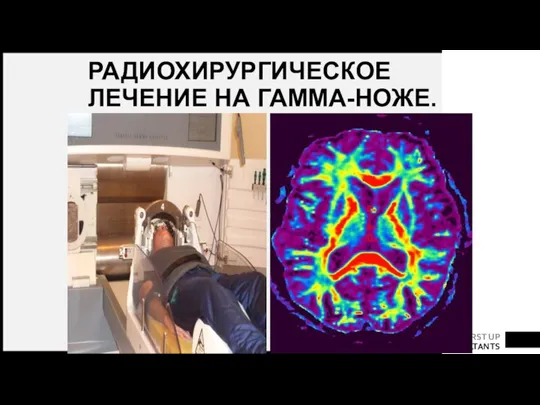
- 86. РАДИОХИРУРГИЧЕСКОЕ ЛЕЧЕНИЕ НА ГАММА-НОЖЕ. Принцип воздействия прежний - производится нацеливание на структуру-мишень с точностью до долей
- 87. РАДИОХИРУРГИЧЕСКОЕ ЛЕЧЕНИЕ НА ГАММА-НОЖЕ.
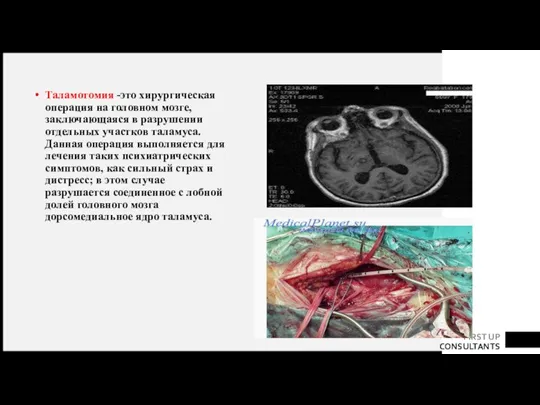
- 88. Таламотомия -это хирургическая операция на головном мозге, заключающаяся в разрушении отдельных участков таламуса. Данная операция выполняется
- 89. Таламотомия показана лишь в тех случаях, когда основным симптомом заболевания является тремор. Для получения положительного результата
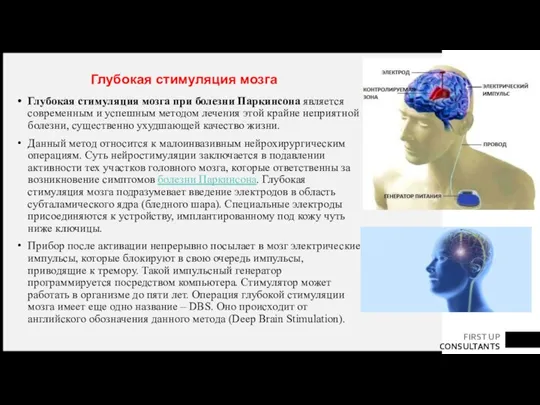
- 90. Глубокая стимуляция мозга при болезни Паркинсона является современным и успешным методом лечения этой крайне неприятной болезни,
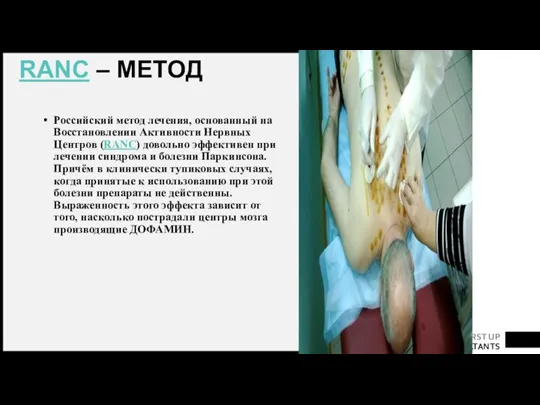
- 91. RANC – МЕТОД Российский метод лечения, основанный на Восстановлении Активности Нервных Центров (RANC) довольно эффективен при
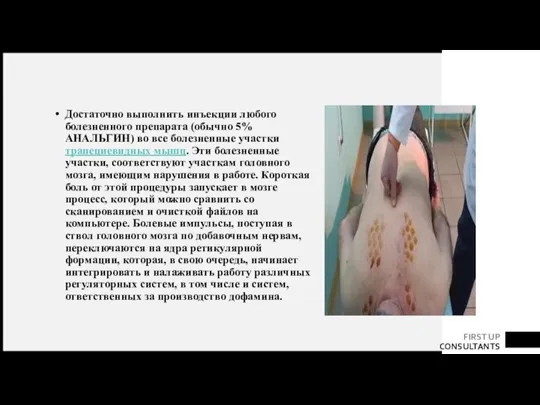
- 92. Достаточно выполнить инъекции любого болезненного препарата (обычно 5% АНАЛЬГИН) во все болезненные участки трапециевидных мышц. Эти
- 94. Скачать презентацию





























































 Связь заболеваний пародонта и риска преждевременных родов и низкого веса новорожденного
Связь заболеваний пародонта и риска преждевременных родов и низкого веса новорожденного Внематочная беременность
Внематочная беременность Скрининговая тепловизорная диагностика параназальных синуситов
Скрининговая тепловизорная диагностика параназальных синуситов Полезные продукты
Полезные продукты Правила личной гигиены
Правила личной гигиены Моё призвание - медицина
Моё призвание - медицина Лекарственные растения презентация. Чабрец
Лекарственные растения презентация. Чабрец Общая этиология
Общая этиология Виды ран и общие правила оказания первой медицинской помощи
Виды ран и общие правила оказания первой медицинской помощи Нарушение проводимости из предсердий
Нарушение проводимости из предсердий Геномные мутации
Геномные мутации Внедрение метода мама-кенгуру в практику интенсивного выхаживания недоношенных детей НДСБ ОХМАТДЕТ
Внедрение метода мама-кенгуру в практику интенсивного выхаживания недоношенных детей НДСБ ОХМАТДЕТ Заболевания почек
Заболевания почек Нейссерии. Род Neisseria
Нейссерии. Род Neisseria ДВС-синдром
ДВС-синдром Санация ротовой полости
Санация ротовой полости Autonomic nervous system
Autonomic nervous system Шов кожи
Шов кожи Маниакально-депрессивный психоз (биполярное аффективное расстройство)
Маниакально-депрессивный психоз (биполярное аффективное расстройство) Регуляция кровообращения
Регуляция кровообращения Проведение СЛР одним спасателем
Проведение СЛР одним спасателем Симптомы при заболеваниях желудочно-кишечного тракта
Симптомы при заболеваниях желудочно-кишечного тракта Phylogenetic disorder of circulatory system
Phylogenetic disorder of circulatory system Монастырское направление в медицине
Монастырское направление в медицине Синдром Брилла-Симмерса
Синдром Брилла-Симмерса The first woman doctor in Russia
The first woman doctor in Russia Ранения. Виды ран
Ранения. Виды ран Хроническая недостаточность надпочечников (болезнь Аддисона)
Хроническая недостаточность надпочечников (болезнь Аддисона)