Содержание
- 2. Положительные и отрицательные списки Все медицинские препараты получают разрешение на реализацию в регулирующих органах Системы возмещения
- 3. Основные вопросы лекарственного обеспечения Ограничительные списки - формуляры, отрицательные и положительные cписки – определяют перечень препаратов
- 4. Перечень жизненно-необходимых и важнейших лекарственных средств (ЖНВЛС) Перечень лекарственных средств, отпускаемых по рецепту врача (фельдшера) при
- 5. Перечень ЖНВЛС: критерии включения научно обоснованные данные об эффективности и безопасности препарата (уровень доказательности А и
- 6. Перечень ДЛО: критерии включения оформленные надлежащим образом данные об эффективности и безопасности препарата при определенном заболевании,
- 7. Льготные перечни ЛС, для которых законодательного регулирования принципов и процедуры включения не существует Перечень централизованно закупаемых
- 8. Критерии включения препаратов в списки возмещения (положительные списки)
- 9. Критерии включения препаратов в списки возмещения
- 10. Дополнительные факторы возмещения стоимости препаратов Льготы в установленных системах оплаты Больные с серьезными и хроническими заболеваниями
- 11. Ограничения по использованию ЛС Медицинские Ограничения по диагнозу, по форме, степени тяжести Ограничения по специализации и
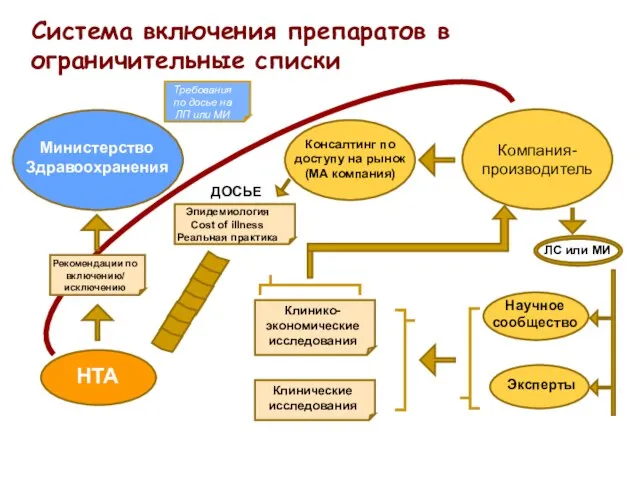
- 12. Система включения препаратов в ограничительные списки
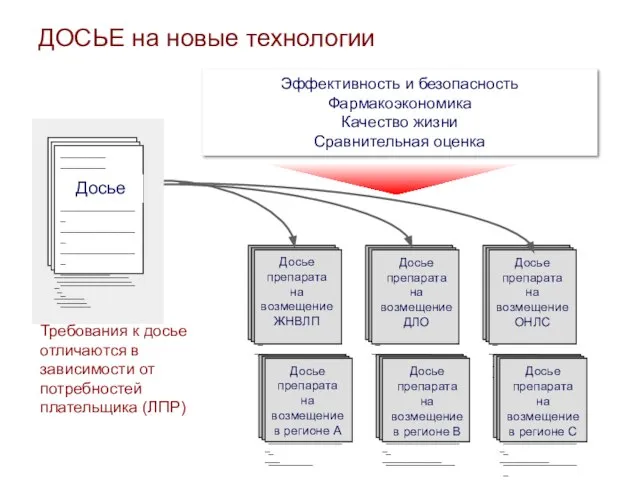
- 13. Досье препарата на возмещение ЖНВЛП Досье препарата на возмещение ДЛО Досье препарата на возмещение ОНЛС Эффективность
- 14. Основные параметры досье на включения ЛП в ограничительные(льготные) перечни Актуальность заболевания Эпидемиология заболевания Реальная практика ведения
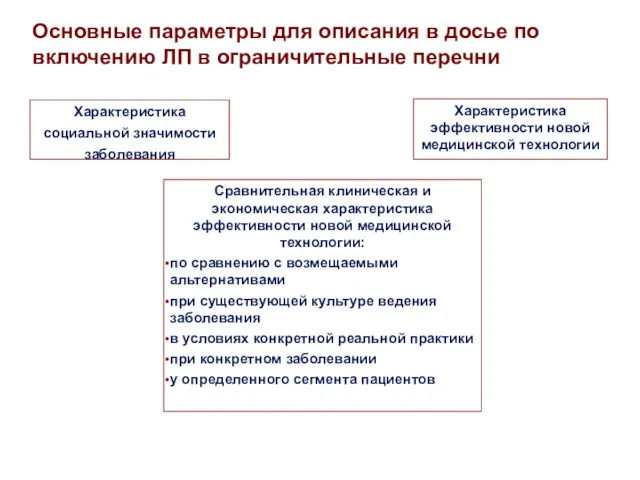
- 15. Основные параметры для описания в досье по включению ЛП в ограничительные перечни Характеристика социальной значимости заболевания
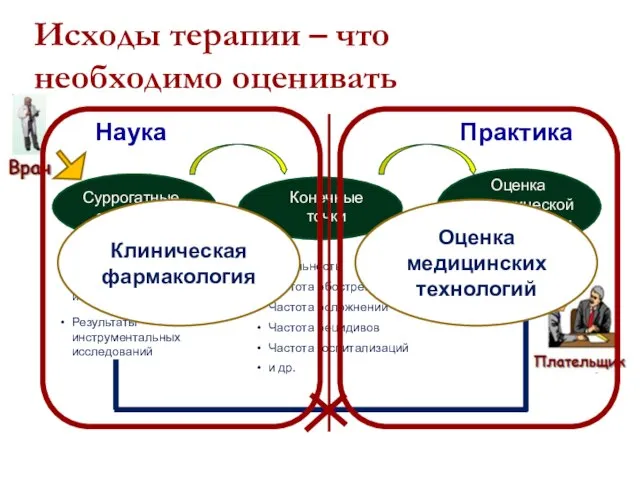
- 16. Исходы терапии – что необходимо оценивать Результаты лабораторных исследований Результаты инструментальных исследований Летальность Частота обострений Частота
- 17. ИННОВАЦИИ Инновация может быть определена как технологический прогресс, приводящий к созданию нового продукта или снижению затрат
- 18. Инновация может быть направлена На терапевтический прогресс ? На процесс разработки и биотехнологии ? На коммерческую
- 19. Вопросы к инновациям Повышает ли технология выживаемость и сокращает ли затраты на ведение заболевания? Как влияет
- 20. Критерии оценки продукта для определения его терапевтической ценности и инновационности Степень новизны препарата - наличие возможностей
- 21. Комплексный подход по оценке ценности технологий Франция
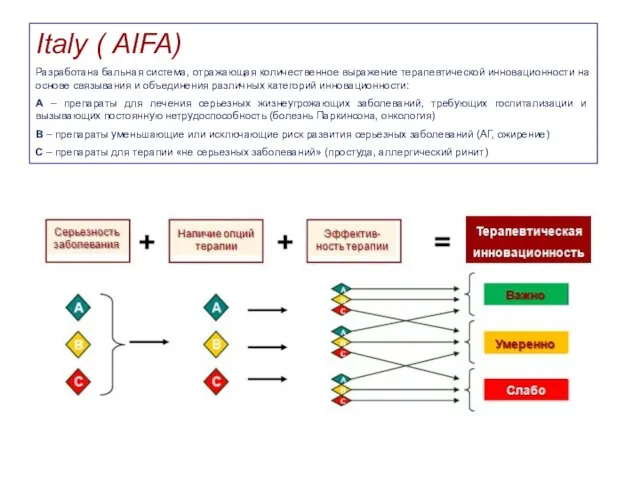
- 22. Italy ( AIFA) Разработана бальная система, отражающая количественное выражение терапевтической инновационности на основе связывания и объединения
- 23. Как надо «посчитать» инновационность Сегодня необходимо разработать «шкалу» суммарной инновационности препаратов, инкорпорированную в прозрачную систему оценки
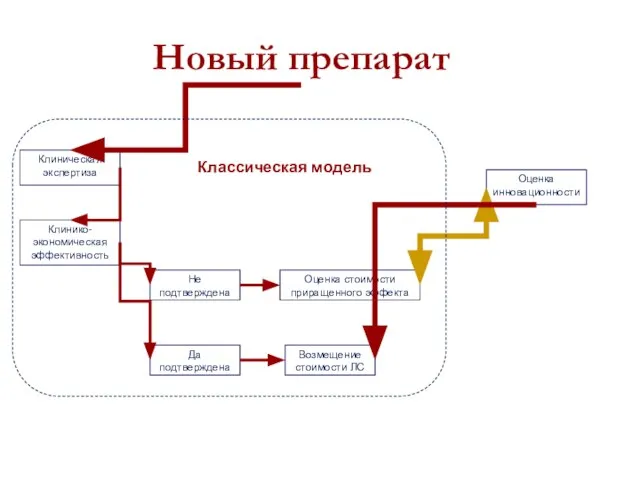
- 24. Новый препарат Клиническая экспертиза Оценка стоимости приращенного эффекта Клинико-экономическая эффективность Оценка инновационности Не подтверждена Да подтверждена
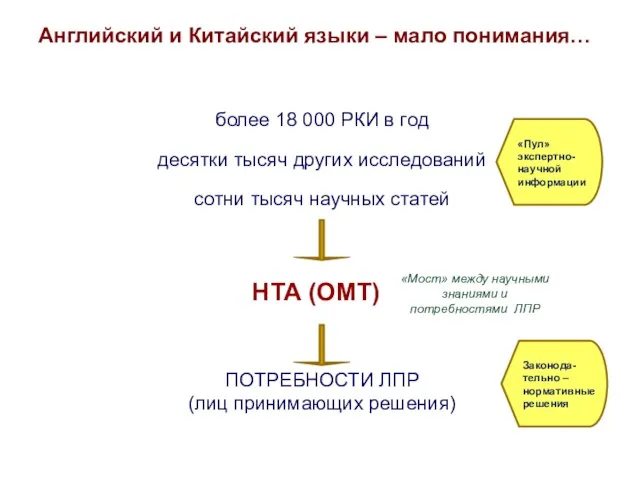
- 25. Английский и Китайский языки – мало понимания… более 18 000 РКИ в год десятки тысяч других
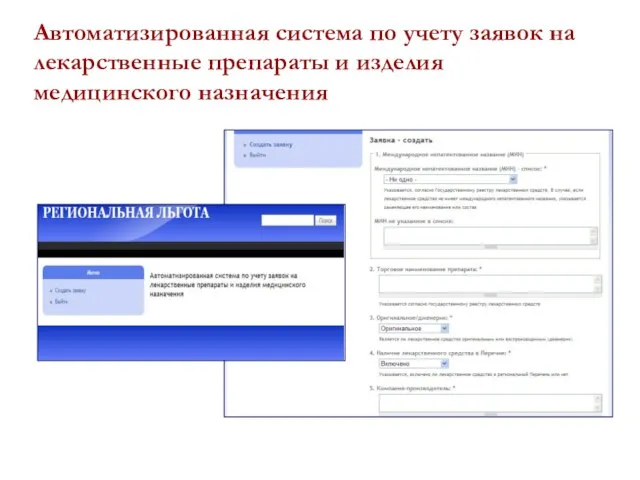
- 26. Автоматизированная система по учету заявок на лекарственные препараты и изделия медицинского назначения
- 27. Что включает в себя автоматизированная система? Сайт в интернете (www.docie.ru) с паролями доступа Возможность заполнения заявок
- 28. Программа ABC/VEN/DDD «Фармкомпайл» Более 280 врачей – провизоров, клинических фармакологов и организаторов здравоохранения применяют данную программу
- 29. Журнал «Медицинские технологии. Оценка и выбор» Концепция: создать эффективный профессионально-ориентированный информационный ресурс – площадку для интеграции
- 31. Скачать презентацию




















 Бронхоэктатическая болезнь у детей
Бронхоэктатическая болезнь у детей Балалардағы артериальды гипертензияның клиникалық белгілері
Балалардағы артериальды гипертензияның клиникалық белгілері Аноректальные пороки
Аноректальные пороки Массаж при сколиозе. Выбор приёмов в зависимости от тонуса мышц пациента
Массаж при сколиозе. Выбор приёмов в зависимости от тонуса мышц пациента Аюрведа: 5 шагов к здоровью. 1 день
Аюрведа: 5 шагов к здоровью. 1 день Маниакально-депрессивный психоз (биполярное аффективное расстройство)
Маниакально-депрессивный психоз (биполярное аффективное расстройство) Денсаулықпен байланысты өмір сапасы
Денсаулықпен байланысты өмір сапасы Гестозы. Классификация
Гестозы. Классификация Нормирование труда в здравоохранении
Нормирование труда в здравоохранении Le bloc opératoire
Le bloc opératoire Острый лейкоз
Острый лейкоз Частная психология
Частная психология Лечение экзо- и эндоцервицитов, ассоциированных с неспецифической микстинфекцией нижнего отдела гениталий у женщин
Лечение экзо- и эндоцервицитов, ассоциированных с неспецифической микстинфекцией нижнего отдела гениталий у женщин Эмбриологические аспекты программы ЭКО
Эмбриологические аспекты программы ЭКО Аптечка доврачебной помощи
Аптечка доврачебной помощи Алкоголизм и его влияние на развитие здоровой личности
Алкоголизм и его влияние на развитие здоровой личности Выявление факторов, влияющих на ожирение
Выявление факторов, влияющих на ожирение Медики в годы Великой Отечественной войны
Медики в годы Великой Отечественной войны Неотложные состояния в педиатрии
Неотложные состояния в педиатрии Защитно-приспособительные реакции при гипоксии
Защитно-приспособительные реакции при гипоксии Врачебная тактика при острой лихорадке неясного происхождения
Врачебная тактика при острой лихорадке неясного происхождения Этиопатогенез зубочелюстных аномалий
Этиопатогенез зубочелюстных аномалий Алыптасу кезеңіндегі (бозбалалық, бойжеткендік) негізгі проблемалар және оның шешу жолдары
Алыптасу кезеңіндегі (бозбалалық, бойжеткендік) негізгі проблемалар және оның шешу жолдары Кровотечения на фоне менопаузальной гормональной терапии (МГТ)
Кровотечения на фоне менопаузальной гормональной терапии (МГТ) Предмет, задачи и методы патологии. Понятие о болезни
Предмет, задачи и методы патологии. Понятие о болезни Безопасная беременность
Безопасная беременность Гипертоническая болезнь
Гипертоническая болезнь Сестринский уход при физиологической беременности
Сестринский уход при физиологической беременности