Ведение первичной медицинской документации в ходе исследования. Информированное согласие пациента, протокол исследования
Содержание
- 2. Информация, полученная в исследовании
- 3. Записи и отчеты
- 4. Требования по проведению КИ
- 5. Протокол и поправки к нему Исследования с участием человека в качестве субъекта не могут проводиться без
- 6. Требования протокола Все вовлеченные стороны обязаны строго соблюдать протокол исследования Любые изменения или отклонения от протокола
- 7. Что такое информированное согласие? “Процедура добровольного подтверждения субъектом своего согласия на участие в конкретном исследовании после
- 8. Информированное согласие Согласие принимается добровольно после предоставления письменной и устной информации о ходе исследования, его целях
- 9. Информированное согласие (2) Разделы 4.8.1 – 4.8.15 Чрезвычайно важная часть исследования Что это? Письменный документ, который
- 10. Информированное согласие (3) 4.8.1 Одобряется комитетом по этике. 4.8.2 По мере появления новой важной информации информированное
- 11. Частые нарушения при документировании ИС Отсутствует дата или подпись в форме ИС Дата получения информированного согласия
- 12. Основные нарушения, выявленные во время инспекций 1. Первичные данные отсутствуют или не совпадают с данными в
- 13. "The consent form is not meant to reassure the subject, quite the contrary, it is meant
- 14. Уязвимые группы Лица без определенного места жительства Неизлечимые больные Сотрудники медицинских учреждений Студенты медицинских университетов Сотрудники
- 15. Брошюра исследователя (БИ) Сводное изложение результатов клинического и доклинического изучения исследуемого продукта, значимых для его исследования
- 16. Брошюра исследователя (2) Для кого предназначена: Компетентные органы Комитеты по этике Исследователь “Живой” постоянно обновляемый документ
- 17. 1. Оглавление 2. Аннотация 3. Введение 4. Физико-химические свойства продукта 5. Доклинические исследования 5.1 Фармакология 5.2
- 18. Брошюра исследователя. Пример для дискуссии Вы монитор и проводите в центре визит инициации. Вы не можете
- 19. Первичные данные Любые оригинальные документы, данные, записи, таблицы, лабораторные распечатки, и др. Данные ЭКГ, рентгеновские пленки,
- 20. Первичные данные (2) Национальный стандарт Российской Федерации ГОСТ Р 52379-2005, раздел 1.42
- 21. Первичные данные (3) ICH Topic E6 Guideline for GCP, section 1.52
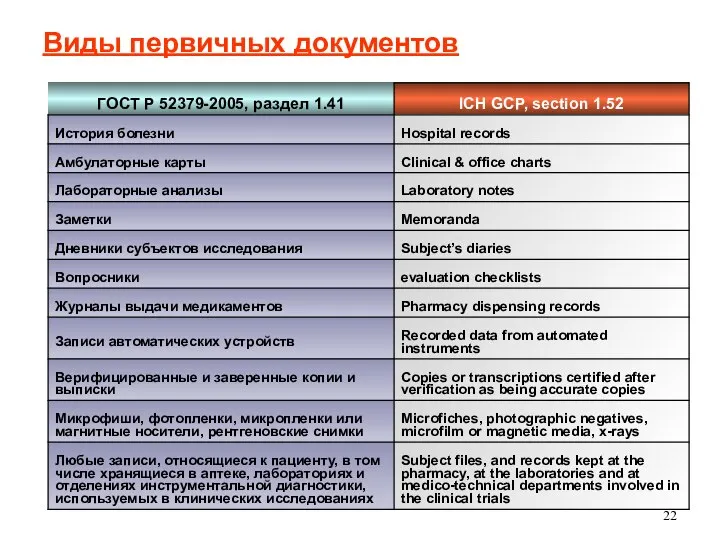
- 22. Виды первичных документов
- 23. Прямой доступ к первичным документам ICH Topic E6 Guideline for GCP, section 1.21, 4.9.7,5.15.1,
- 24. Прямой доступ к первичным документам (2) Разрешение на изучение, анализ, проверку и копирование любых записей и
- 25. Конфиденциальность персональных данных
- 26. Конфиденциальность персональных данных (2) Федеральный закон Российской Федерации от 27 июля 2006 г. N 152-ФЗ О
- 27. Верификация первичных данных (SDV)
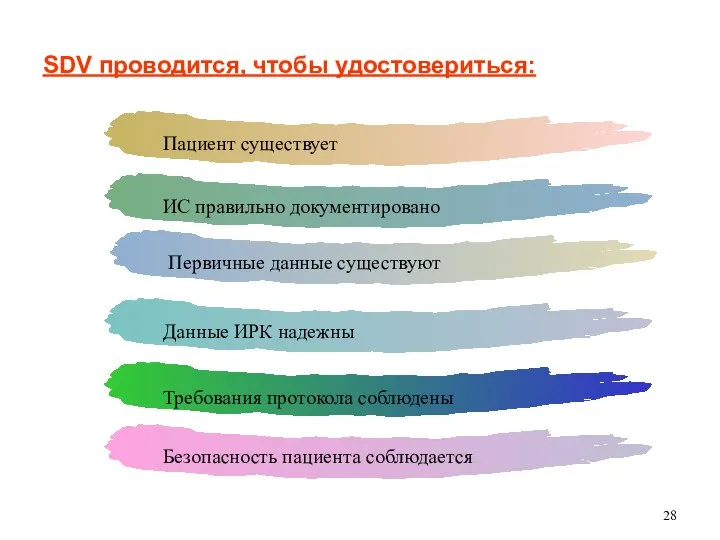
- 28. SDV проводится, чтобы удостовериться:
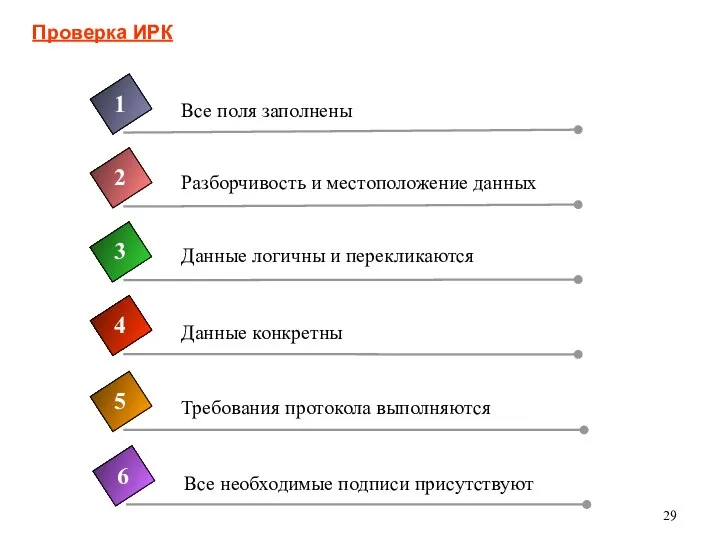
- 29. Проверка ИРК
- 30. ИРК – 3 «кита» ИРК - документ на бумажном, электронном или оптическом носителе, предназначенный для внесения
- 32. Скачать презентацию

























 Тема 3. Биологические опасности и защита от них (1)
Тема 3. Биологические опасности и защита от них (1) Жұқпалы аурулар
Жұқпалы аурулар Заболевания прямой кишки
Заболевания прямой кишки Аскаридоз. Аскарида людська
Аскаридоз. Аскарида людська джп
джп Сестринский процесс
Сестринский процесс Опікова токсемія
Опікова токсемія Механические повреждения тела
Механические повреждения тела Перелом бедра 60+
Перелом бедра 60+ Хроническое нарушение мозгового кровообращения
Хроническое нарушение мозгового кровообращения Инструментальные методы исследование органов дыхания у детей
Инструментальные методы исследование органов дыхания у детей Введение. История фармакологии. Общая фармакология
Введение. История фармакологии. Общая фармакология Надлежащая аптечная практика лекарственных средств для медицинского применения
Надлежащая аптечная практика лекарственных средств для медицинского применения Клиническая задача
Клиническая задача Бронхиальная астма
Бронхиальная астма Рак полости рта: вовремя распознать и вылечить!
Рак полости рта: вовремя распознать и вылечить! Язвезвенная болезнь двенадцатиперстной кишки у детей
Язвезвенная болезнь двенадцатиперстной кишки у детей Жировая эмболия
Жировая эмболия Фізіологія пологів. Знеболення пологів
Фізіологія пологів. Знеболення пологів Периоды новорожденности
Периоды новорожденности Правовой обзор в сфере ВИЧ-инфекции
Правовой обзор в сфере ВИЧ-инфекции Особенности диетотерапии после трансплантации почки Особенности диетотерапии после трансплантации почки
Особенности диетотерапии после трансплантации почки Особенности диетотерапии после трансплантации почки Инсульт. Факторы риска, диагностика и первая помощь
Инсульт. Факторы риска, диагностика и первая помощь Роль и функции акушерки при оказании первичной реанимационной помощи новорождённому в родильном зале
Роль и функции акушерки при оказании первичной реанимационной помощи новорождённому в родильном зале Искусственное очищение крови и других жидкостей человеческого тела. Принцип действия диализа. Методы диализа
Искусственное очищение крови и других жидкостей человеческого тела. Принцип действия диализа. Методы диализа Опухоли
Опухоли Тофацитиниб (Tofacitinibum)
Тофацитиниб (Tofacitinibum) Имплантация. История и определение, виды имплантатов в МД, их особенности, подготовка и процесс установки
Имплантация. История и определение, виды имплантатов в МД, их особенности, подготовка и процесс установки