Слайд 2Эквивалент
– это часть молекулы (атома) вещества, равноценная в химической реакции одному атому

или иону водорода или одному электрону.
Слайд 3или
Эквивалентом вещества называется такое его количество, которое соединяется с 1 молем атомов

водорода или замещает то же количество атомов водорода в химических реакциях.
Слайд 4молярная масса эквивалента вещества
– это масса одного моль эквивалентов вещества, равноценная в

химической реакции массе 1 моль атомов или ионов водорода или количеству электронов 1 моль.
Слайд 5или эквивалентной массой
называется масса 1 эквивалента вещества

Слайд 6Расчет молярной массы эквивалента вещества осуществляется по следующим правилам:
1.Химические элементы.
Мэ = М

/ n
Где Мэ – молярная масса эквивалента элемента,
М – молярная масса элемента,
n - валентность.
Слайд 7Расчет молярной массы эквивалента вещества осуществляется по следующим правилам:
2.Кислоты и основания.
Мэ =

М / n
Где Мэ – молярная масса эквивалента вещества,
М – молярная масса вещества,
n – основность кислоты (количество Н) или кислотность (количество групп ОН) основания.
Слайд 8Расчет молярной массы эквивалента вещества осуществляется по следующим правилам:
3.Соли и оксиды.
Мэ =

М / (N * n)
Где Мэ – молярная масса эквивалента вещества,
М – молярная масса вещества,
N – количество катионов в формуле,
n – формальный заряд катиона.
Слайд 9Расчет молярной массы эквивалента вещества осуществляется по следующим правилам:
4.Окислители и восстановители.
Мэ =

М / n
Где Мэ – молярная масса эквивалента вещества,
М – молярная масса вещества,
n – количество электронов, присоединяемое одной молекулой окислителя или отдаваемое одной молекулой восстановителя.
Слайд 10Молярная масса одного итого же вещества может рассчитываться по – разному, в

зависимости от его химических свойств.
Слайд 11Для экспериментального определения молярной массы эквивалента вещества необходимо найти массу данного вещества,

равноценную в химической реакции молярной массе эквивалента другого известного вещества
Слайд 12Источник
Задачи и упражнения по общей химии: Учеб. Пособие для вузов/Под.ред. В.А.Рабиновича и

Х..Рубиной.- 24-е изд., испр.- Л.: Химия, 1986.-272 с.,ил.











 Фуллерены (шары Бакминстера)
Фуллерены (шары Бакминстера) Алюминий и его органические производные
Алюминий и его органические производные Презентация на тему Кристаллические решетки 9 класс
Презентация на тему Кристаллические решетки 9 класс  Энергетический обмен
Энергетический обмен Ионная связь
Ионная связь Свойства солей, оксидов, оснований
Свойства солей, оксидов, оснований Генетические ряды Fe2+ и Fе3+. Качественные реакции на Fе2+ и Fе3+
Генетические ряды Fe2+ и Fе3+. Качественные реакции на Fе2+ и Fе3+ Презентация на тему Йод
Презентация на тему Йод  Роль Хеуорса, Фишера, Лемье в изучении структуры углеводов
Роль Хеуорса, Фишера, Лемье в изучении структуры углеводов Конструкционные и специальные материалы холодильной техники
Конструкционные и специальные материалы холодильной техники Перициклические реакции
Перициклические реакции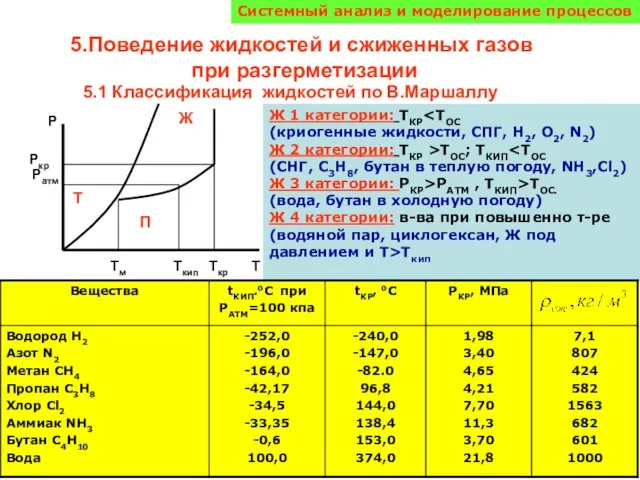 Поведение жидкостей и сжиженных газов при разгерметизации
Поведение жидкостей и сжиженных газов при разгерметизации Контроль качества лекарственных средств, производных карбоновых кислот и аминокислот
Контроль качества лекарственных средств, производных карбоновых кислот и аминокислот Получение армированных фотополимерных композиций
Получение армированных фотополимерных композиций Group 6 Cations
Group 6 Cations Русские ученые и топонимы в периодической системе химических элементов Д.И. Менделеева
Русские ученые и топонимы в периодической системе химических элементов Д.И. Менделеева Пищевые кислоты
Пищевые кислоты Предельные углеводороды. Алканы, насыщенные углеводороды, парафины, циклоалканы
Предельные углеводороды. Алканы, насыщенные углеводороды, парафины, циклоалканы Полиамиды (ПА)
Полиамиды (ПА) Окислители в пиросоставах
Окислители в пиросоставах Вебинар. Гидролиз солей
Вебинар. Гидролиз солей Совместимость материалов
Совместимость материалов Молярная масса вещества
Молярная масса вещества Композитные материалы
Композитные материалы Типы химической связи
Типы химической связи Презентация на тему Законы газового состояния вещества
Презентация на тему Законы газового состояния вещества  Development of the system of concepts on the topic redox reactions in the school course of inorganic chemistry
Development of the system of concepts on the topic redox reactions in the school course of inorganic chemistry Аммиак: состав, строение, свойства, применение
Аммиак: состав, строение, свойства, применение