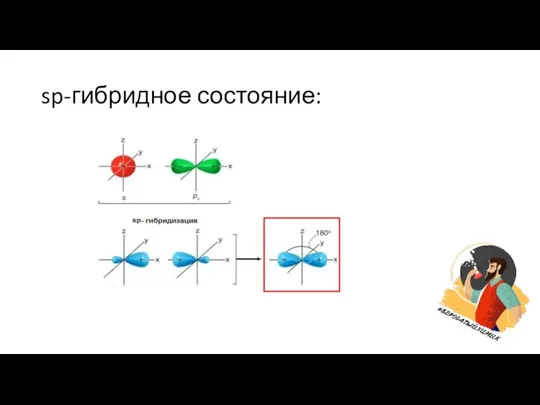
Слайд 2Гибридизация – это смешение атомных орбиталей различного типа (например, s, p и

d), в результате которого образуются одинаковые по форме и энергии гибридные орбитали (например, sp3, sp2 ,sp и т.д. ).
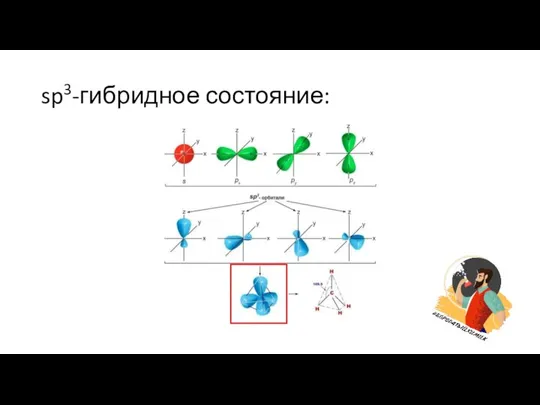
Слайд 4Особенности sp3-гибридного состояния:
Форма молекулы – тетраэдр;
Угол между связями в симметричной

молекуле – 109˚28’ (если в молекуле гибридизуется неподеленная электронная пара, угол может меняться);
Характерна для молекул алканов, циклоалканов, воды, аммиака, насыщенных спиртов и аминов, так же для атомов О, С, N, не содержащих кратных связей.
Слайд 5sp2-гибридное состояние:
sp2 – гибридизация
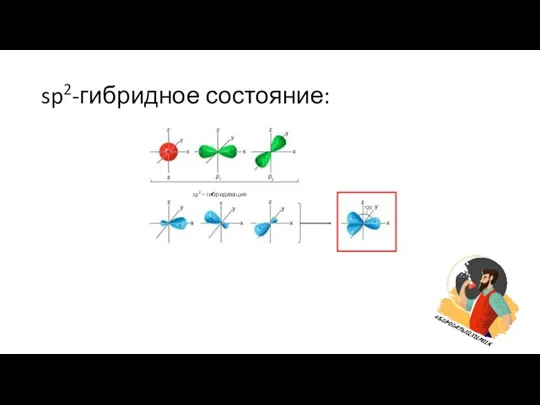
Слайд 6Особенности sp2-гибридного состояния:
Форма молекулы – треугольник;
Угол между связями в симметричной молекуле

- 120˚;
Характерна для атомов О, С, N, с одной двойной связью. Т.е. следующих классов веществ: алкены, диены, арены, циклоалкены, циклодиены и многие другие.




 Химическое равновесие
Химическое равновесие Химия и география. Блиц-опрос. 7 класс
Химия и география. Блиц-опрос. 7 класс Амилаза. Строение амилазы
Амилаза. Строение амилазы Моющие и чистящие средства
Моющие и чистящие средства Основные химические законы
Основные химические законы Соли: получение
Соли: получение Синтетическое моторное масло. Маркировка моторных масел
Синтетическое моторное масло. Маркировка моторных масел Khim_8
Khim_8 Химические реакции
Химические реакции Систематизация знаний по периодической системе химических элементов
Систематизация знаний по периодической системе химических элементов химия
химия Nevarne snovi
Nevarne snovi Основания. Классификация
Основания. Классификация Стелс-материалы
Стелс-материалы Тип кристаллической решетки у белого фосфора…. Тест
Тип кристаллической решетки у белого фосфора…. Тест Классификация и свойства кислот
Классификация и свойства кислот Сeквенирование нуклеиновых кислот
Сeквенирование нуклеиновых кислот Набор для выращивания монокристалла. Защита проекта
Набор для выращивания монокристалла. Защита проекта Алканы. Строение, номенклатура, изомерия, физические свойства
Алканы. Строение, номенклатура, изомерия, физические свойства Реакции разложения и соединения
Реакции разложения и соединения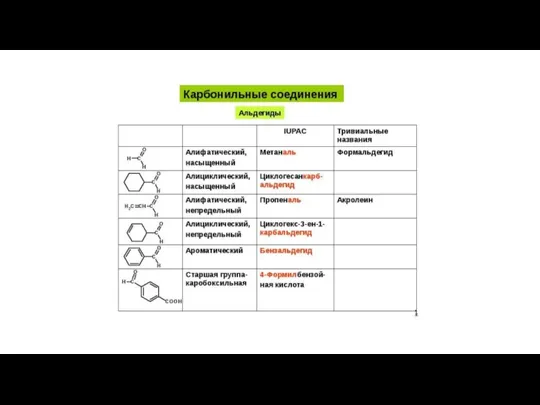 Карбонильные соединения (альдегиды)
Карбонильные соединения (альдегиды) карбоновые кислоты
карбоновые кислоты Вуглеводи. Групи
Вуглеводи. Групи Вычисление температур стеклования полимера при различных степенях отверждения смолы
Вычисление температур стеклования полимера при различных степенях отверждения смолы Сера
Сера Валенттілік. Атом-молекулалы ілім
Валенттілік. Атом-молекулалы ілім Классификация органических соединений
Классификация органических соединений Метанол. Краткая характеристика
Метанол. Краткая характеристика