Содержание
- 2. I. Введение Неорганические ионы (анионов и катионов) Органические ионы Углеводы Гликопротеины и др. Аналиты (определяемые вещества)
- 3. Экологический контроль (природные и сточные воды, метеорологический контоль, контроль промышленных выбросов и т.д.) Водоподготовка (питьевая вода)
- 4. Особенности метода В основе - стехиометрический ионный обмен Сорбенты (неподвижная фаза) – ионообменнкики разной силы невысокой
- 5. Возможность определять количественно сразу несколько компонентов Экспрессность Высокая чувствительность (до 10-9 г/мл без концентрирования) Возможность частичной
- 6. Сложность синтеза ионообменных сорбентов Эффективность разделения хуже, чем в стандартной обращенофазной ВЭЖХ Сильно коррозионная среда Чувствительность
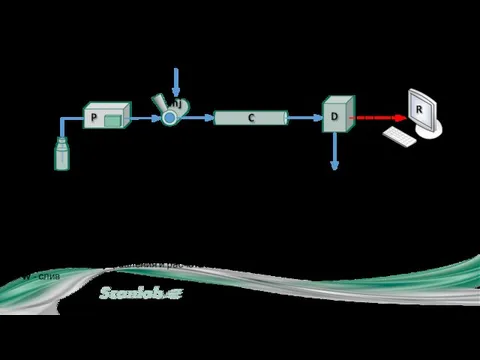
- 7. I. ИХ система P Inj C D R P – насос - для подачи подвижной фазы
- 8. I. Введение
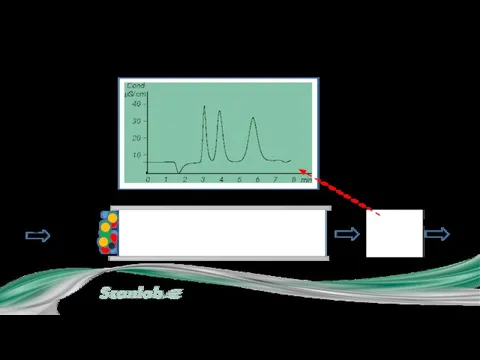
- 9. I. Процесс разделения на колонке Из инжектора Детектор Слив Проба Колонка
- 10. I. Введение Основные характеристики «типичного» ИХ метода
- 11. I.1. Ионный обмен Матрица Активные группы зафиксированные ионы
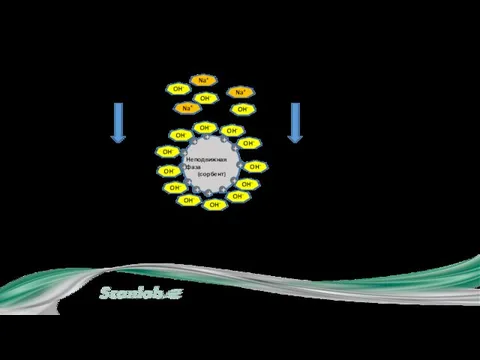
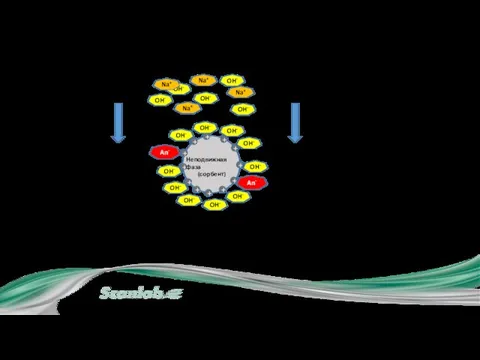
- 12. I.1. Схема ионного обмена Na+ OH- Na+ OH- OH- OH- OH- OH- OH- OH- OH- OH-
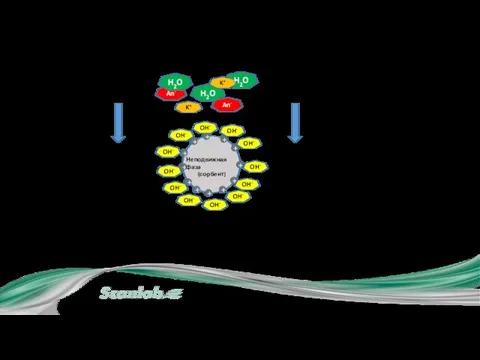
- 13. I.1. Схема ионного обмена An- H2O OH- H2O H2O K+ An- OH- OH- OH- OH- OH-
- 14. I.1. Схема ионного обмена Na+ OH- Na+ Разделение анионов OH- OH- OH- OH- OH- OH- OH-
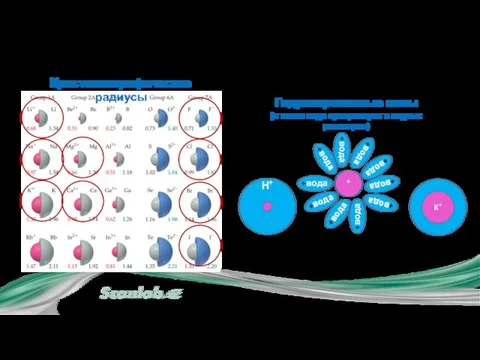
- 15. Кристаллографические радиусы Гидратированные ионы (в таком виде сусществуют в водных растворах) + I.1. Схема ионного обмена
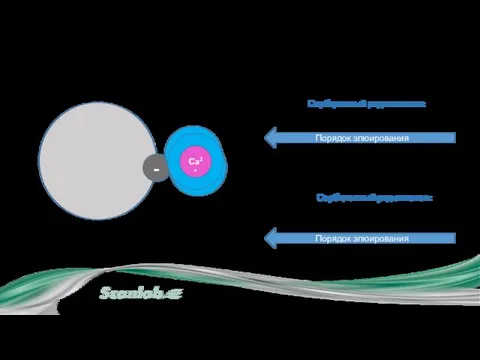
- 16. Сорбционный ряд катионов: Ba+2 > Pb+2 > Ca+2 > Cu+2 > Mg+2 > Cs+ > Rb+
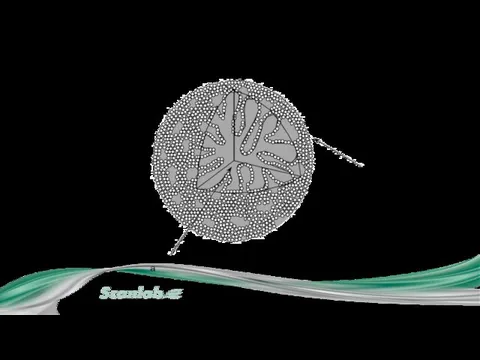
- 17. 2. Ионообменные сорбенты Матрица Активные группы зафиксированные ионы
- 18. I.2. Ионообменные сорбенты Сорбент должен иметь низкую ионообменную ёмкость (ограниченное количество активных центров): Катиониты : 4
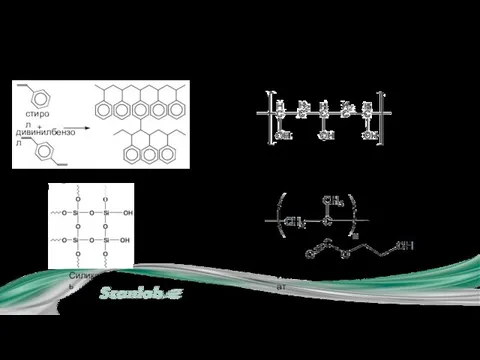
- 19. I.2. Ионообменные сорбенты. Матрицы стирол дивинилбензол Сополимер стирола и дивинилбензола Силикагель Поливиниловый спирт Полигидроксиметакрилат
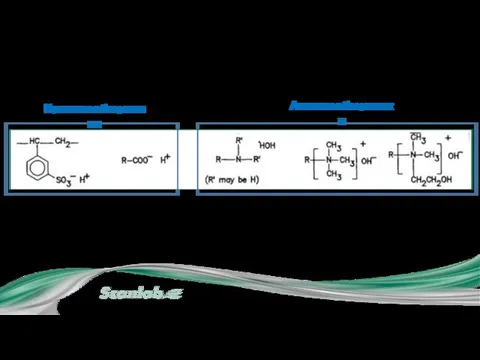
- 20. I.2. Ионообменные сорбенты . Активные группы Сульфо-группа Сильный Карбоксильная-группа Слабый Вторичные или третичные амино-группы Слабый Катионообменники
- 21. I.3. Подвижные фазы Особенности подвижных фаз Практически всегда – водные растворы электролитов – солей, кислот и
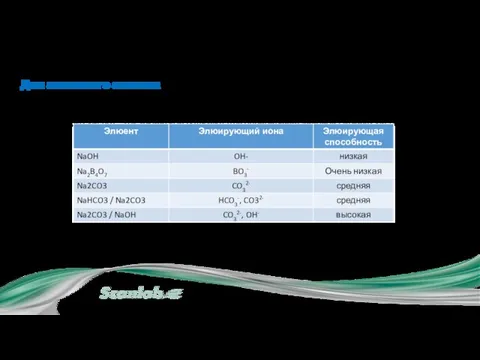
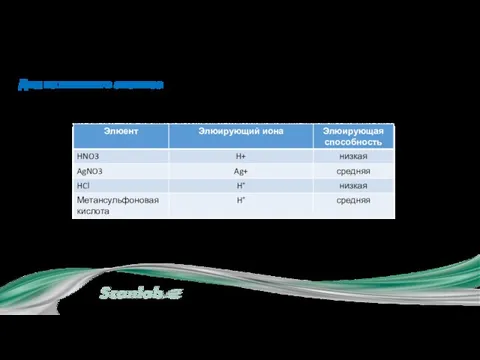
- 22. Для анионного анализа Наиболее распространенными элюентами в ионной хроматографии анионов являются разбавленные растворы солей слабых кислот.
- 23. Для катионного анализа Наиболее распространенными элюентами в ионной хроматографии анионов являются разбавленные растворы солей слабых кислот.
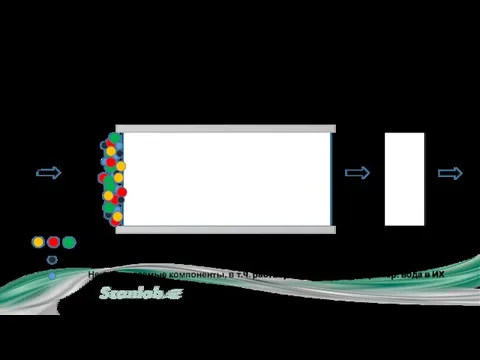
- 24. 2.1 Разделение в колонке и детектирование Из инжектора Детектор Слив Проба Колонка Аналит (то, что мы
- 25. 2.1 Разделение в колонке и детектирование
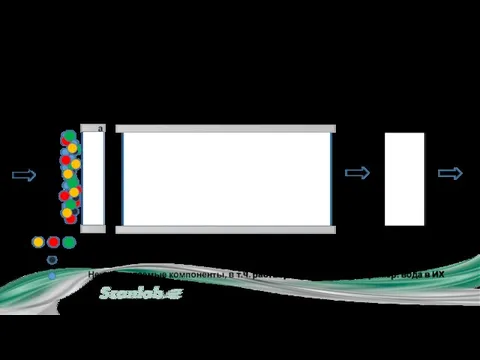
- 26. 2.1 Защитные предколонки
- 27. 2.1 Защитные предколонки Из инжектора Детектор Слив Проба Колонка Аналит (то, что мы ищем в пробах,
- 28. Спасибо за внимание!
- 30. Скачать презентацию












 1_
1_ Планарные потенциометрические сенсоры на основе пилларарена -DNS-162
Планарные потенциометрические сенсоры на основе пилларарена -DNS-162 Ископаемые углеводороды
Ископаемые углеводороды Презентация на тему Сложные эфиры
Презентация на тему Сложные эфиры  Водород
Водород Кремний Полупроводники в электронике_Горб
Кремний Полупроводники в электронике_Горб Влияние пластифицирующих добавок на свойства декоративного мелкозернистого бетона
Влияние пластифицирующих добавок на свойства декоративного мелкозернистого бетона Переработка нефти
Переработка нефти Металлы. Контрольная работа
Металлы. Контрольная работа Электролитическая диссоциация
Электролитическая диссоциация Исследование физико-химических свойств щавелевой кислоты
Исследование физико-химических свойств щавелевой кислоты Природные источники углеводородов
Природные источники углеводородов Наблюдения в сходящемся свете. Коноскопия
Наблюдения в сходящемся свете. Коноскопия Презентация на тему Биополимеры
Презентация на тему Биополимеры  Разбор заданий
Разбор заданий Турнир знатоков химии
Турнир знатоков химии Неделя химии в МБОУ (викторина)
Неделя химии в МБОУ (викторина) Ліпіди і їх роль в життєдіяльності клітини
Ліпіди і їх роль в життєдіяльності клітини Ароматические углеводороды (арены)
Ароматические углеводороды (арены) Презентация на тему Классификация химических реакций
Презентация на тему Классификация химических реакций  Гидролиз. Виды гидролиза
Гидролиз. Виды гидролиза Применение хидких кристалов в промышленности
Применение хидких кристалов в промышленности Плотность вещества
Плотность вещества Соли в свете теории электролитической диссоциации
Соли в свете теории электролитической диссоциации Физические свойства металлов
Физические свойства металлов Водневий та металічний звязок
Водневий та металічний звязок Основания
Основания Диссоциация веществ
Диссоциация веществ