Слайд 2 Ваша цель:
1.Познакомиться с молярным объемом газов;
2. Изучить основные законы

химии: закон Авогадро, закон Гей – Люссака;
3. Научится решать типовые задачи;
Слайд 3
Девиз урока:
У пространства нет размера, а у знаний нет предела!

Слайд 4
Проверка домашнего задания:

Слайд 6
2. С какими законами вы познакомились на прошлом уроке?

Слайд 7
3. В чем заключается сущность закона сохранения массы веществ?

Слайд 84. Сформулируйте закон постоянства состава и укажите, для каких веществ он всегда

строго выполняется?
Слайд 9
5. Что такое массовая доля и как она рассчитывается?

Слайд 11
Вопрос:
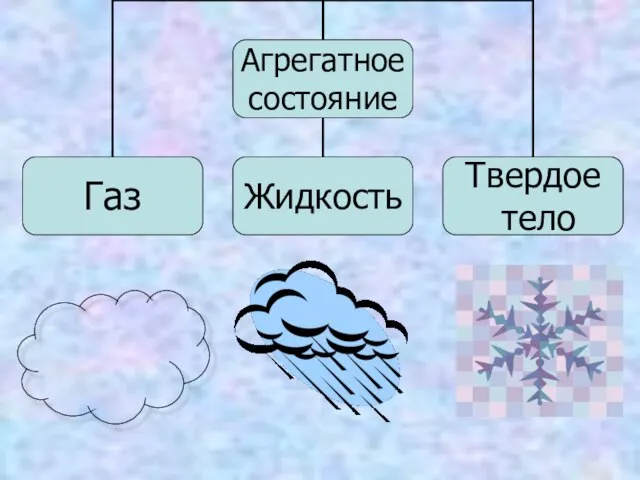
В каких агрегатных состояниях могут находится вещества?

Слайд 13Агрегатное состояние веществ и переходы между ними

Слайд 15 Амедео Авогадро
высказал предположение в 1811 году, что
в одинаковых объемах различных газов

находится одно и тоже число молекул.
Позже эта гипотеза стала законом Авогадро.
Слайд 16 Закон Авогадро:
В равных объемах различных газов при одинаковых условиях (температура,

давление) содержится одинаковое число молекул.
Слайд 17Первое следствие из закона Авогадро:
Одинаковое число молекул различных газов при одинаковых условиях

занимают одинаковый объем.
Слайд 19Молярный объем газа Vm — величина, определяемая отношением объема данной порции газа

V к химическому количеству вещества n в этой порции:
Слайд 20Нормальные условия: температура — 0°С давление — 101,325 кПа

Слайд 21Молярный объем любого газа при нормальных условиях:
Второе следствие из закона Авогадро

Слайд 22Вычисление по уравнению реакции объема газа по известному химическому количеству одного из

веществ
Слайд 23Задача:
Какой объем водорода (н. у.) можно получить при действии соляной кислоты HCl

на цинк химическим количеством 0,5 моль?
Слайд 244. Закон объемных отношений (закон Гей-Люссака):

Слайд 25 Гей-Люссак (1778-1850)
При неизменных температуре и давлении объемы
вступающих в реакцию газов относятся

друг к другу,
а также к объемам образующихся газообразных продуктов
как небольшие целые числа.
Слайд 26Расчет объемных отношений газов по химических уравнениям

Слайд 27Обобщение
Объем газов определяется не размером молекул, а расстоянием между ними, которые

при одинаковых условиях для всех газов примерно одинаковы.
Слайд 28Задача:
Найдите V хлора который потребуется для получения 80 г хлороводорода? какой

V азота имеет такую же массу, что и 40,32 л NH3 (н.у.)?
Слайд 29В равных объемах различных газов при одинаковых условиях (давление, температура) содержится одинаковое

число молекул.
Слайд 30Молярный объем газа есть объем его порции химическим количеством 1 моль. При

нормальных условиях (температура 0°С и давление — 101,325 кПа) молярный объем любого газа является величиной постоянной, равной 22,4 дм3/моль.
Слайд 31Коэффициенты перед газообразными веществами в уравнениях химических реакций соответствуют объемным отношениям этих

веществ.
Слайд 32Закрепление
Какой V (при н. у.) занимают (I вариант) – любой газ химическим

количеством 2 моль, (II - вариант) – азот массой 2 г.
Слайд 33I вариант
Какой объем углерод (IV) – оксида можно получить действием избытка разбавленной

серной кислоты на натрий-карбонат химическим количеством 0,35 моль?
II вариант
Какой объем кислорода потребуется для полного сжигания 200 дм3 (при н.у.) метана и какой объем углерод (IV)-оксида при этом образуется?
Слайд 34Оцените своё состояние после урока
Мне хорошо Как всегда Уныло Я много

знаю Я плохо понял
и умею
Слайд 35Домашнее задание:
§ 5 стр. 29-32, 35-37. Упр. 1-7, 12.


































 Алкины
Алкины Замедленное коксование нефтяного сырья
Замедленное коксование нефтяного сырья Презентация на тему Химические свойства кислот
Презентация на тему Химические свойства кислот  Празеодим
Празеодим Трансляция. Активирование аминокислоты
Трансляция. Активирование аминокислоты Аммиак. Соли аммония
Аммиак. Соли аммония Презентация на тему Природный газ
Презентация на тему Природный газ  Алотропия углерода
Алотропия углерода Презентация на тему История семи великих камней Алмазного фонда России
Презентация на тему История семи великих камней Алмазного фонда России  Полиморфизм кристаллов изатина
Полиморфизм кристаллов изатина Неорганические вещества
Неорганические вещества Способы получения веществ 14 (IVА) группы элементов
Способы получения веществ 14 (IVА) группы элементов Приключение кислорода
Приключение кислорода Химия в нашем доме. Введение в курс. Урок №1
Химия в нашем доме. Введение в курс. Урок №1 Титриметрический анализ
Титриметрический анализ Основания, их классификация и свойства
Основания, их классификация и свойства Презентация на тему Азотная кислота и ее свойства
Презентация на тему Азотная кислота и ее свойства  Презентация для заочников
Презентация для заочников Периодическая система химических элементов Д.И. Менделеева
Периодическая система химических элементов Д.И. Менделеева Предельные одноатомные спирты: свойства, получение, применение
Предельные одноатомные спирты: свойства, получение, применение Опасная бытовая химия!
Опасная бытовая химия! Алкены. Тестирование
Алкены. Тестирование Получение функциональных плёнок на основе TiO2
Получение функциональных плёнок на основе TiO2 Алюминий и алюминиевые сплавы
Алюминий и алюминиевые сплавы 10_KISLOTNO_OSNOVNOE_TITROVANIE
10_KISLOTNO_OSNOVNOE_TITROVANIE Вещества и материалы. Строение и свойства вещества. 6 класс
Вещества и материалы. Строение и свойства вещества. 6 класс Основы химической кинетики
Основы химической кинетики Презентация на тему Использование Икт в преподавании химии
Презентация на тему Использование Икт в преподавании химии