Содержание
Слайд 21. Заряд ядра атома +8 имеют атомы химического элемента:
А). азота б) кислорода
В)
1. Заряд ядра атома +8 имеют атомы химического элемента:
А). азота б) кислорода
В)

серы г) хлора
2. Число общих электронных пар в молекуле хлора
А) одна Б) две В) три Г) четыре
3. Ковалентная полярная связь имеется в молекуле вещества, формула которого:
А) Р₄ Б) СО₂ В) О₂ г) NaCl
2. Число общих электронных пар в молекуле хлора
А) одна Б) две В) три Г) четыре
3. Ковалентная полярная связь имеется в молекуле вещества, формула которого:
А) Р₄ Б) СО₂ В) О₂ г) NaCl
Слайд 34. Степень окисления азота в ряду веществ, формулы которых N₂ - NO
4. Степень окисления азота в ряду веществ, формулы которых N₂ - NO

- NO₂ - HNO₃
А) повышается от 0 до +5
Б) понижается от +5 до 0
В) повышается от -3 до +5
Г) понижается от +5 до +2
5. Уравнение химической реакции
H₂S + Cl₂ = 2HCl + S соответствует схеме превращения хлора: А) Clº → Cl⁻ˈ
б) Cl⁻ˈ → Cl⁺ в) Clº → Cl ⁺ г) Cl⁻ˈ → Clº
Слайд 46. Вещество Х в ряду превращений
СО₂ → Х → Са(НСО₃)₂ →СО₂
6. Вещество Х в ряду превращений
СО₂ → Х → Са(НСО₃)₂ →СО₂

имеет формулу:
А) Са(ОН)₂ Б)СО В) СаСО3 г) СаО
7. Химическая реакция возможна между веществами, формулы которых:
А) H₂SO₄ и CO₂ Б) H₂SO₄ и Au
В) H₂SO₄ и BaSO₄ ) H₂SO₄ и MgO
8. Реактивом на хлорид- анион является катион:
а) Н ⁺ б)Аg⁺ в) Ba²⁺ г)NH⁴⁺
9. Вычислите массу (в кг) хлороводорода, который получается при взаимодействии 4, 48 м³ хлора с избытком водорода.
Запишите уравнения реакций по схеме:
P → Zn₃P₂ → P₂O₅ → H₃PO₄ → Na₃PO₄ → Ag₃ PO₄
А) Са(ОН)₂ Б)СО В) СаСО3 г) СаО
7. Химическая реакция возможна между веществами, формулы которых:
А) H₂SO₄ и CO₂ Б) H₂SO₄ и Au
В) H₂SO₄ и BaSO₄ ) H₂SO₄ и MgO
8. Реактивом на хлорид- анион является катион:
а) Н ⁺ б)Аg⁺ в) Ba²⁺ г)NH⁴⁺
9. Вычислите массу (в кг) хлороводорода, который получается при взаимодействии 4, 48 м³ хлора с избытком водорода.
Запишите уравнения реакций по схеме:
P → Zn₃P₂ → P₂O₅ → H₃PO₄ → Na₃PO₄ → Ag₃ PO₄
 Коррозия металлов
Коррозия металлов Оксиды. Классификация. Химические и физические свойства
Оксиды. Классификация. Химические и физические свойства Аммиак. Азот
Аммиак. Азот Статистика в аналитической химии
Статистика в аналитической химии Контроль якості імуногематологічних досліджень за допомогою діагностичних моноклональних реагентів та стандартних еритроцитів
Контроль якості імуногематологічних досліджень за допомогою діагностичних моноклональних реагентів та стандартних еритроцитів Относительный вклад % буферных систем крови в поддержание в ней протолитического гомеостаза
Относительный вклад % буферных систем крови в поддержание в ней протолитического гомеостаза Износостойкие стали и сплавы
Износостойкие стали и сплавы Составление уравнений окислительно-восстановительных реакций
Составление уравнений окислительно-восстановительных реакций Алкадиены. Физические свойства
Алкадиены. Физические свойства Растворы. Лекция 7
Растворы. Лекция 7 Изучение геохимических свойств редкоземельных элементов
Изучение геохимических свойств редкоземельных элементов Кремний. Технический кремний
Кремний. Технический кремний Календарь юного химика. 2013-2014 учебный год
Календарь юного химика. 2013-2014 учебный год Обратимые и необратимые химические реакции. Химическое равновесие
Обратимые и необратимые химические реакции. Химическое равновесие Железо и его соединения
Железо и его соединения Магматические породы
Магматические породы Условия хранения и подготовка скоропортящихся грузов к перевозкам
Условия хранения и подготовка скоропортящихся грузов к перевозкам Тест по неметаллам
Тест по неметаллам строение атома
строение атома Алканы. Строение. Изомерия и номенклатура
Алканы. Строение. Изомерия и номенклатура Общие химические свойства неметаллов
Общие химические свойства неметаллов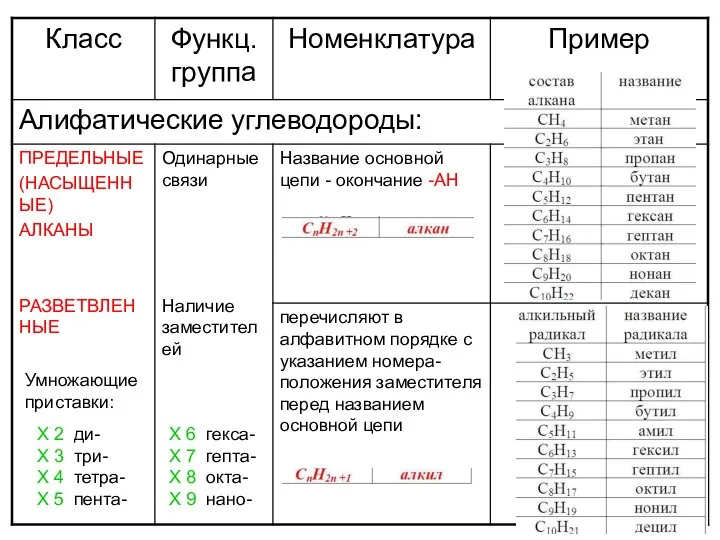 Алифатические углеводороды
Алифатические углеводороды Каких заданий не бывает на ЕГЭ по химии и почему
Каких заданий не бывает на ЕГЭ по химии и почему Сырье, продукты, параметры гидроочистки
Сырье, продукты, параметры гидроочистки Электронное и пространственное строение алкенов. Гомология и изомерия алкенов
Электронное и пространственное строение алкенов. Гомология и изомерия алкенов Решение задач. Подготовка к контрольной работе по химии
Решение задач. Подготовка к контрольной работе по химии Взаимодействие кислот с металлами. Кислоты-окислители
Взаимодействие кислот с металлами. Кислоты-окислители Реакция полимеризации
Реакция полимеризации