Содержание
- 3. Особенные свойства муравьиной кислоты Муравьиную кислоту можно рассматривать , как молекулу содержащую две функциональные группы. Это
- 4. Специфические свойства муравьиной кислоты. Реакция «серебрянного зеркала» HCOOH + 2[Ag(NH3)2 → 4NH3 ↑ + CO2 ↑
- 5. 5. Муравьиная кислота окисляется перманганатом калия до углекислого газа: 5HCOOH + 2KMnO4 + 3H2SO4 → 5CO2
- 6. Специфические свойства карбоновых кислот 1. Образование функциональных производных R-CO-X R-COOH + PCl5 → R-CO-Cl + POCl3
- 7. 2. Образование амидов. CH3COOH + NH3→CH3COONH4 t˚C→ CH3CONH2 + H2O При взаимодействии аммиака с карбоновыми кислотами
- 8. 3. Образование ангидридов. С помощью оксида фосфора (V) можно дегидратировать (то есть отщепить воду) карбоновую кислоту
- 9. Особенности непредельных кислот (акриловой и олеиновой) 1.Реакции присоединения Присоединение воды и бромоводорода к акриловой кислоте происходит
- 11. Скачать презентацию








 Стекло. История открытия. Самое древнее производство Эпохи фараонов
Стекло. История открытия. Самое древнее производство Эпохи фараонов Основи молекулярно-кінетичної теорії
Основи молекулярно-кінетичної теорії Кислородсодержащие органические соединения
Кислородсодержащие органические соединения Подготовка к ГИА по химии
Подготовка к ГИА по химии Презентация на тему Научная химическая лаборатория Ломоносова
Презентация на тему Научная химическая лаборатория Ломоносова  Гидроксиды металлов
Гидроксиды металлов Химические равновесия в растворах. Лекция 2 часть 2
Химические равновесия в растворах. Лекция 2 часть 2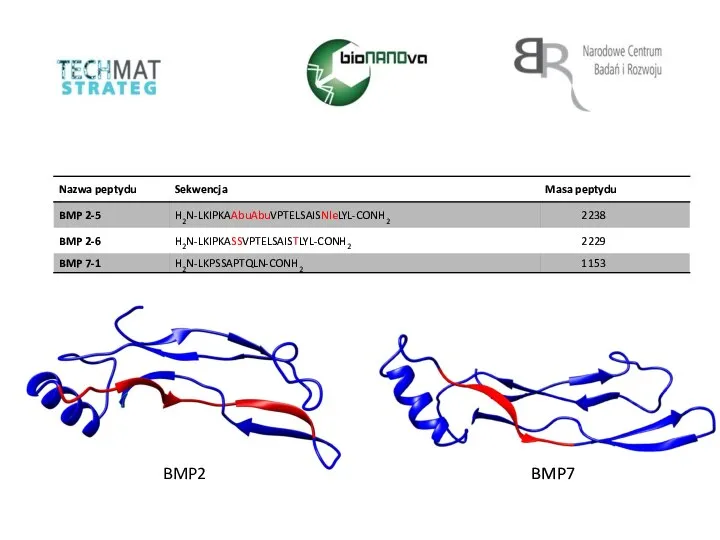 Nazwa peptydu. Sekwencja
Nazwa peptydu. Sekwencja Полімери. Пінополістирол
Полімери. Пінополістирол 5 группа элементов
5 группа элементов Химические свойства насыщенных альдегидов и кетонов (продолжение)
Химические свойства насыщенных альдегидов и кетонов (продолжение) Водородная химическая связь
Водородная химическая связь Коррозия. способы защиты от коррозии
Коррозия. способы защиты от коррозии Презентация на тему Спирты (9 класс)
Презентация на тему Спирты (9 класс)  Электролиз воды
Электролиз воды Генетические ряды углеводородов. Обобщение и систематизация знаний
Генетические ряды углеводородов. Обобщение и систематизация знаний Адсорбционные материалы. Цеолиты
Адсорбционные материалы. Цеолиты Химическая термодинамика
Химическая термодинамика Термодинамическое равновесие между фазами
Термодинамическое равновесие между фазами Физическая химия. Вводная лекция
Физическая химия. Вводная лекция Строение вещества. ОВР. Окислительно-восстановительные реакции
Строение вещества. ОВР. Окислительно-восстановительные реакции Материаловедение. Технология конструкционных материалов. Диаграмма состояния Fe-Fe3C
Материаловедение. Технология конструкционных материалов. Диаграмма состояния Fe-Fe3C Мыльная история
Мыльная история Оксиды. Классификация. Химические и физические свойства
Оксиды. Классификация. Химические и физические свойства алотропні модифікації неметалів
алотропні модифікації неметалів Презентация для заочников
Презентация для заочников Генетическая связь неорганических соединений
Генетическая связь неорганических соединений Алкины. Понятие об алкинах
Алкины. Понятие об алкинах