Содержание
- 2. Аммиак может быть обязан своим названием оазису бога Аммона в Северной Африке, находящемуся на перекрестке караванных
- 3. По некоторым другим сведениям, аммиак мог получить современное название от древнеегипетского слова «амониан». Так называли всех
- 4. Сокращенное название «аммиак» которым мы всегда пользуемся, ввел в обиход в 1801 году русский ученый -
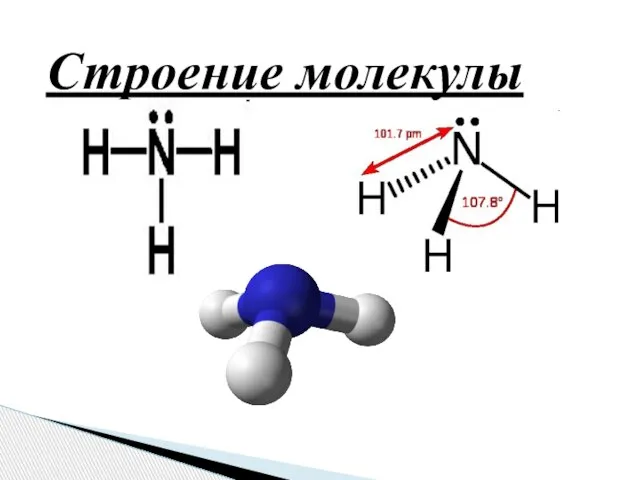
- 5. Строение молекулы
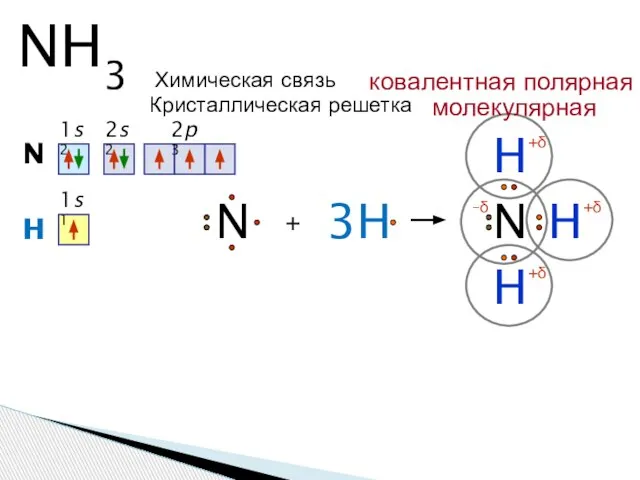
- 6. NH3 N 1s2 2s2 2p3 + H N H H 3H H N 1s1 +δ +δ
- 7. Молекула аммиака имеет форму тригональной пирамиды с атомом азота в вершине. Три неспаренных p-электрона атома азота
- 8. Физические свойства (при н.у. ) бесцветный газ с резким характерным запахом (запах нашатырного спирта) легче воздуха
- 9. По физиологическому действию на организм относится к группе веществ удушающего и нейротропного действия, способных вызвать токсический
- 10. Получение аммиака Для получения аммиака в лаборатории используют действие сильных щелочей на соли аммония: 2NH4Cl +
- 11. Промышленный способ получения аммиака основан на прямом взаимодействии водорода и азота: N2(г) + 3H2(г) ↔ 2NH3(г)
- 12. Химические свойства аммиака Для аммиака характерны реакции: 1) с изменением степени окисления атома азота (реакции окисления);
- 13. Реакции с изменением степени окисления атома азота (реакции окисления) N-3 → N0→ N+2 NH3-сильный восстановитель
- 14. с кислородом Горение аммиака (при нагревании) 4NH3 + 3O2 → 2N2 + 6H20 Каталитическое окисление амииака
- 15. с оксидами металлов 2NH3 +3CuO =3Cu + N2 +3H2O
- 16. с сильными окислителями 2NH3 + 3Cl2 = N2 + 6HCl (при нагревании)
- 17. Реакции без изменения степени окисления атома азота (присоединение - образование иона аммония NH4+ по донорно-акцепторному механизму
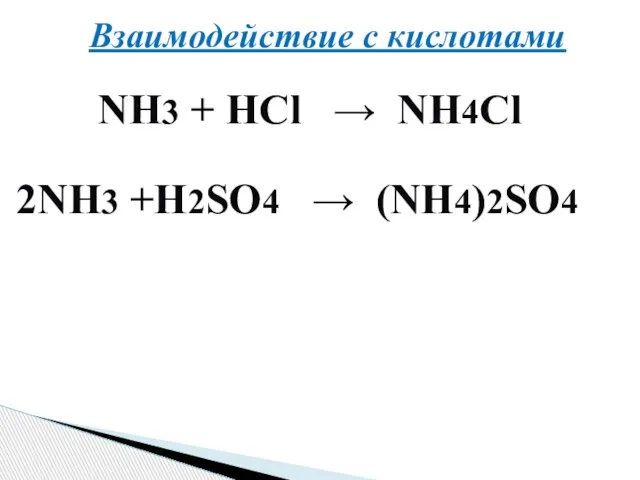
- 18. Взаимодействие с кислотами NH3 + HCl → NH4Cl 2NH3 +H2SO4 → (NH4)2SO4
- 19. Взаимодействие с водой NH3 + H2O = NH4OH При добавлении фенолфталеина‑ раствор становится малиновым, так как
- 20. Применение аммиака Производство пластмасс и волокон 2. В составе моющих средств
- 21. 3. Производство азотных удобрений 4. В сельском хозяйстве
- 22. 5. Производство азотной кислоты 6. Получение взрывчатых веществ
- 23. 7. В медицине
- 24. По объемам производства аммиак занимает одно из первых мест; ежегодно во всем мире получают около 100
- 26. Скачать презентацию



















 20170625_otkrytyy_integrirovannyy_urok_himiya-geografiya
20170625_otkrytyy_integrirovannyy_urok_himiya-geografiya Лекция 1
Лекция 1 Теория химического строения органических веществ А.М. Бутлерова
Теория химического строения органических веществ А.М. Бутлерова Металлическая и водородная и химическая связь
Металлическая и водородная и химическая связь Бытовая химия
Бытовая химия Обсидиан
Обсидиан Предмет органической химии
Предмет органической химии Презентация на тему Выдающиеся русские ученые химики
Презентация на тему Выдающиеся русские ученые химики  Презентация на тему Оксиды углерода
Презентация на тему Оксиды углерода  Янтарь
Янтарь Нанокристаллические и аморфные металлы и сплавы
Нанокристаллические и аморфные металлы и сплавы Арены. Бензол
Арены. Бензол Азот N2
Азот N2 10_KISLOTNO_OSNOVNOE_TITROVANIE
10_KISLOTNO_OSNOVNOE_TITROVANIE Карбоновые кислоты
Карбоновые кислоты Известная и неизвестная вода
Известная и неизвестная вода Натрий, свойства атома, химические и физические свойства
Натрий, свойства атома, химические и физические свойства кислородосодерж. орг. соед. (1)
кислородосодерж. орг. соед. (1) Расчеты по уравнениям химических реакций
Расчеты по уравнениям химических реакций Стехиометрические законы химии
Стехиометрические законы химии Органическая химия: Жиры
Органическая химия: Жиры Классификация реакций. Теория-кинетика
Классификация реакций. Теория-кинетика Кислые горные породы
Кислые горные породы Соединения серы
Соединения серы Фотометрический анализ
Фотометрический анализ Создание из таблицы Менделеева и растворимости мини-справочник - шпаргалку
Создание из таблицы Менделеева и растворимости мини-справочник - шпаргалку Классификация аминокислот в зависимости от природы радикалов
Классификация аминокислот в зависимости от природы радикалов Конструкционные и специальные материалы холодильной техники
Конструкционные и специальные материалы холодильной техники