Содержание
- 2. Электролиты - вещества, растворы и расплавы которых проводят электрический ток (NaCl, NaOH, HCl).
- 3. Электролиты
- 4. Кислоты- это электролиты, которые диссоциируют на катионы водорода и анионы кислотного остатка. HCI = H+ +
- 5. Многоосновные кислоты диссоциируют ступенчато: 1 стадия: H3PO4 H+ + H2PO4- 2 стадия: H2PO4- H+ + HPO42-
- 6. Основания- это электролиты, которые диссоциируют на катионы металлов и анионы гидроксогрупп. NaOH = Na+ + OH-
- 7. Соли - это электролиты, которые диссоциируют на катионы металла и анионы кислотного остатка. Na Cl =
- 8. Вывод: Общие свойства кислот объясняются наличием в них ионов H+ , а общие свойства щелочей –
- 10. Скачать презентацию






 Электролиз. Правила электролиза
Электролиз. Правила электролиза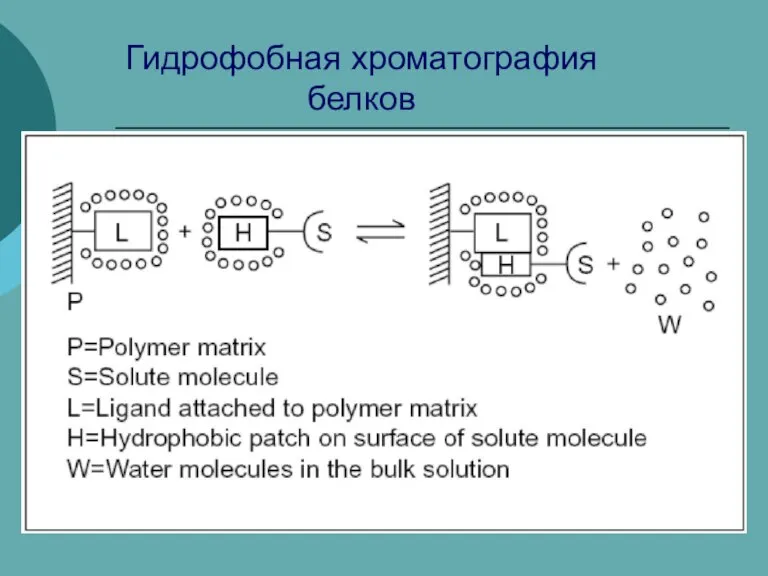 Гидрофобная хроматография белков
Гидрофобная хроматография белков 7609f31d31514fe19b6df19a98197139 (1)
7609f31d31514fe19b6df19a98197139 (1) Бикомпонентные покрытия
Бикомпонентные покрытия Сера и ее соединения
Сера и ее соединения Презентация на тему Строение атома Химическая связь
Презентация на тему Строение атома Химическая связь  Взаимодействие плазмы с поверхностью. Проблемы термоядерного реактора
Взаимодействие плазмы с поверхностью. Проблемы термоядерного реактора Определение времени прохождения диффузии
Определение времени прохождения диффузии Презентация на тему Сплавы металлов
Презентация на тему Сплавы металлов  Химия. Спирты
Химия. Спирты Углерод и его аллотропные модификации. Органическая химия - химия углерода
Углерод и его аллотропные модификации. Органическая химия - химия углерода Газообразные (газ)
Газообразные (газ) Химические свойства алкенов. Получение
Химические свойства алкенов. Получение Хлорорганические соединения
Хлорорганические соединения Химические элементы
Химические элементы Соли: получение
Соли: получение Азотная кислота
Азотная кислота Белки-1 2020
Белки-1 2020 Основания (Ме+n(ОН)-n)
Основания (Ме+n(ОН)-n) Расчётно-графическая работа по теме Мыловарение
Расчётно-графическая работа по теме Мыловарение Альдегиды. Получение и применение
Альдегиды. Получение и применение Презентация на тему Изотопы
Презентация на тему Изотопы  Типы химических реакций
Типы химических реакций Растительные жиры. Пальмовое масло
Растительные жиры. Пальмовое масло Химия в быту
Химия в быту Кристаллическое строение металлов и сплавов. Аморфные и кристаллические тела
Кристаллическое строение металлов и сплавов. Аморфные и кристаллические тела Алкены. Ҳимические свойства алкенов
Алкены. Ҳимические свойства алкенов Порядок в жидкостях
Порядок в жидкостях