Слайд 2К(-) «восстановитель», т. к. происходит процесс передачи электронов катионам из раствора или

расплава.
А(+) «окислитель», т. к. происходит процесс отдачи электронов анионами.
Слайд 3Проведение электролиза с помощью инертного (нерасходуемого) анода:
Два конкурирующих окислительных и два восстановительных

процесса
К (-): восстановление катионов и ионов водорода
А (+): окисление анионов и гидроксид-ионов
Слайд 4Проведение электролиза с помощью активного (расходуемого) анода:
К (-): восстановление катионов соли и

ионов водорода, восстановление катионов металла, полученных при растворении анода
А (+): окисление анионов и гидроксид-ионов, анодное растворение металла – материала анода.
Слайд 5Правила электролиза с помощью инертного (нерасходуемого) анода:
На аноде могут образовываться следующие продукты:
а)

при электролизе растворов, содержащих ионы: F и анионы кислородосодержащих кислот, ОН – выделяется кислород
б) при окислении галогенид-ионов выделяются свободные галогены
в) при окислении анионов органических кислот происходит процесс:
Слайд 6На катоде:
а) При электролизе растворов солей, содержащих ионы, расположенные в ряду напряжений

левее алюминия, на катоде выделяется водород, если правее, то металл.
б) При электролизе растворов солей, содержащих ионы, расположенные в ряду алюминием и водородом, на катоде могут протекать конкурирующие процессы как восстановления катионов, так и выделения водорода.











 Типы кристаллических решеток
Типы кристаллических решеток Судын оксидтермен реакциясы
Судын оксидтермен реакциясы Ионная химическая связь
Ионная химическая связь Классы неорганических соединений
Классы неорганических соединений Истина - дочь времени, а не авторитета
Истина - дочь времени, а не авторитета Презентация на тему Виды кристаллических решеток
Презентация на тему Виды кристаллических решеток 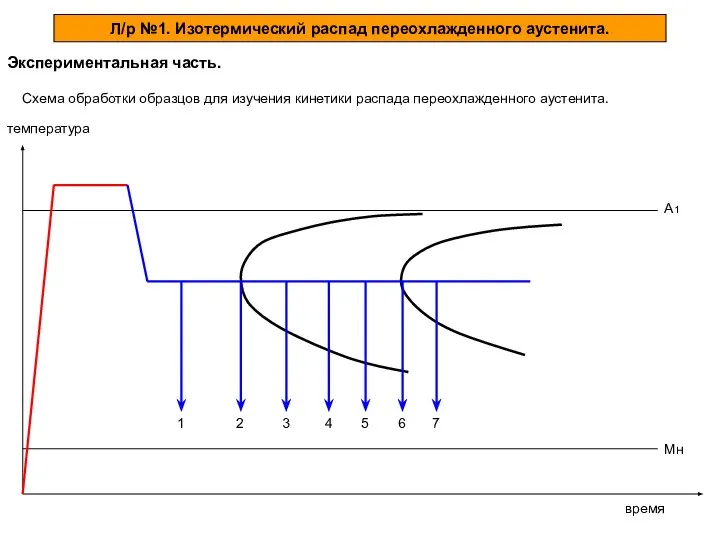 Изотермический распад переохлажденного аустенита. Экспериментальная часть
Изотермический распад переохлажденного аустенита. Экспериментальная часть Содержание варианта ЕГЭ
Содержание варианта ЕГЭ 11_.21
11_.21 Использование комплексно-ориентированных заданий на уроках
Использование комплексно-ориентированных заданий на уроках Окислительно-восстановительные реакции (ОВР)
Окислительно-восстановительные реакции (ОВР) Реакции окисления-восстановления в химическом анализе. (Лекция 7.2)
Реакции окисления-восстановления в химическом анализе. (Лекция 7.2) Алканы
Алканы Химия и автомобиль
Химия и автомобиль Общая характеристика элементов подгруппы углерода. Углерод – его строение и свойства
Общая характеристика элементов подгруппы углерода. Углерод – его строение и свойства Природный каучук
Природный каучук Классификация оксидов
Классификация оксидов Химические реакции
Химические реакции Образование и получение веществ. 6 класс
Образование и получение веществ. 6 класс Металлы
Металлы Закон сохранения массы веществ. Уравнения химических реакций.
Закон сохранения массы веществ. Уравнения химических реакций. Сравнительная характеристика стиральных порошков
Сравнительная характеристика стиральных порошков Валентность. Определение валентности по формулам
Валентность. Определение валентности по формулам Кроссворд. Плотность
Кроссворд. Плотность Алкены
Алкены Коррозия металлов
Коррозия металлов Вещества с атомной кристаллической решеткой
Вещества с атомной кристаллической решеткой Cкорость химических реакций
Cкорость химических реакций