Содержание
- 2. Коррозия – рыжая крыса, Грызет металлический лом. В Шефнер.
- 3. - называют самопроизвольное разрушение металлов и сплавов под влиянием окружающей среды Зачем нам нужно изучать этот
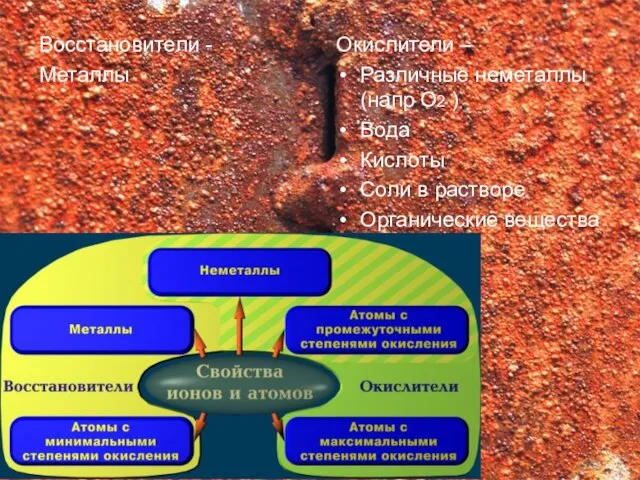
- 4. Восстановители - Металлы Окислители – Различные неметаллы(напр О2 ) Вода Кислоты Соли в растворе Органические вещества
- 5. Химическая Коррозия Электрохимическая коррозия С 170 -171 учебника виды коррозии
- 6. Компоненты окружающей среды окисляют непосредственно металл. Протекающие при химической коррозии окислительно - восстановительные реакции осуществляются путем
- 7. Коррозия протекающая в токопроводящей среде. Помимо химической реакции, в системе возникает электрический ток. Процесс электрохимической коррозии
- 8. 1 группа – щелочные металлы – наименьшая коррозийная стойкость.(побочная подгруппа – весьма стойкие металлы) 2 группа
- 9. 3 группа – Алюминий – образуется прочная оксидная пленка ( но она разрушается в растворах кислот
- 10. 5,6,7,8группы. – металлы побочных подгрупп обладают высокой способностью к пассивации, а следовательно, большой коррозионной стойкостью. Осмий,
- 12. Скачать презентацию







 Эмульсия. Основные типы эмульсий
Эмульсия. Основные типы эмульсий Квантовая химия
Квантовая химия Алкены Бутен
Алкены Бутен Металлы
Металлы Химический диктант по органической химии. 9 класс
Химический диктант по органической химии. 9 класс Химические реакции. Классификация
Химические реакции. Классификация Знакомство с химией
Знакомство с химией Применение каучука
Применение каучука Неорганический мозговой штурм
Неорганический мозговой штурм Практическая работа: Очистка загрязнённой поваренной соли
Практическая работа: Очистка загрязнённой поваренной соли Буферные системы
Буферные системы Cеминар 6 -Алканы-2
Cеминар 6 -Алканы-2 Химические реакции
Химические реакции Электроосмос. Практическое применение электроосмоса
Электроосмос. Практическое применение электроосмоса Магматические горные породы
Магматические горные породы 1_
1_ Физические и химические свойства металлов
Физические и химические свойства металлов Строение электронных оболочек атома
Строение электронных оболочек атома Железо
Железо Производные салициловой, пара-аминобензойной кислот, применяемые в медицине
Производные салициловой, пара-аминобензойной кислот, применяемые в медицине коррозия металлов
коррозия металлов Индикаторная бумага
Индикаторная бумага Тренажер - Валентность. 8 класс
Тренажер - Валентность. 8 класс Потенциометрический анализ, титрование
Потенциометрический анализ, титрование Алкины
Алкины Лучший тест для подготовки к ЕГЭ по химии
Лучший тест для подготовки к ЕГЭ по химии Тривиальные названия веществ, наиболее часто встречаемых в ЕГЭ
Тривиальные названия веществ, наиболее часто встречаемых в ЕГЭ Блок колонн на установке замедленного коксования производительностью 730000 тонн/год гудрона (поз.к-1, кх-1)
Блок колонн на установке замедленного коксования производительностью 730000 тонн/год гудрона (поз.к-1, кх-1)