Содержание
- 2. Неорганические полимеры Неорганические полимеры — полимеры, не содержащие в повторяющемся звене связей C-C, но способные содержать
- 3. Классификация полимеров 1. Гомоцепные полимеры Углерод и халькогены (пластическая модификация серы). 2. Гетероцепные полимеры Способны многие
- 4. Минеральное волокно асбест
- 5. Характеристика асбеста Асбест (греч. ἄσβεστος, — неразрушимый) — собирательное название группы тонковолокнистых минералов из класса силикатов.
- 6. Химический состав По химическому составу асбесты представляют собой водные силикаты магния, железа, отчасти кальция и натрия.
- 7. Безопасность Асбест практически инертен и не растворяется в жидких средах организма, но обладает заметным канцерогенным эффектом.
- 8. Применение асбеста Производства огнеупорных тканей (в том числе для пошива костюмов для пожарных). В строительстве (в
- 9. Роль неорганических полимеров в формировании литосферы
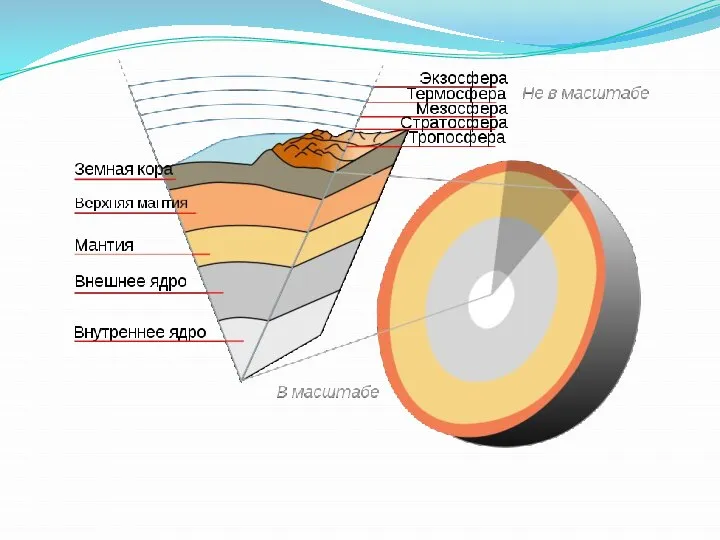
- 10. Литосфера Литосфера — твёрдая оболочка Земли. Состоит из земной коры и верхней части мантии, до астеносферы.
- 12. Химический состав Основными компонентами земной коры и поверхностного грунта Луны являются оксиды Si и Al и
- 13. Гранит Гранит - кислая магматическая интрузивная горная порода. Состоит из кварца, плагиоклаза, калиевого полевого шпата и
- 14. Базальт Минеральный состав. Основная масса сложена микролитами плагиоклазов, клинопироксена, магнетита или титаномагнетита, а также вулканическим стеклом.
- 15. Кварц (Оксид кремния(IV), кремнезем)
- 16. Формула: SiO2 Цвет: бесцветный, белый, фиолетовый, серый, жёлтый, коричневый Цвет черты: белая Блеск: стеклянный, в сплошных
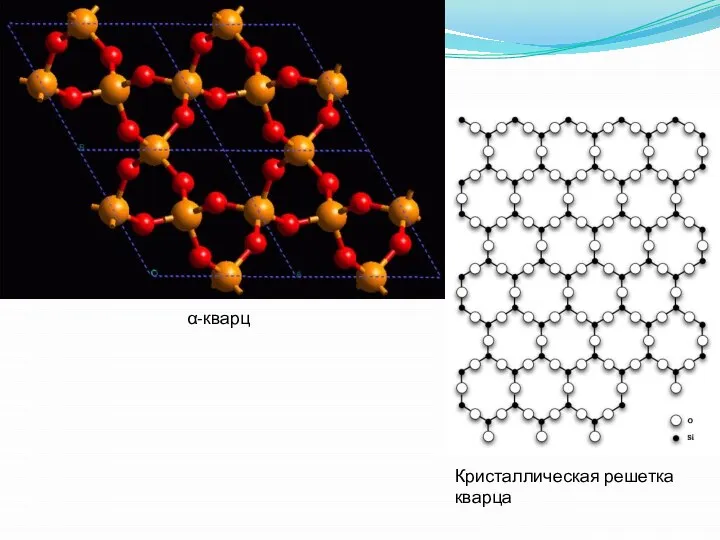
- 19. α-кварц Кристаллическая решетка кварца
- 20. Химические свойства
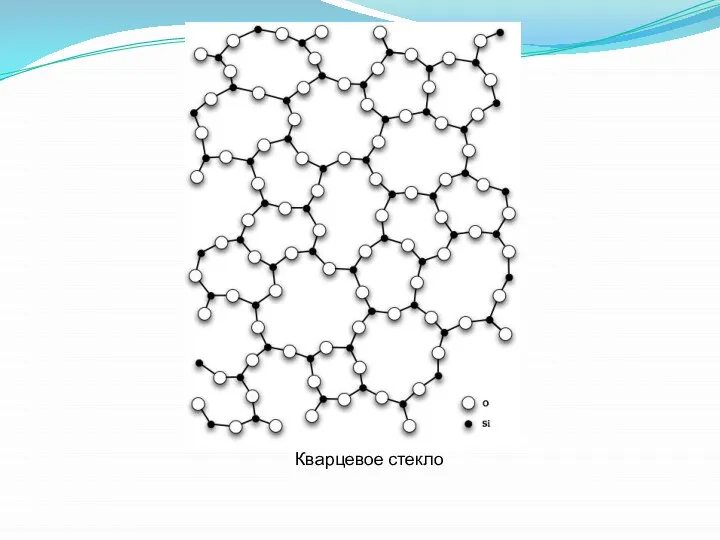
- 21. Кварцевое стекло
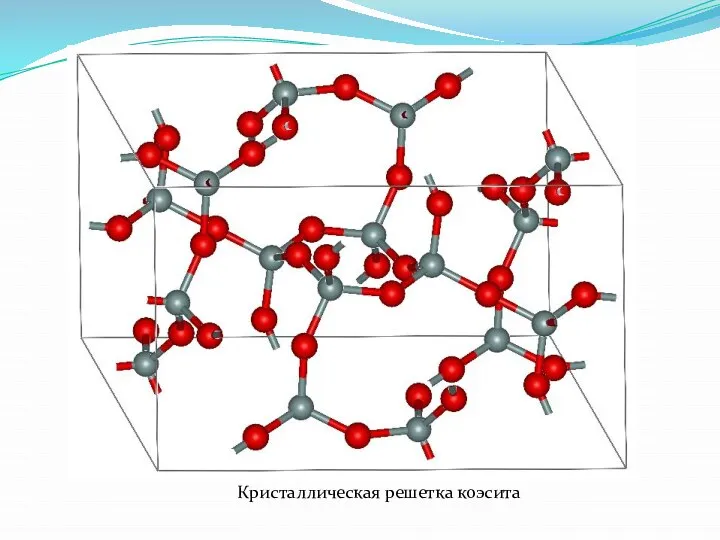
- 22. Кристаллическая решетка коэсита
- 23. Применение Кварц используется в оптических приборах, в генераторах ультразвука, в телефонной и радиоаппаратуре В больших количествах
- 24. Корунд (Al2O3 , глинозем)
- 25. Формула: Al2O3 Цвет: голубой, красный, жёлтый, коричневый, серый Цвет черты: белая Блеск: стеклянный Плотность: 3,9—4,1 г/см³
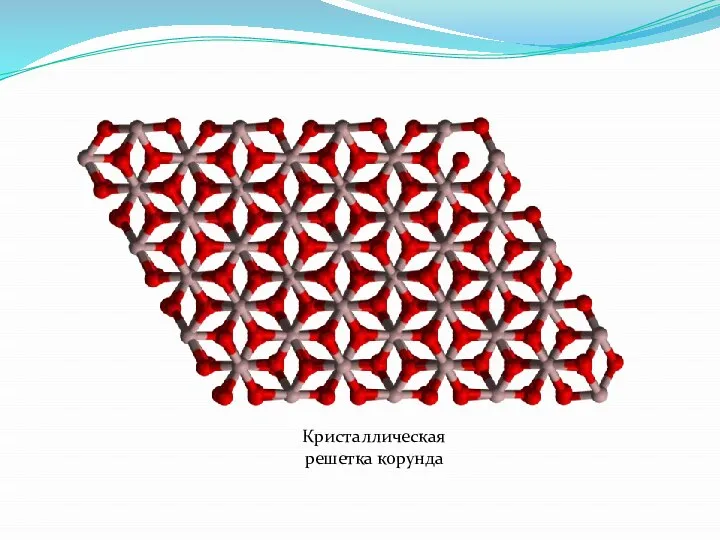
- 26. Кристаллическая решетка корунда
- 27. Применение Используют как абразивный материал Используется как огнеупорный материал Драгоценные камни
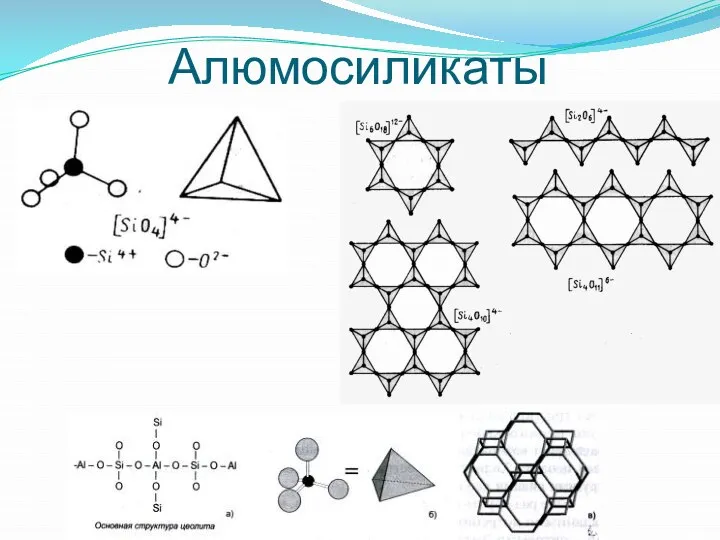
- 29. Алюмосиликаты
- 30. Алюмосиликаты Алюмосиликаты Слоистые (слюда) Каркасным (полевые шпаты, цеолиты) Кольцевые (кордиерит) Цепочечные (пироксены) Ленточные (амфиболы)
- 31. Теллур
- 32. Теллур цепочечного строения Кристаллы - гексагональные, атомы в них образуют спиральные цепи и связаны ковалентными связями
- 33. Применение теллура Производстве полупроводниковых материалов Производство резины Высокотемпературная сверхпроводимость
- 34. Селен
- 35. Селен цепочечного строения Черный Серый Красный
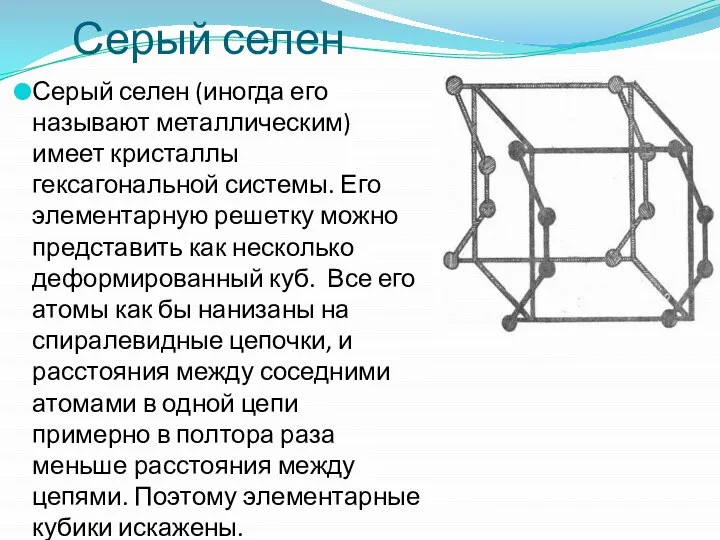
- 36. Серый селен Серый селен (иногда его называют металлическим) имеет кристаллы гексагональной системы. Его элементарную решетку можно
- 37. Применение серого селена Обычный серый селен обладает полупроводниковыми свойствами, это полупроводник p-типа, т.е. проводимость в нем
- 38. Красный селен Красный селен представляет собой менее устойчивую аморфную модификацию. Полимер цепного строения, но малоупорядоченной структуры.
- 39. Сера
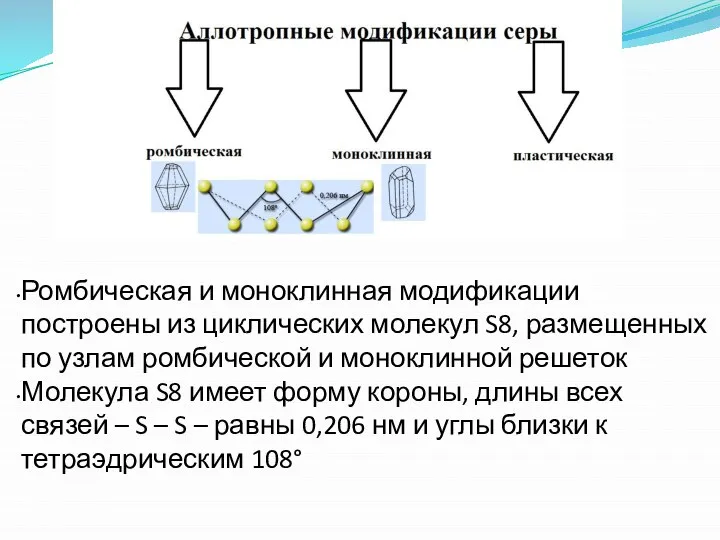
- 40. Ромбическая и моноклинная модификации построены из циклических молекул S8, размещенных по узлам ромбической и моноклинной решеток
- 41. Особенности строения Пластическая модификация серы образована спиральными цепями из атомов серы с левой и правой осями
- 42. Ромбическая сера Моноклинная сера Пластическая сера Расплав серы при медленном охлаждении При комнатной t° При добавлении
- 43. Получение пластической серы
- 44. Применение серы Получение серной кислоты; В бумажной промышленности; в сельском хозяйстве (для борьбы с болезнями растений,
- 45. Аллотропные модификации углерода
- 46. Сравнительная характеристика
- 48. Скачать презентацию





































 2.Химич. м-ды колич. ан-за
2.Химич. м-ды колич. ан-за Химия переходных элементов. Триада железа и металлы платиновой группы
Химия переходных элементов. Триада железа и металлы платиновой группы Бутадиен-стирольный каучук. 10 класс
Бутадиен-стирольный каучук. 10 класс Значение и применение спиртов
Значение и применение спиртов Теория валентных связей
Теория валентных связей Кислород. Применение и круговорот в природе. 8 класс
Кислород. Применение и круговорот в природе. 8 класс Сұрақтар
Сұрақтар Презентация по Химии "Анилин"
Презентация по Химии "Анилин" 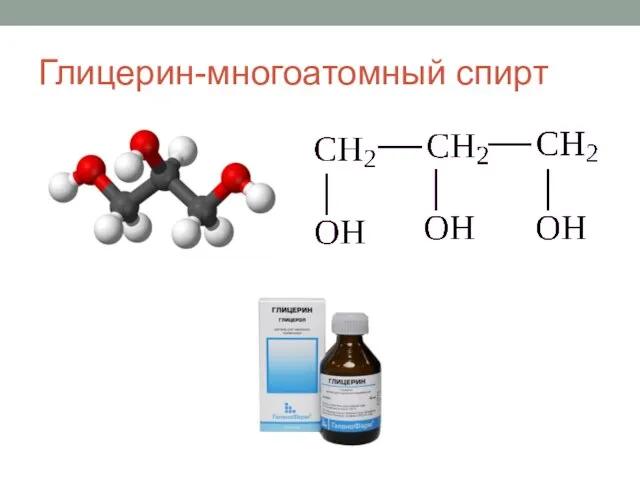 Жиры. Классификация жиров
Жиры. Классификация жиров Разработка математического описания расчета октанового числа бензинов каталитического риформинга с групповой кинетикой
Разработка математического описания расчета октанового числа бензинов каталитического риформинга с групповой кинетикой Сера
Сера Электролитическая диссоциация
Электролитическая диссоциация Структура периодической таблицы элементов
Структура периодической таблицы элементов d-элементы.Распространение в природе и основные материалы
d-элементы.Распространение в природе и основные материалы Альдегиды и кетоны. (Лекция 6.2)
Альдегиды и кетоны. (Лекция 6.2) Изменения, происходящие с веществами
Изменения, происходящие с веществами Элементы принадлежащие к VII группе периодической таблицы - галогены
Элементы принадлежащие к VII группе периодической таблицы - галогены Характеристика щелочных металлов (9 класс)
Характеристика щелочных металлов (9 класс) Аэрированный сшитый полимерный раствор (АСПР)
Аэрированный сшитый полимерный раствор (АСПР) Кислоты. Классификация. Номенклатура
Кислоты. Классификация. Номенклатура Виды нагрева и материалы резистивных нагревателей, их стойкость к температуре, ростовой атмосфере и расплаву
Виды нагрева и материалы резистивных нагревателей, их стойкость к температуре, ростовой атмосфере и расплаву Карбоновые кислоты
Карбоновые кислоты Термостабилизаторы. Доноры водорода
Термостабилизаторы. Доноры водорода Алмашу реакциясе
Алмашу реакциясе Алкадиены. Строение. Изомерия. Свойства
Алкадиены. Строение. Изомерия. Свойства Нахождение молекулярной формулы по данным о массовых долях элементов и относительной молекулярной массе (или молярной массе)
Нахождение молекулярной формулы по данным о массовых долях элементов и относительной молекулярной массе (или молярной массе) Свойства черных и цветных металлов
Свойства черных и цветных металлов Теория электролитической диссоциации
Теория электролитической диссоциации