Содержание
- 2. 1-Е ПОЛОЖЕНИЕ ТЭД. Все вещества по их способности проводить электрический ток в растворах делятся на электролиты
- 3. ВЕЩЕСТВА В РАСТВОРАХ Электролиты (водные растворы проводят эл.ток) Неэлектролиты (водные растворы не проводят эл. ток) Вещества
- 4. ЗАДАНИЯ К I-МУ ПОЛОЖЕНИЮ ТЭД Укажите вид связи и принадлежность данных веществ к электролитам и неэлектролитам:
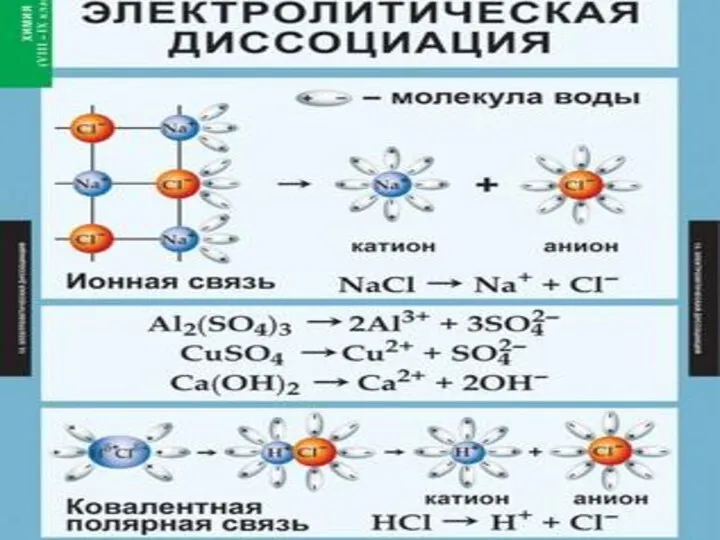
- 5. II-Е ПОЛОЖЕНИЕ ТЭД В РАСТВОРАХ ЭЛЕКТРОЛИТЫ ДИССОЦИИРУЮТ, Т.Е. РАСПАДАЮТСЯ НА ИОНЫ. Ионы – ЭТО ПОЛОЖИТЕЛЬНО ИЛИ
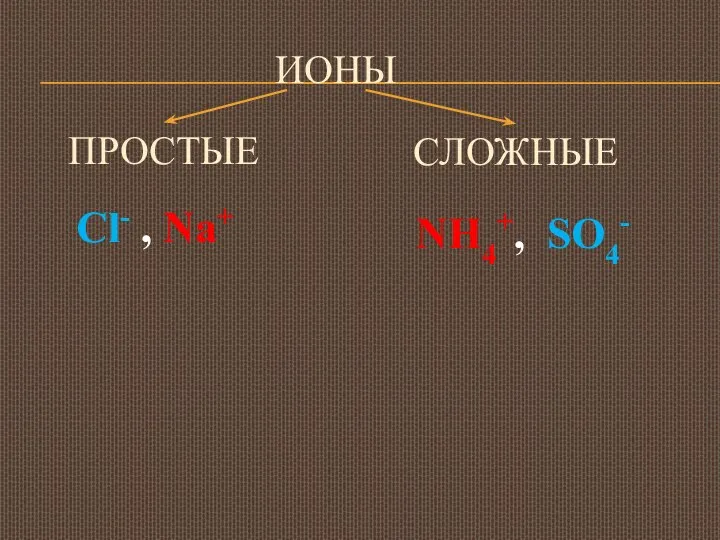
- 6. ИОНЫ ПРОСТЫЕ Сl- , Na+ СЛОЖНЫЕ NH4+, SO4-
- 7. III-Е ПОЛОЖЕНИЕ ТЭД ПРИЧИНОЙ ДИССОЦИАЦИИ ЭЛЕКТРОЛИТА ЯВЛЯЕТСЯ ЕГО ВЗАИМОДЕЙСТВИЕ С МОЛЕКУЛАМИ ВОДЫ (ГИДРАТАЦИЯ). Вещества с ковалентной
- 9. IV-Е ПОЛОЖЕНИЕ ТЭД Под действием электрического тока положительные ионы движутся к катоду и называются катионами, а
- 10. Типы ионов По заряду: положительные, или катионы: Катионы металлов ( Мn+ ) Катион водорода (H+) Катион
- 11. Упрощённо процесс диссоциации изображают с помощью уравнений диссоциации: NaCl = Na+ + Cl- HCl = H+
- 12. ЗАДАНИЯ КО II-МУ ПОЛОЖЕНИЮ ТЭД Назовите частицы: а) H, H2 , H+ ; б) Cl2 ,
- 13. V-Е ПОЛОЖЕНИЕ ТЭД Разные электролиты по-разному диссоциируют на ионы и поэтому делятся на: Сильные (соли, щелочи,
- 14. VI-Е ПОЛОЖЕНИЕ ТЭД Свойства растворов электролитов определяются свойствами тех ионов, которые они образуют при диссоциации. По
- 15. ОДНООСНОВНЫЕ КИСЛОТЫ МНОГООСНОВНЫЕ КИСЛОТЫ Диссоциируют в одну ступень HNO3 HNO3 = H+ + NO3- Диссоциируют в
- 16. 2. ОСНОВАНИЯ – ЭТО ЭЛЕКТРОЛИТЫ, КОТОРЫЕ ДИССОЦИИРУЮТ НА КАТИОНЫ МЕТАЛЛА И АНИОНЫ ГИДРОКСОГРУПП ОДНОКИСЛОТНЫЕ ОСНОВАНИЯ МНОГОКИСЛОТНЫЕ
- 17. 3. СОЛИ – ЭТО ЭЛЕКТРОЛИТЫ, КОТОРЫЕ ДИССОЦИИРУЮТ НА КАТИОНЫ МЕТАЛЛА И АНИОНЫ КИСЛОТНОГО ОСТАТКА Независимо от
- 18. ЗАДАНИЕ К 6-МУ ПОЛОЖЕНИЮ Напишите уравнения диссоциации следующих веществ: HCl, H3PO4, KOH
- 20. Скачать презентацию















 Производство серной кислоты
Производство серной кислоты Вода в природе. Состав, свойства и применение воды
Вода в природе. Состав, свойства и применение воды Бишофит - новый старый антигололедный реагент
Бишофит - новый старый антигололедный реагент Вода. Растворы
Вода. Растворы Закон сохранения массы и химические уравнения
Закон сохранения массы и химические уравнения Соли
Соли Нефть. Способы переработки нефти
Нефть. Способы переработки нефти Металлы побочных подгрупп
Металлы побочных подгрупп Модель химического образования на основе технологического подхода. Методическая система учителя химии
Модель химического образования на основе технологического подхода. Методическая система учителя химии Возможности окрашивания поверхности стекла путем высокотемпературной ионообменной обработки с выбранными реагентами
Возможности окрашивания поверхности стекла путем высокотемпературной ионообменной обработки с выбранными реагентами Химический элемент кислород
Химический элемент кислород Химическая география чудес природы
Химическая география чудес природы Материаловедение. Методы исследования в материаловедении (лекция 1)
Материаловедение. Методы исследования в материаловедении (лекция 1) Презентация по Химии "Схема получения моноизотопного кремния"
Презентация по Химии "Схема получения моноизотопного кремния"  Посвящение в химики
Посвящение в химики Наша стирка по-байкальски. Синтетические моющие средства (СМС¸ детергенты)
Наша стирка по-байкальски. Синтетические моющие средства (СМС¸ детергенты) Презентация на тему Неметаллы, особенности строения
Презентация на тему Неметаллы, особенности строения  Схема монооксигеназной цепи микросом
Схема монооксигеназной цепи микросом Общая характеристика оксидов
Общая характеристика оксидов Серная кислота
Серная кислота Основные понятия химии
Основные понятия химии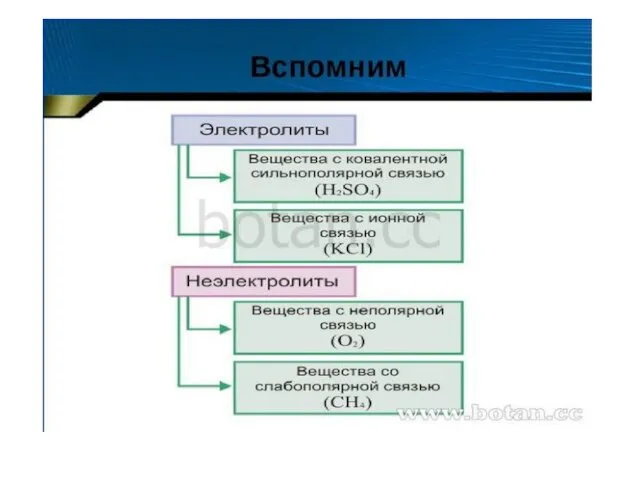 Диссоциация веществ
Диссоциация веществ Химическая связь и ее типы
Химическая связь и ее типы Соли. Химические свойства
Соли. Химические свойства Соль. Добыча соли
Соль. Добыча соли Металлы. Атомы металлов
Металлы. Атомы металлов Природные источники углеводорода
Природные источники углеводорода Кислоты. Кислоты, вокруг нас
Кислоты. Кислоты, вокруг нас