Слайд 2Спирты
Спирты — органические соединения, содержащие одну или более гидроксильных групп (гидроксил, −OH), непосредственно связанных с насыщенным (находящимся
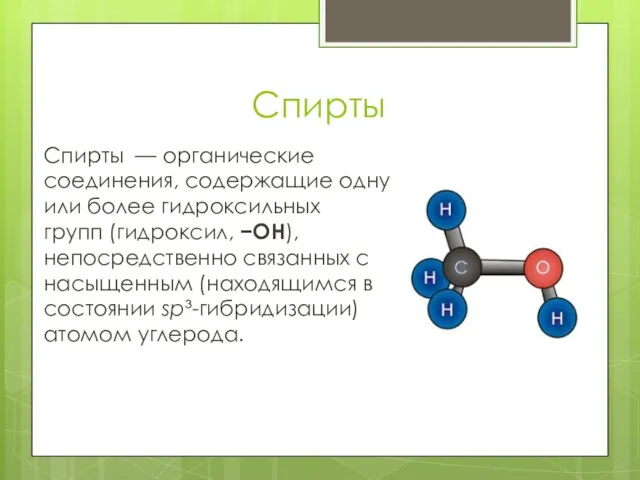
в состоянии sp³-гибридизации) атомом углерода.
Слайд 3Классификация спиртов
По числу гидроксильных групп:
Одноатомные
двухатомные (гликоли)
трёхатомные

Слайд 4По характеру углеводородного радикала:
предельные спирты
непредельные (имеют кратные связи)спирты
ароматические спирты

Слайд 5Номенклатура
По номенклатуре ИЮПАК названия простых спиртов образуются от названий соответствующих алканов с добавлением суффикса «-ол», положение которого

указывается арабской цифрой.
Слайд 6Изомерия
Начиная с 3 гомологического ряда появляется изомерия положения функциональной группы (пропанол-1 и

пропанол-2), а ч 4 – изомерия углеродного скелета.
Межклассовая с простыми эфирами
Слайд 7Физические свойства
Молекулы спиртов, подобно молекуле воды, имеют угловое строение. Угол R−O−H в молекуле метанола равен
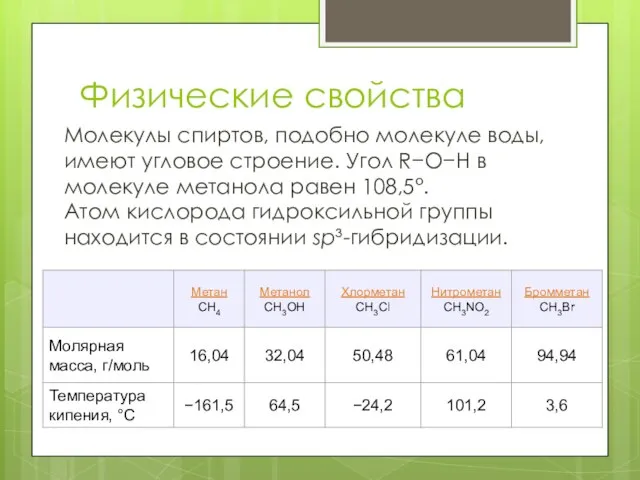
108,5°. Атом кислорода гидроксильной группы находится в состоянии sp³-гибридизации.
Слайд 8Химические свойства
Реакции, протекающие по связи О–Н.
При взаимодействии с активными металлами (Na, K,

Mg, Al) спирты проявляют свойства слабых кислот и образуют соли, называемые алкоголятами или алкоксидами:
2CH3OH + 2Na → 2CH3OK + H2
Алкоголяты химически не стабильны и при действии воды гидролизуются с образованием спирта и гидроксида металла:
C2H5OК + H2O → C2H5OH + КOH
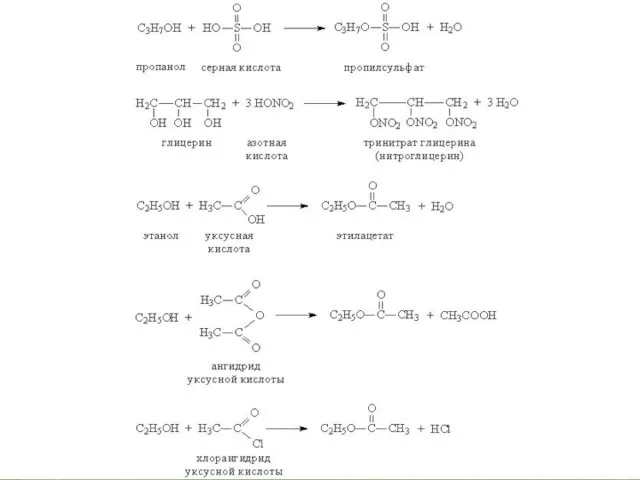
Слайд 9При взаимодействии с минеральными или органическими кислотами спирты образуют сложные эфиры –

соединения, содержащие фрагмент R–O–A (А – остаток кислоты). Образование сложных эфиров происходит и при взаимодействии спиртов с ангидридами и хлорангидридами карбоновых кислот
Слайд 11При действии окислителей (К2Cr2O7, KMnO4) первичные спирты образуют альдегиды, а вторичные – кетоны.

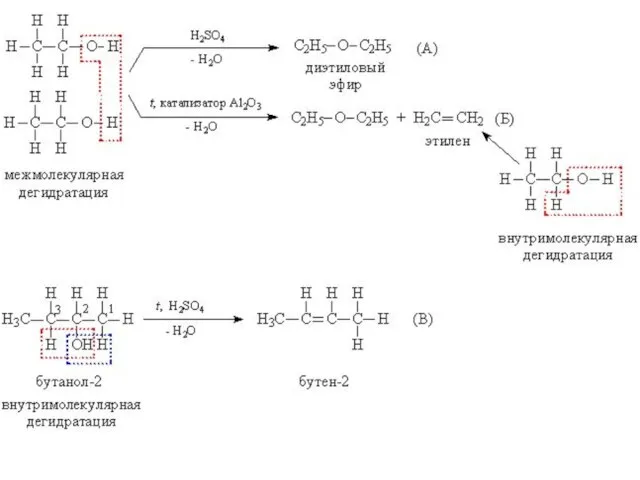
Слайд 12В присутствии катализаторов или сильных минеральных кислот происходит дегидратация спиртов (отщепление воды),

при этом реакция может идти в двух направлениях:
а) межмолекулярная дегидратация с участием двух молекул спирта, при этом связи С–О у одной из молекул разрываются, в результате образуются простые эфиры – соединения, содержащие фрагмент R–О–R.
б) при внутримолекулярной дегидратации образуются алкены - углеводороды с двойной связью. Часто оба процесса – образование простого эфира и алкена – протекают параллельно.
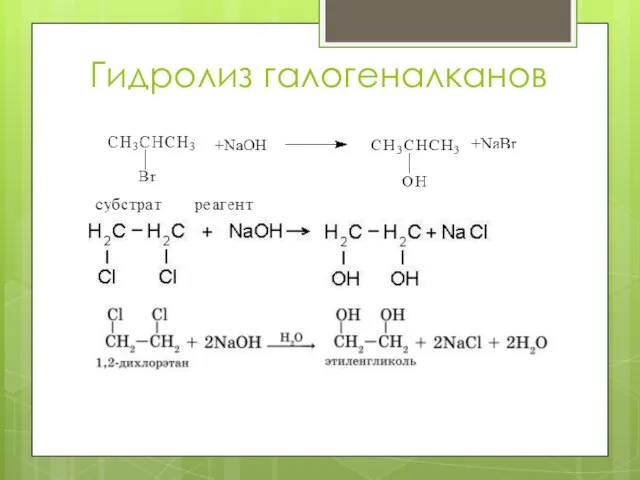
Слайд 14Взаимодействие спиртов с галогеноводородами

Слайд 15Получение спиртов
Гидратация алкенов (правило Марковникова):
Алкены присоединяют воду в кислой среде по механизму электрофильного

присоединения, по правилу Марковникова.
Слайд 17Гидрирование альдегидов и кетонов
(при воздействии температуры и платинового катализатора)















 Коррозия металлов. Экзаменационные вопросы
Коррозия металлов. Экзаменационные вопросы Chemsheets AS 1009 (Electron arrangement)
Chemsheets AS 1009 (Electron arrangement) Обобщение по теме Теория химического строения органических веществ
Обобщение по теме Теория химического строения органических веществ Классификация процессов коррозии
Классификация процессов коррозии Обобщение и систематизация знаний по теме Углеводороды
Обобщение и систематизация знаний по теме Углеводороды Презентация на тему Галогены и здоровье человека
Презентация на тему Галогены и здоровье человека  Производство аммиака
Производство аммиака Хімія у вирішенні промислової проблеми
Хімія у вирішенні промислової проблеми Презентация на тему Металлы и неметаллы
Презентация на тему Металлы и неметаллы  Презентация на тему Мыло. Синтетические моющие средства
Презентация на тему Мыло. Синтетические моющие средства  Презентация на тему Палладий
Презентация на тему Палладий  Классификация НПВС (по химической структуре активности)
Классификация НПВС (по химической структуре активности) Растворы. Процесс растворения (1)
Растворы. Процесс растворения (1) Формирование универсальных учебных действий
Формирование универсальных учебных действий Строение атома
Строение атома ЛК 2_окислительно-восстановительные процессы
ЛК 2_окислительно-восстановительные процессы Презентация на тему Основные законы химии
Презентация на тему Основные законы химии  Предельные углеводороды Алканы
Предельные углеводороды Алканы Железо в продуктах питания
Железо в продуктах питания Презентация на тему: Чистые вещества и смеси
Презентация на тему: Чистые вещества и смеси Оксиды азота
Оксиды азота Органические вещества
Органические вещества Презентация на тему Альдегиды (10 класс)
Презентация на тему Альдегиды (10 класс)  Получение формальдегида методом дегидрирования метанола
Получение формальдегида методом дегидрирования метанола Окислительновосстановительные индикаторы. Задача 12 Команда: Мастера Беспорядка
Окислительновосстановительные индикаторы. Задача 12 Команда: Мастера Беспорядка Реакции этерификации
Реакции этерификации Проточные реакторы непрерывного действия. (Лекция 5)
Проточные реакторы непрерывного действия. (Лекция 5) Разминка
Разминка