Содержание
- 2. Открытие Fe Знакомство же с железом относится к более позднему времени. Получать его некоторые народы научились
- 3. Строение атома Схема строения атома: +26 ) ) ) ) 2e 8e 14e 2e Электронная формула:
- 4. Получение В лабораторных условиях железо можно получить из его соединений следующими способами: восстановление железа из оксида
- 5. Чистое железо — серебристо-белый металл, быстро тускнеющий (ржавеющий) на влажном воздухе или в воде, содержащей кислород.
- 6. Химические свойства
- 7. Применение Применение железа в строительстве Применение железа строительной отраслью в наши дни нельзя переоценить, ведь металлоконструкции
- 9. Скачать презентацию
Слайд 2 Открытие Fe
Знакомство же с железом относится к более позднему времени. Получать
Открытие Fe
Знакомство же с железом относится к более позднему времени. Получать

его некоторые народы научились раньше, а некоторые — значительно позже. Дело в том, что самородное железо в природе почти не встречается. Предполагается, что первое железо, которое попало в человеческие руки, было метеоритного происхождения. Первые упоминания о железе встречаются около 5 тысяч лет назад, тогда оно ценилось дороже самородного золота, которое служило оправой для изделий из железа. Согласно историческим фактам племена, проживавшие на территории современной Армении, уже в начале третьего тысячелетия до нашей эры умели получать железо. В Египте и Древней Греции железо получали во втором, а в Китае — в середине 1-го тысячелетия до н. э.
Слайд 3 Строение атома
Схема строения атома:
+26 ) ) ) )
2e 8e 14e
Строение атома
Схема строения атома:
+26 ) ) ) )
2e 8e 14e

2e
Электронная формула: 1s22s22p63s23p63d64s2
Металл средней активности, восстановитель:
Fe0-2e-→Fe+2, окисляется восстановитель
Fe0-3e-→Fe+3, окисляется восстановитель
Основные степени окисления: +2, +3
Электронная формула: 1s22s22p63s23p63d64s2
Металл средней активности, восстановитель:
Fe0-2e-→Fe+2, окисляется восстановитель
Fe0-3e-→Fe+3, окисляется восстановитель
Основные степени окисления: +2, +3
Слайд 4Получение
В лабораторных условиях железо можно получить из его соединений следующими способами:
восстановление железа из оксида Fe2O3 водородом при
Получение
В лабораторных условиях железо можно получить из его соединений следующими способами:
восстановление железа из оксида Fe2O3 водородом при

нагревании:
Fe2O3+3H2−→−t2Fe+3H2O↑⏐⏐;
восстановление железа из его оксидов алюминием при нагревании:
Fe2O3+2Al−→−t2Fe+Al2O3;
электролиз водных растворов солей железа(II).
В промышленных условиях железо получают из руд, массовая доля железа в которых — не менее 16 %.
Чистое железо получают восстановлением из оксидов (железо пирофорное), электролизом водных растворов его солей (железо электролитическое), разложением пентакарбонила железа Fe(CO)5 при нагревании до t 250°С. Особо чистое железо (99,99%) получают с помощью зонной плавки. Технически чистое железо (около 0,16% примесей углерода, кремния, марганца, фосфора, серы и др.) выплавляют, окисляя компоненты чугуна в мартеновских сталеплавильных печах и в кислородных конверторах. Сварочное или кирпичное железо получают, окисляя примеси малоуглеродистой стали железным шлаком или путём восстановления руд твёрдым углеродом. Основную массу железа выплавляют в виде сталей (до 2% углерода) или чугунов (свыше 2% углерода).
Fe2O3+3H2−→−t2Fe+3H2O↑⏐⏐;
восстановление железа из его оксидов алюминием при нагревании:
Fe2O3+2Al−→−t2Fe+Al2O3;
электролиз водных растворов солей железа(II).
В промышленных условиях железо получают из руд, массовая доля железа в которых — не менее 16 %.
Чистое железо получают восстановлением из оксидов (железо пирофорное), электролизом водных растворов его солей (железо электролитическое), разложением пентакарбонила железа Fe(CO)5 при нагревании до t 250°С. Особо чистое железо (99,99%) получают с помощью зонной плавки. Технически чистое железо (около 0,16% примесей углерода, кремния, марганца, фосфора, серы и др.) выплавляют, окисляя компоненты чугуна в мартеновских сталеплавильных печах и в кислородных конверторах. Сварочное или кирпичное железо получают, окисляя примеси малоуглеродистой стали железным шлаком или путём восстановления руд твёрдым углеродом. Основную массу железа выплавляют в виде сталей (до 2% углерода) или чугунов (свыше 2% углерода).
Слайд 5Чистое железо — серебристо-белый металл, быстро тускнеющий (ржавеющий) на влажном воздухе или
Чистое железо — серебристо-белый металл, быстро тускнеющий (ржавеющий) на влажном воздухе или

в воде, содержащей кислород. Железо пластично, легко подвергается ковке и прокатке, t плавления 1539°С а t кипения 2862°С. Обладает сильными магнитными свойствами (ферромагнетик), хорошей тепло- и электропроводностью.
Ферромагнетик —такое вещество, которое при t ниже точки Кюри, способно обладать намагниченностью в отсутствие внешнего магнитного роля.
Температура Кюри – t , при которой его феррменитные свойства исчезают.
Ферромагнетик —такое вещество, которое при t ниже точки Кюри, способно обладать намагниченностью в отсутствие внешнего магнитного роля.
Температура Кюри – t , при которой его феррменитные свойства исчезают.
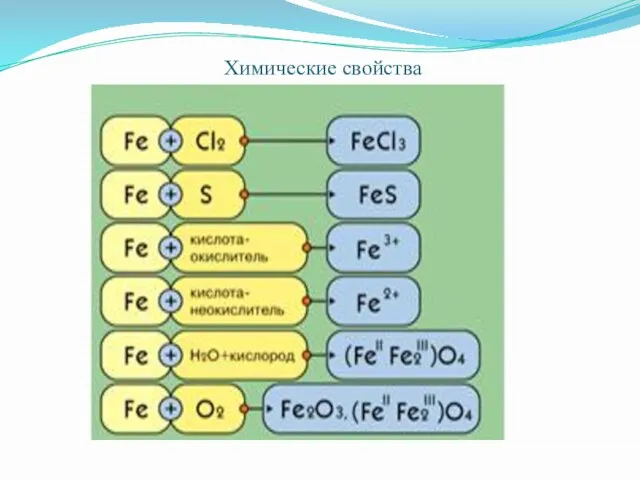
Слайд 6 Химические свойства
Химические свойства
Слайд 7Применение
Применение железа в строительстве
Применение железа строительной отраслью в наши дни нельзя переоценить,
Применение
Применение железа в строительстве
Применение железа строительной отраслью в наши дни нельзя переоценить,

ведь металлоконструкции являются основой абсолютно любого современного строения. В этой сфере Fe используется в составе обычных сталей, литейного чугуна и сварочного железа. Данный элемент находится везде, начиная с ответственных конструкций и заканчивая анкерными болтами и гвоздями.
Применение железа в медицине
Известно, что в каждом взрослом человеке содержится до 4 грамм железа. Этот элемент крайне важен для функционирования организма, в частности, для здоровья кровеносной системы (гемоглобин в эритроцитах). Существует множество лекарственных препаратов на основе железа, которые позволяют повышать содержание Fe во избежание развития железодефицитной анемии.
Использование железа в промышленности
Использование железа и его сплавов – чугуна и стали – это основа приборостроения и изготовления прочей техники. Благодаря цианидам и оксидам Fe функционирует лакокрасочная промышленность, сульфаты железа применяются при водоподготовке. Тяжелая промышленность и вовсе немыслима без использования сплавов на основе Fe+C. Словом, Железо – это незаменимый, но вместе с тем доступный и относительно недорогой металл, который в составе сплавов имеет практически неограниченную сферу применения.
Применение железа в медицине
Известно, что в каждом взрослом человеке содержится до 4 грамм железа. Этот элемент крайне важен для функционирования организма, в частности, для здоровья кровеносной системы (гемоглобин в эритроцитах). Существует множество лекарственных препаратов на основе железа, которые позволяют повышать содержание Fe во избежание развития железодефицитной анемии.
Использование железа в промышленности
Использование железа и его сплавов – чугуна и стали – это основа приборостроения и изготовления прочей техники. Благодаря цианидам и оксидам Fe функционирует лакокрасочная промышленность, сульфаты железа применяются при водоподготовке. Тяжелая промышленность и вовсе немыслима без использования сплавов на основе Fe+C. Словом, Железо – это незаменимый, но вместе с тем доступный и относительно недорогой металл, который в составе сплавов имеет практически неограниченную сферу применения.
Следующая -
Летописи и другие исторические сочинения Свойства кислорода. Оксиды
Свойства кислорода. Оксиды Задача №8: Не тормози. Команда: Карбораны
Задача №8: Не тормози. Команда: Карбораны Натуральный каучук
Натуральный каучук Электростанция в кармане
Электростанция в кармане Железо. Физические свойства
Железо. Физические свойства Общая характеристика неметаллов подгруппы кислород
Общая характеристика неметаллов подгруппы кислород Полимеры
Полимеры Смог як хімічне явище
Смог як хімічне явище Презентация на тему Классы неорганических веществ
Презентация на тему Классы неорганических веществ  Массовая доля элемента в веществе
Массовая доля элемента в веществе Химия и производство
Химия и производство Стеклообразование, структура и свойства стекол системы Na2O – B2O3 – SiO2 на основе комплексного борсодержащего сырья
Стеклообразование, структура и свойства стекол системы Na2O – B2O3 – SiO2 на основе комплексного борсодержащего сырья Использование информационноко-ммуникационных технологий по формированию УУД на уроках химии
Использование информационноко-ммуникационных технологий по формированию УУД на уроках химии Алкины. Ацетилен
Алкины. Ацетилен Оксиды
Оксиды Непредельные углеводороды
Непредельные углеводороды Наркотики и прекурсоры
Наркотики и прекурсоры Повторение классов соединений. Составление формул по названиям
Повторение классов соединений. Составление формул по названиям Основные классы неорганических соединений
Основные классы неорганических соединений Презентация на тему Степень окисления
Презентация на тему Степень окисления  Кислоты основания и соли как электролиты
Кислоты основания и соли как электролиты 14257fc50bc406ef33f49ad14aa3f48b
14257fc50bc406ef33f49ad14aa3f48b Химия и производство
Химия и производство Реакции разложения
Реакции разложения Химическая кибернетика
Химическая кибернетика Титриметрический анализ. Основные понятия
Титриметрический анализ. Основные понятия Метод окислительно - восстановительного титрования
Метод окислительно - восстановительного титрования Химия на войне
Химия на войне