Содержание
- 2. 1. Фармаконадзор 2. Необходимость фармаконадзора 3. Исторические данные 4. Современная система фармаконадзора в мире 5. Цель
- 3. Фармаконадзор вид деятельности по мониторингу эффективности и безопасности лекарственных препаратов, направленный на выявление, оценку и предотвращение
- 4. Необходимость системы фармаконадзора 1) Клинические исследования проводятся в строго контролируемых условиях в течение относительно короткого промежутка
- 5. Исторические данные Стимулом к формированию системы фармаконадзора стала «талидомидовая трагедия»: 1 октября 1957 г. немецкая фирма
- 6. Талидомидовая трагедия
- 7. Талидомидовая трагедия В США, несмотря на давление со стороны фармкомпаний, Фрэнсис О. Келси, первая женщина-глава FDA,
- 8. Проблемы обращения лекарственных препаратов. Актуальность фармаконадзора Современный уровень проблемы по безопасности применения лекарственных препаратов в странах
- 9. Цель фармаконадзора Лекарственное средство считается безопасным для применения, если польза от его применения превышает риск. Эрвэ
- 10. Общая схема системы фармаконадзора в России
- 11. Средства фармаконадзора 1. Средства получения данных по безопасности фармаконадзора: 1.1 Сообщения от потребителей / пациентов/ медицинских
- 12. Извещение о нежелательных реакциях и отсутствии терапевтического действия
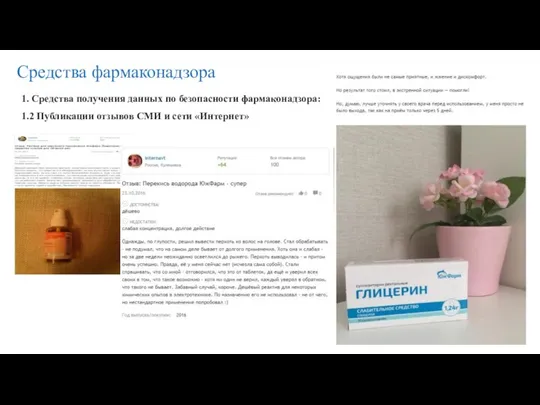
- 13. Средства фармаконадзора 1. Средства получения данных по безопасности фармаконадзора: 1.2 Публикации отзывов СМИ и сети «Интернет»
- 14. Средства фармаконадзора 1. Средства получения данных по безопасности фармаконадзора: 1.3 Публикации литературных данных: медицинские литературные обзоры,
- 15. Средства фармаконадзора 1. Средства получения данных по безопасности фармаконадзора: 1.4 Данные регуляторных органов
- 16. Средства фармаконадзора 1. Средства получения данных по безопасности фармаконадзора: 1.4 Претензии / вопросы и предложения от
- 17. Средства фармаконадзора 2. Выявление рисков / оценка риска / оценка соотношения «польза – риск»
- 18. Средства фармаконадзора 3. Минимизация выявленного риска / оценка соотношения «польза – риск» Примеры мер минимизация риска:
- 19. Средства фармаконадзора Например, внесение изменений в инструкцию по медицинскому применению как мера минимизации выявленного риска действующего
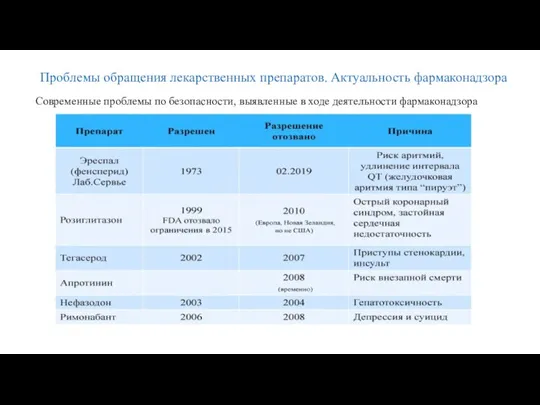
- 20. Современные проблемы по безопасности, выявленные в ходе деятельности фармаконадзора Проблемы обращения лекарственных препаратов. Актуальность фармаконадзора
- 21. Заключение описания деятельности фармаконадзора
- 22. Информирование о нежелательных реакциях Для предоставления данных по безопасности лекарственных средств в регуляторные органы, необходим заполнить
- 23. Извещение о нежелательных реакциях и отсутствии терапевтического действия
- 24. Ответственность Уголовный кодекс РФ Статья 237. Сокрытие информации об обстоятельствах, создающих опасность для жизни или здоровья
- 25. Ответственность КоАП Статья 19.7.8. Непредставление сведений или представление заведомо недостоверных сведений в федеральный орган исполнительной власти,
- 26. Ответственность Уголовный кодекс РФ Статья 238. Производство, хранение, перевозка либо сбыт товаров и продукции, выполнение работ
- 28. Скачать презентацию























 Аллергические и аутоиммунные заболевания в терапии
Аллергические и аутоиммунные заболевания в терапии 20141015_biokhimicheskie_endemii
20141015_biokhimicheskie_endemii Острый и хронический гастрит
Острый и хронический гастрит Осложнения сахарного диабета. Часть 3
Осложнения сахарного диабета. Часть 3 Оказание первой помощи при несчастных случаях на производстве
Оказание первой помощи при несчастных случаях на производстве Мочевыделительная система
Мочевыделительная система Тема 8-9_Первая помощь при неотложных состояниях1
Тема 8-9_Первая помощь при неотложных состояниях1 Вколоченный вывих зуба: определение, клиника, диагностика, лечение
Вколоченный вывих зуба: определение, клиника, диагностика, лечение Паразиты человека
Паразиты человека Физиология дыхания
Физиология дыхания Оказание услуг общего ухода и помощи при осуществлении повседневной деятельности. Лекция 2
Оказание услуг общего ухода и помощи при осуществлении повседневной деятельности. Лекция 2 Сотрясение головного мозга. Симптомы
Сотрясение головного мозга. Симптомы ВИЧ-инфекция у беременных
ВИЧ-инфекция у беременных Роды через влагалище, после предыдущего кесарева сечения
Роды через влагалище, после предыдущего кесарева сечения Аритмii
Аритмii Операции, подготавливающие родовые пути
Операции, подготавливающие родовые пути Наблюдение и уход за пациентами с инсультом
Наблюдение и уход за пациентами с инсультом Ларингіт у дітей
Ларингіт у дітей Воспаление. Классификация воспаления
Воспаление. Классификация воспаления Дистанционный познавательный проект Тайны Гиппократа
Дистанционный познавательный проект Тайны Гиппократа Stop, туберкулёз!
Stop, туберкулёз! Экзотические виды массажа
Экзотические виды массажа Инспекция зданий
Инспекция зданий Стресс-ЭКГ Велоэргометрия и тредмил-тест
Стресс-ЭКГ Велоэргометрия и тредмил-тест Злокачественные заболевания пищевода
Злокачественные заболевания пищевода Балалардағы семіру, жіктеу, қауіп факторлары. Клиника, диагноз, емдеу
Балалардағы семіру, жіктеу, қауіп факторлары. Клиника, диагноз, емдеу Гиподинамия
Гиподинамия Пузырек
Пузырек