Содержание
- 2. ЦЕЛЬ И ЗАДАЧИ Цель: построить модель машинного обучения на основе алгоритма “случайных лесов” (random forest), которая
- 3. АКТУАЛЬНОСТЬ Сердечно-сосудистые заболевания являются основной причиной смерти и инвалидизации во всем мире. Поиск новых способов лечения
- 4. МАТЕРИАЛЫ И МЕТОДЫ Машинное обучение (machine learning, ML) – совокупность методов искусственного интеллекта, позволяющих строить алгоритмы
- 5. Скрипты для обработки данных и построения модели были написаны на языке программирования Python. Для 1D представления
- 6. Для отбора ингибиторов ренина использовалась база данных ChEMBL. Всего было найдено 5154 лиганда. Для дальнейшей работы
- 7. Фингерпринты – представление молекул в виде битовой строки, где каждый бит соответствует наличию (1) либо отсутствию
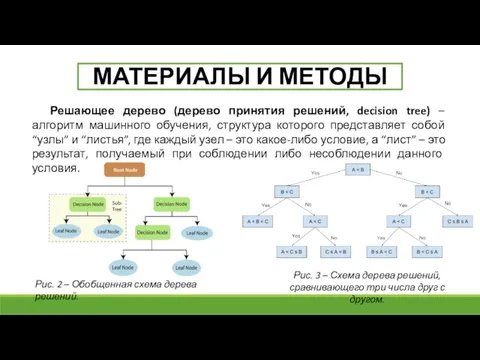
- 8. Решающее дерево (дерево принятия решений, decision tree) – алгоритм машинного обучения, структура которого представляет собой “узлы”
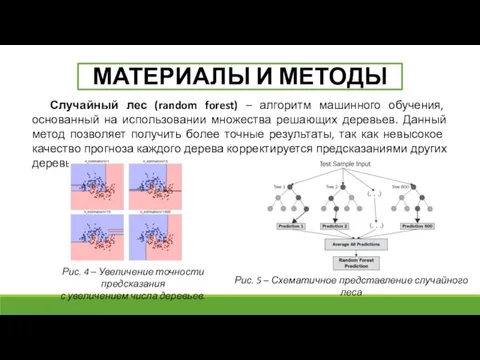
- 9. Случайный лес (random forest) – алгоритм машинного обучения, основанный на использовании множества решающих деревьев. Данный метод
- 10. МАТЕРИАЛЫ И МЕТОДЫ В качестве меры активности молекул использовалась IC50. Для удобства анализа данной меры активности
- 11. РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ С помощью метода RandomForestClassifier была построена QSAR модель “случайных лесов”. Обучение модели
- 12. РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ Метрики качества модели составили: Точность предсказания на тренировочных данных: 0,9472; Точность предсказания
- 13. РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ Конфузионная матрица (confusion matrix) – таблица, представляющая результаты предсказания в сравнении с
- 14. РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ По метрикам качества модели можно сделать вывод, что данная модель находит практически
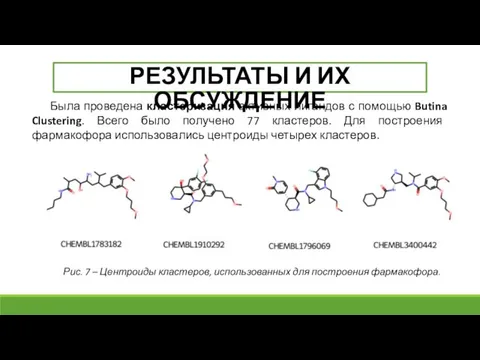
- 15. РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ Была проведена кластеризация активных лигандов с помощью Butina Clustering. Всего было получено
- 16. РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ Построение фармакофора проводилось с помощью алгоритма MAPex. Полученный фармакофор имеет 4 фармакофорных
- 17. РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ По данному фармакофору был проведен поиск в базе данных ZINCPharmer, были сохранены
- 18. РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ 1811 соединений, которые удовлетворяли критериям Липински были проверены по фильтру PAINS (Pan-assay
- 19. Для оставшихся 1245 соединений были получены их фингерпринты. С использованием QSAR модели, которая была построена ранее
- 21. Скачать презентацию















 Расти и развиваться здоровыми. Почему мы иногда болеем
Расти и развиваться здоровыми. Почему мы иногда болеем Состояние острой интоксикации ПАВ. Синдром отмены ПАВ
Состояние острой интоксикации ПАВ. Синдром отмены ПАВ Немедикаментозные методы коррекции эмоциональных нарушений
Немедикаментозные методы коррекции эмоциональных нарушений Антиагрегантная терапия в лечении хронических цереброваскулярных нарушений
Антиагрегантная терапия в лечении хронических цереброваскулярных нарушений Гидролазы (13 подклассов)
Гидролазы (13 подклассов) В.П. Демихов - основоположник мировой трансплантологии
В.П. Демихов - основоположник мировой трансплантологии Холера. История
Холера. История Блокады сердца
Блокады сердца Рецепт
Рецепт Нәтижелер мен талқылаулар, қорытынды
Нәтижелер мен талқылаулар, қорытынды Антикоагулянты 2022 МИД
Антикоагулянты 2022 МИД Гиперосмолярная кома
Гиперосмолярная кома Вскармливание детей грудного возраста
Вскармливание детей грудного возраста Нанохімія та нанотехнології в медицині. Токсичність нанооб'єктів
Нанохімія та нанотехнології в медицині. Токсичність нанооб'єктів Анатомо-фізіологічні особливості ендокринної системи у дітей та семіотика уражень
Анатомо-фізіологічні особливості ендокринної системи у дітей та семіотика уражень Массаж для новорожденных
Массаж для новорожденных Вспомогательные репродуктивные технологии. Нормативно-правовое регулирование
Вспомогательные репродуктивные технологии. Нормативно-правовое регулирование Сидячие ванночки
Сидячие ванночки Ангиогенез и его роль в развитии опухоли
Ангиогенез и его роль в развитии опухоли Воспалительные процессы в сердце
Воспалительные процессы в сердце Жүйке талшықтарының физиологиялық қасиеттері. Парабиоз
Жүйке талшықтарының физиологиялық қасиеттері. Парабиоз Добровольное медицинское страхование в РФ
Добровольное медицинское страхование в РФ Моя мама - фармацевт
Моя мама - фармацевт Artificial heart
Artificial heart Эпизоотии и эпифитотии
Эпизоотии и эпифитотии Перитонит. Классификация
Перитонит. Классификация Хроническая болезнь почек
Хроническая болезнь почек Фотодерматоз
Фотодерматоз