Содержание
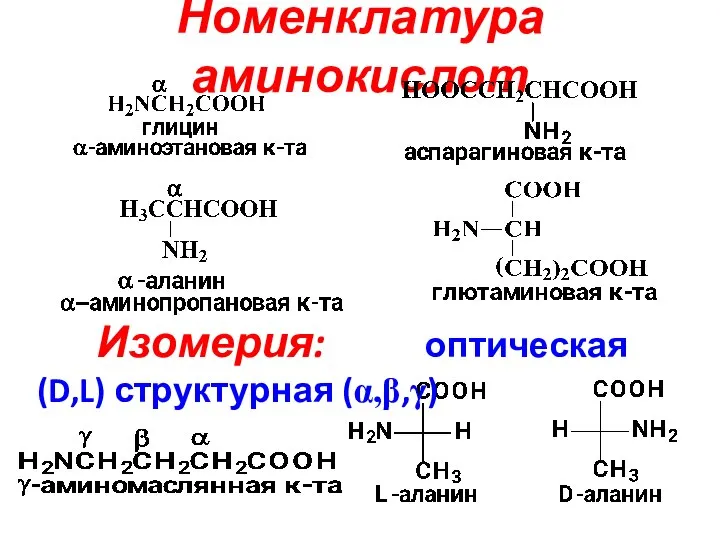
- 2. Номенклатура аминокислот Изомерия: оптическая (D,L) структурная (α,β,γ)
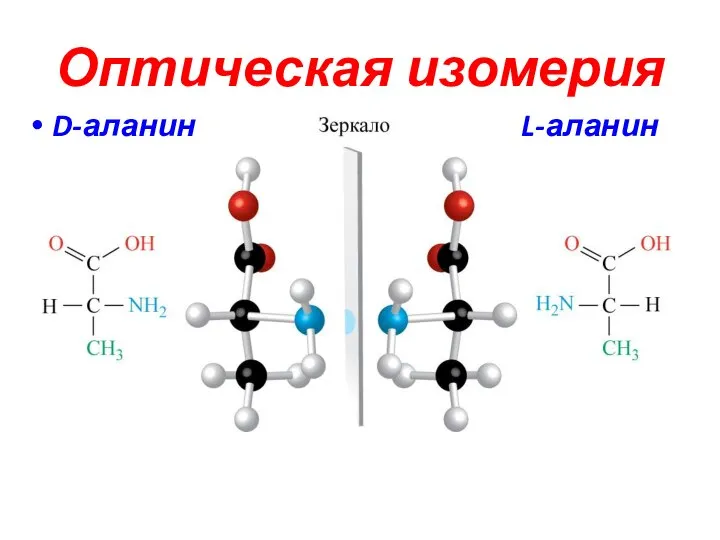
- 3. Оптическая изомерия D-аланин L-аланин
- 4. Способы получения 1. Гидролиз белков (для α-аминокислот)- Н+,ОН- ферментативный. Разделяют аминокислоты: ионообменной хром-ей, электрофорезом, ГЖХ. 2.
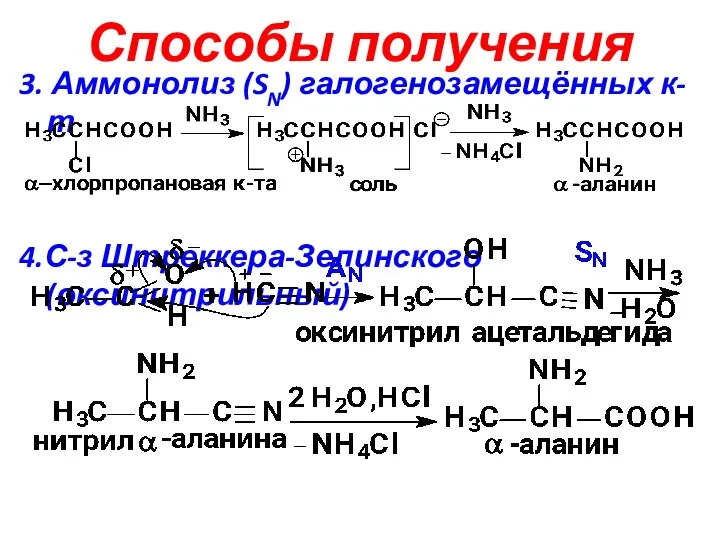
- 5. Способы получения 3. Аммонолиз (SN) галогенозамещённых к-т 4.С-з Штреккера-Зелинского(оксинитрильный)
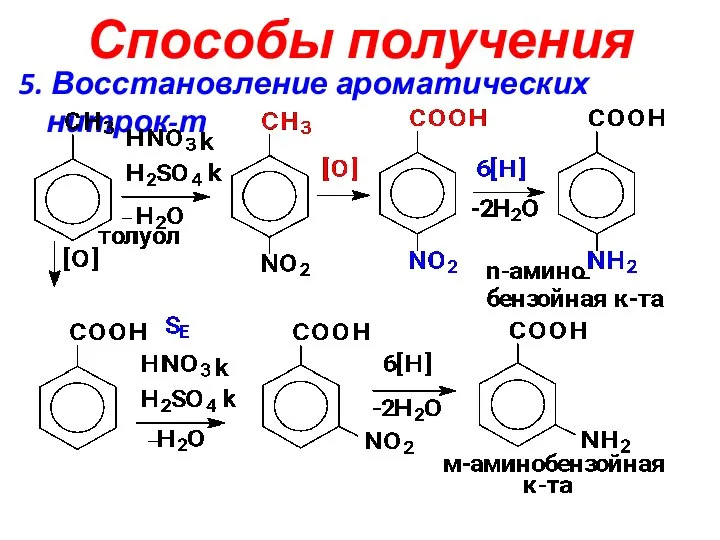
- 6. Способы получения 5. Восстановление ароматических нитрок-т
- 7. Физические св-ва α-аминок-т α-Аминокислоты–бесцветные крист. в-ва, ЛР в H2O, высокая tпл, нелетучи. Природные α-аминокислоты L-ряда –
- 8. Глутамат натрия E621 мононатриевая соль глутаминовой кислоты
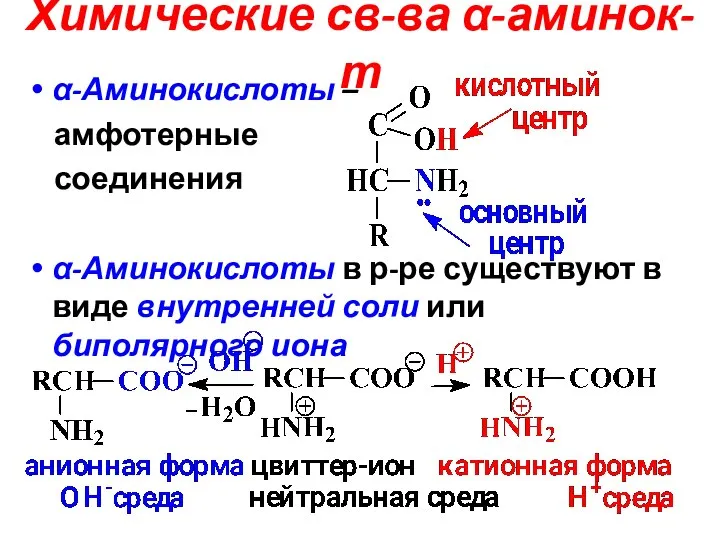
- 9. Химические св-ва α-аминок-т α-Аминокислоты – амфотерные соединения α-Аминокислоты в р-ре существуют в виде внутренней соли или
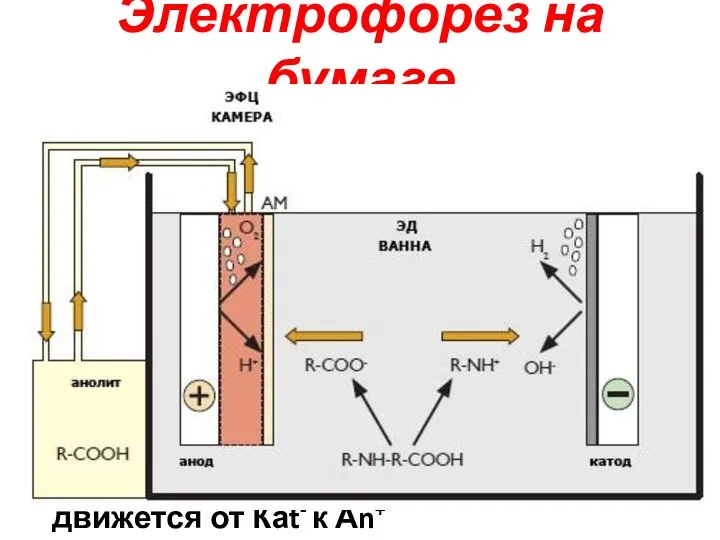
- 10. Ацетатный буферный р-р – аминокислота в катионной форме движется от Аn+ к Каt- Аммиачный буферный р-р
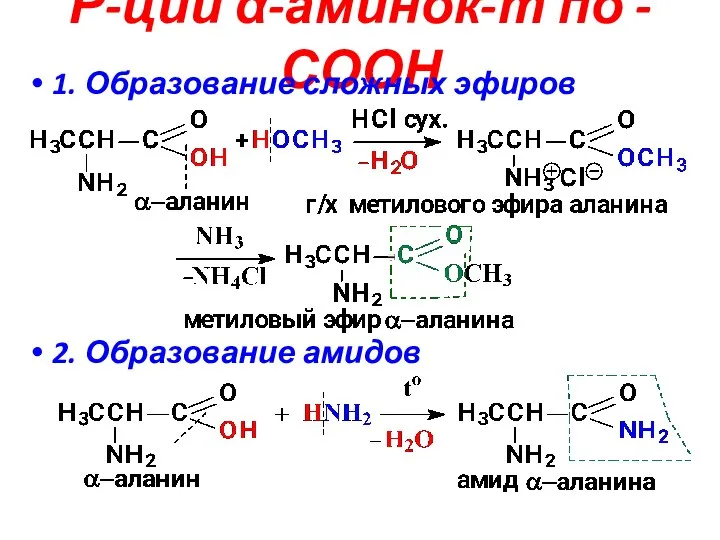
- 11. Р-ции α-аминок-т по -СООН 1. Образование сложных эфиров 2. Образование амидов
- 12. Р-ции α-аминок-т по -СООН 3. Образование галогенангидридов Ангидридов и галогенангидридов аминокислот не существует из-за высокой реакционоспособ-ти
- 13. Р-ции α-аминок-т по -NH2 1. Ацилирование (как способ защиты –NH2) 2. Алкилирование
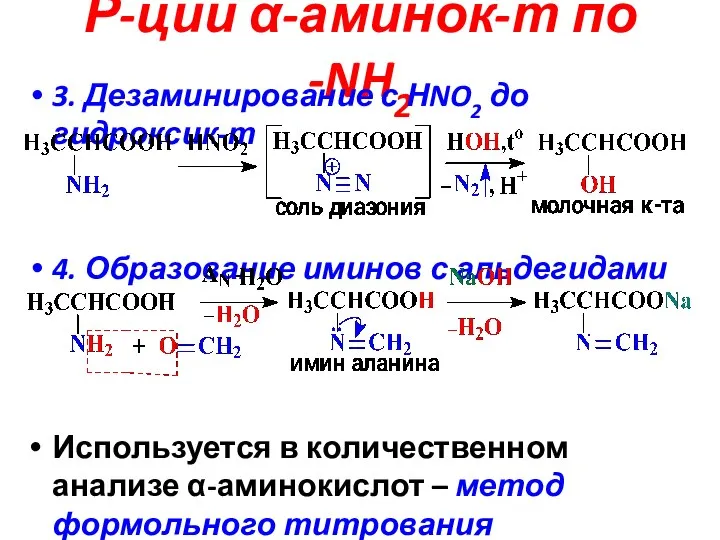
- 14. Р-ции α-аминок-т по -NH2 3. Дезаминирование с НNO2 до гидроксик-т 4. Образование иминов с альдегидами Используется
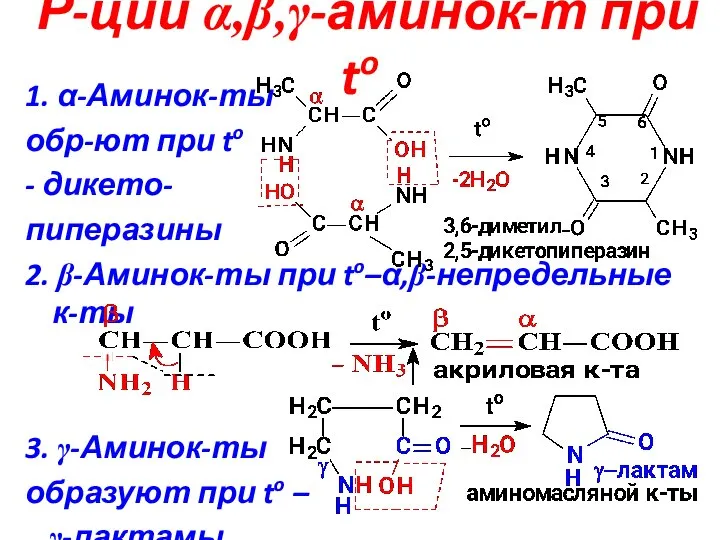
- 15. Р-ции α,β,γ-аминок-т при to 1. α-Аминок-ты обр-ют при to - дикето- пиперазины 2. β-Аминок-ты при to–α,β-непредельные
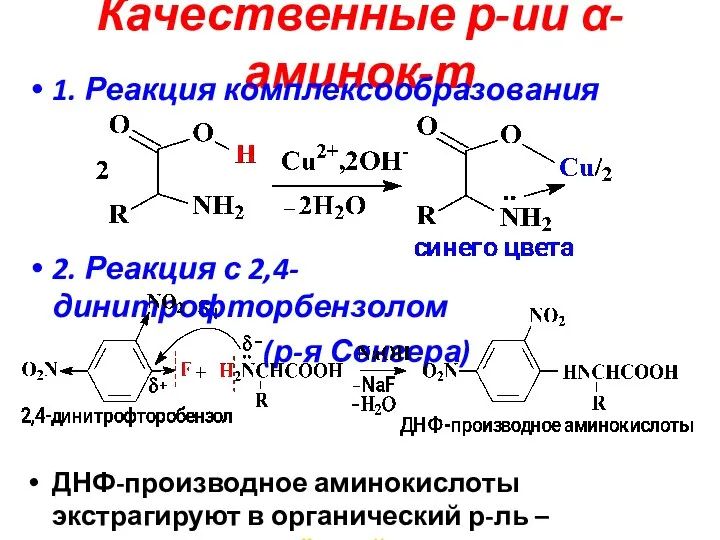
- 16. Качественные р-ии α-аминок-т 1. Реакция комплексообразования 2. Реакция с 2,4-динитрофторбензолом (р-я Сенгера) ДНФ-производное аминокислоты экстрагируют в
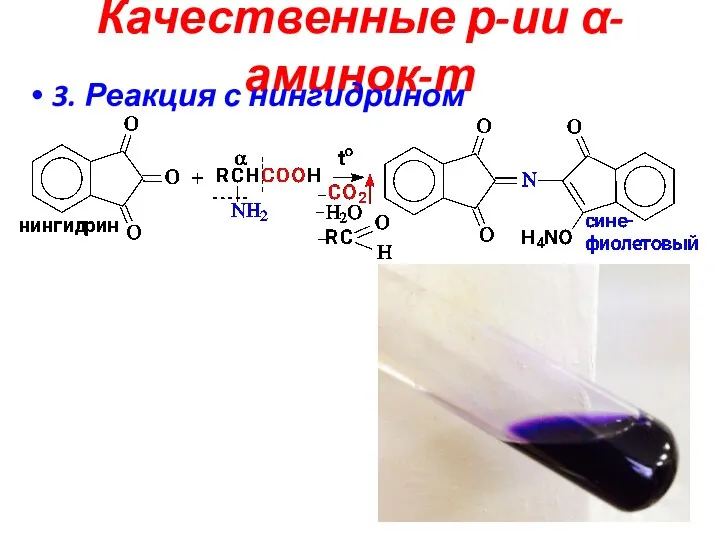
- 17. Качественные р-ии α-аминок-т 3. Реакция с нингидрином
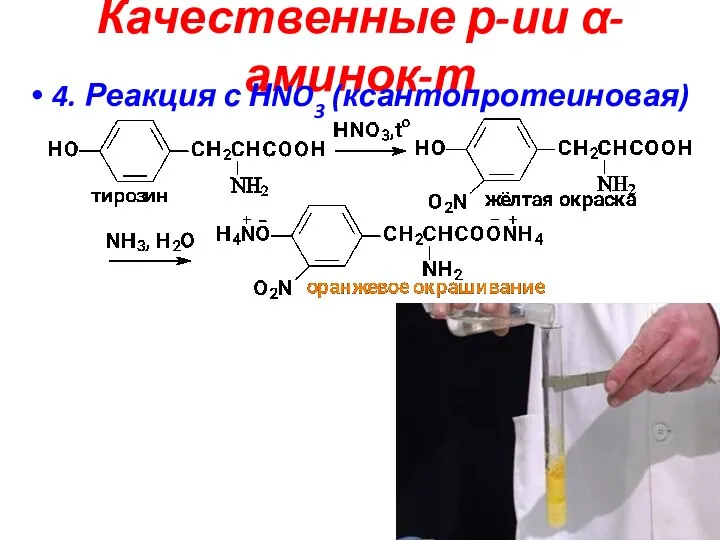
- 18. Качественные р-ии α-аминок-т 4. Реакция с НNO3 (ксантопротеиновая)
- 19. Применение аминокислот
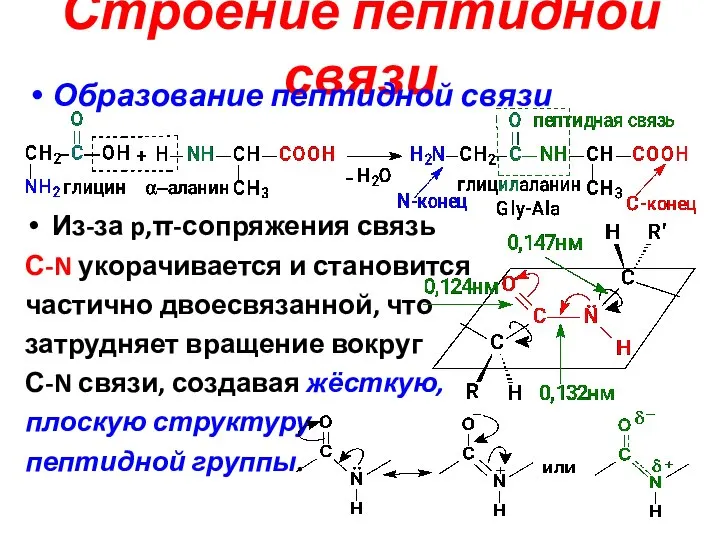
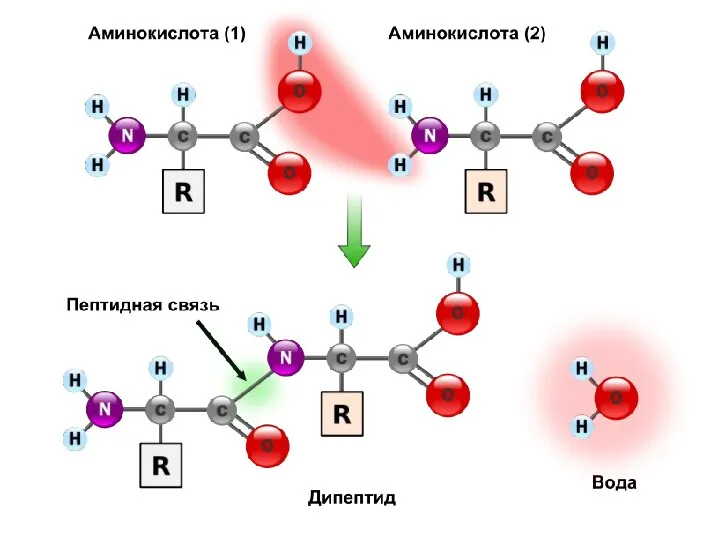
- 20. Строение пептидной связи Образование пептидной связи Из-за p,π-сопряжения связь С-N укорачивается и становится частично двоесвязанной, что
- 22. Пептидный синтез 1 ст. Защита -NH2 1-ой аминокислоты Ацилирование (SN) проводят хлорангидридами: 2 ст. Активация –СООН
- 23. Пептидный синтез 3 ст. Защита –СООН 2-ой аминокислоты 4 ст. Образование пептидной связи 5 ст. Удаление
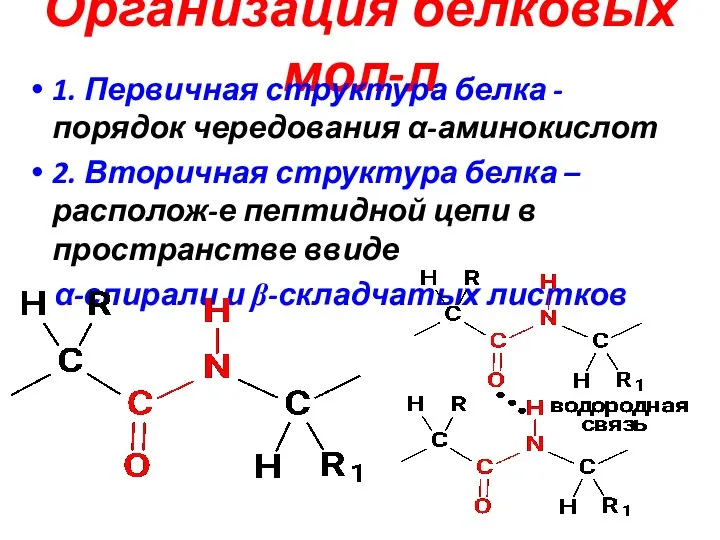
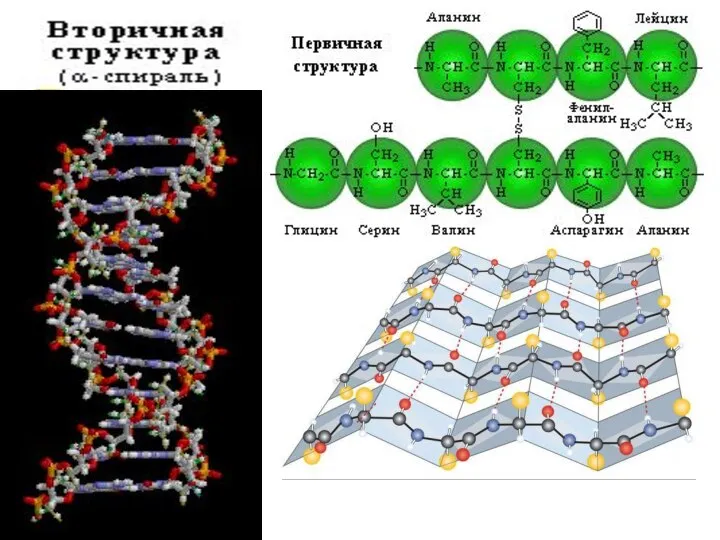
- 24. Организация белковых мол-л 1. Первичная структура белка - порядок чередования α-аминокислот 2. Вторичная структура белка –располож-е
- 27. Скачать презентацию








 Ароматерапия
Ароматерапия Фракционный состав нефти. Химический состав нефти
Фракционный состав нефти. Химический состав нефти Céramiques lesquelles choisi ?
Céramiques lesquelles choisi ? Арены. 10 класс
Арены. 10 класс Органическая химия. Введение
Органическая химия. Введение Технология получения полиуретанов
Технология получения полиуретанов Практико-ориентированные задачи по химии для студентов гуманитарных специальностей
Практико-ориентированные задачи по химии для студентов гуманитарных специальностей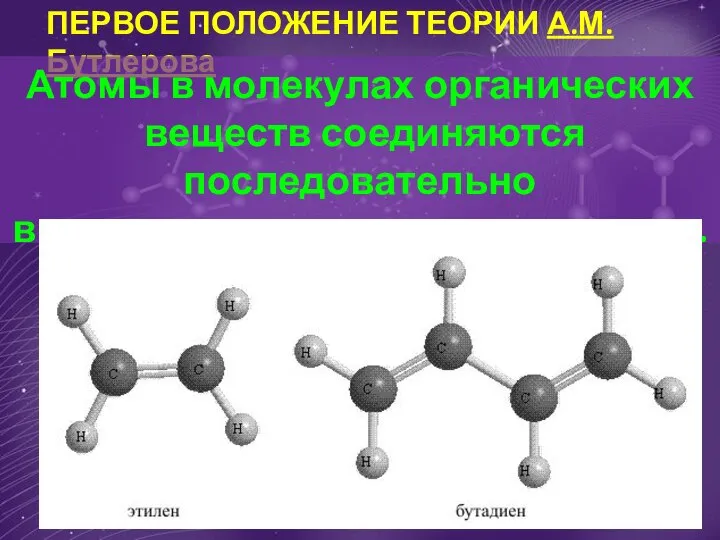 Первое положение теории А.М. Бутлерова Атомы в молекулах органических веществ соединяются последовательно
Первое положение теории А.М. Бутлерова Атомы в молекулах органических веществ соединяются последовательно Презентация на тему Бром
Презентация на тему Бром  Выращивание кристаллов соли и сахара в домашних условиях
Выращивание кристаллов соли и сахара в домашних условиях Презентация на тему Стронций
Презентация на тему Стронций  Алкены
Алкены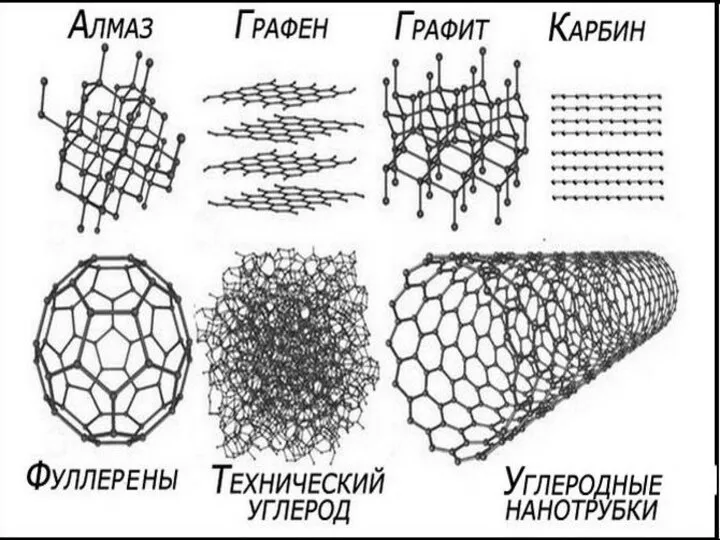 Углеродные нанотрубки
Углеродные нанотрубки Составление формул по валентности. Понятие
Составление формул по валентности. Понятие Положение металлов в периодической системе химических элементов
Положение металлов в периодической системе химических элементов Алканы
Алканы Учебное задание Расчет теплоты сгорания
Учебное задание Расчет теплоты сгорания Избыток, недостаток. Решение задач
Избыток, недостаток. Решение задач Кремний и его соединения
Кремний и его соединения Спирты и фенолы. (Лекция 6.1)
Спирты и фенолы. (Лекция 6.1) Валентность. Определение валентности элемента в оксиде
Валентность. Определение валентности элемента в оксиде Гемоглобин. Структура и свойства молекулы гемоглобина
Гемоглобин. Структура и свойства молекулы гемоглобина Какую воду мы пьем
Какую воду мы пьем Качественная реакция на многоатомные спирты
Качественная реакция на многоатомные спирты Олимпиада Ломоносов
Олимпиада Ломоносов Применение каучука
Применение каучука Презентация на тему Фолиевая кислота
Презентация на тему Фолиевая кислота  Химия в загадках
Химия в загадках