Содержание
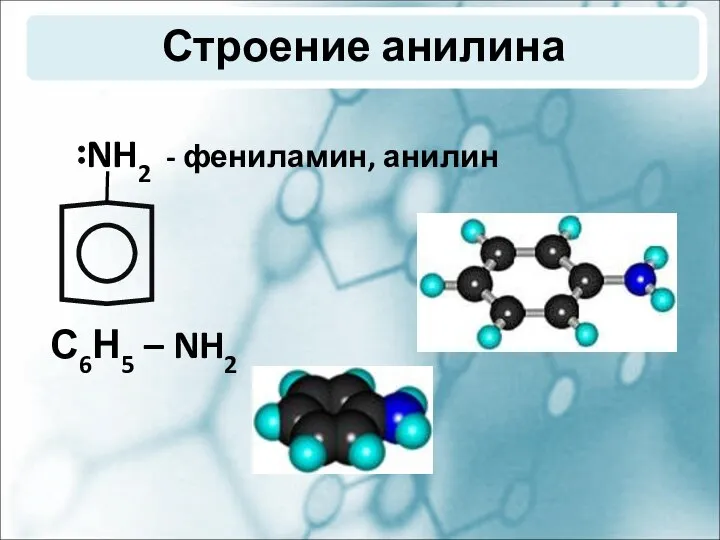
- 2. Строение анилина NH2 - фениламин, анилин С6Н5 – NH2
- 3. Физические свойства Анилин – бесцветная маслянистая жидкость, малорастворимая в воде, со слабым характерным запахом. Тяжелее воды.
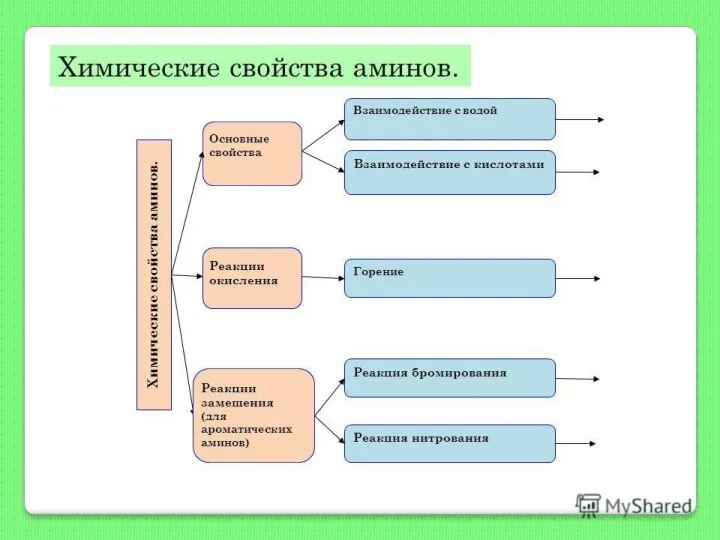
- 4. Химические свойства Бензольное ядро оттягивает свободную электронную пару от азота на себя. На атоме азота уменьшается
- 5. Химические свойства С6Н5–NH2 + HCl С6Н5–NH3 Cl хлорид фениламмония – хорошо растворим в воде, при добавлении
- 6. Химические свойства Аминогруппа подает электронную плотность на бензольное кольцо. В результате этого происходит поляризация единого 6-р-электронного
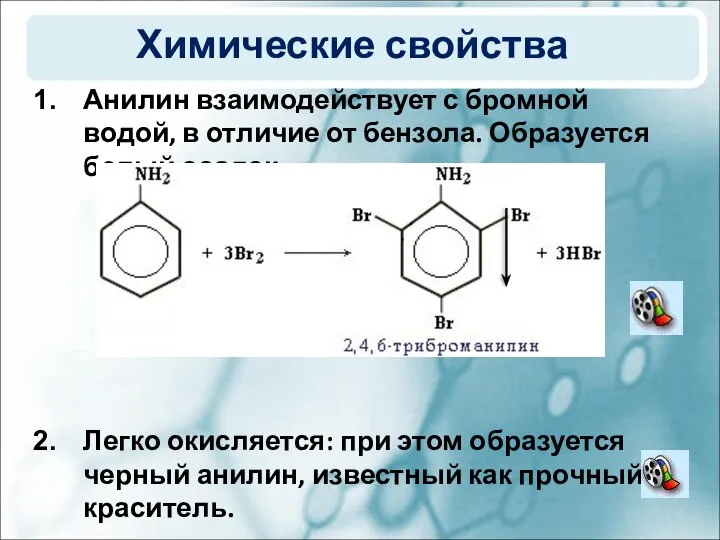
- 7. Химические свойства Анилин взаимодействует с бромной водой, в отличие от бензола. Образуется белый осадок. Легко окисляется:
- 8. Химические свойства Качественная реакция на анилин – реакция с хлорной известью Са(Cl)OCl – появляется характерное фиолетовое
- 10. Получение анилина Реакция Зинина – восстановление нитробензола водородом при t = 3000C C6H5 – NO2 +
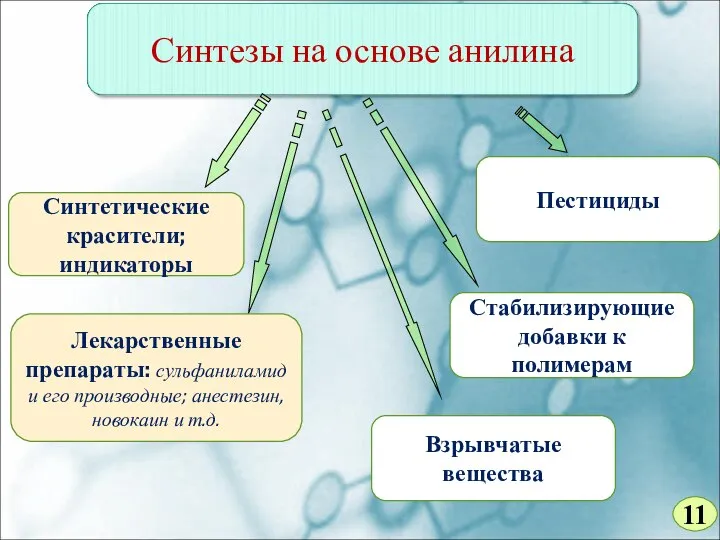
- 11. Синтетические красители; индикаторы Лекарственные препараты: сульфаниламид и его производные; анестезин, новокаин и т.д. Взрывчатые вещества Пестициды
- 13. Скачать презентацию






 Общая характеристика неметаллов
Общая характеристика неметаллов Изомерия. Классификация органических веществ.
Изомерия. Классификация органических веществ. Химия спирты одноатомные предельные
Химия спирты одноатомные предельные Композитные материалы
Композитные материалы Демокрит его вклад в развитие взглядов на строение вещества
Демокрит его вклад в развитие взглядов на строение вещества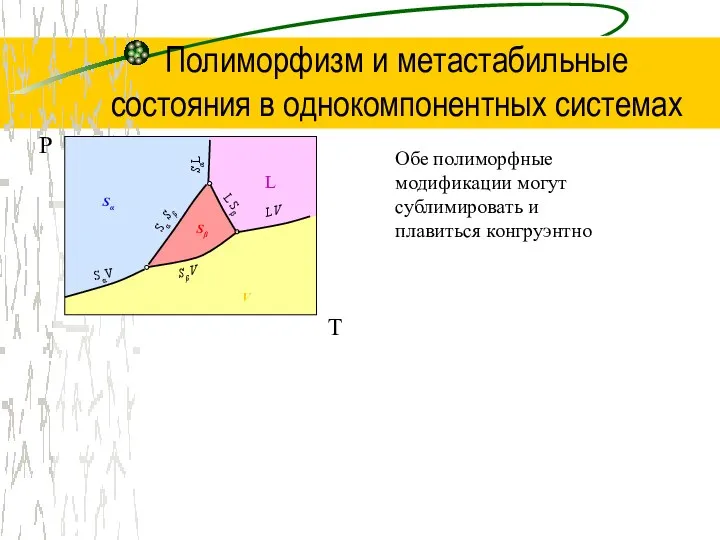 Полиморфизм и метастабильные состояния в однокомпонентных системах
Полиморфизм и метастабильные состояния в однокомпонентных системах Основи масообміну
Основи масообміну Количество вещества. Моль
Количество вещества. Моль Алюміній. Фізичні та хімічні властивості
Алюміній. Фізичні та хімічні властивості Хроматография
Хроматография Углеродистые конструкционные стали
Углеродистые конструкционные стали Жидкокристаллический эластомер как роторный актуатор
Жидкокристаллический эластомер как роторный актуатор Презентация на тему Игра по химии «Остров Периодическая Система»
Презентация на тему Игра по химии «Остров Периодическая Система»  Свойства растворов электролитов
Свойства растворов электролитов Производство аммиака
Производство аммиака Кислород. Общая характеристика, получение и свойства
Кислород. Общая характеристика, получение и свойства Презентация на тему Металлы
Презентация на тему Металлы  Количество вещества, число Авогадро, молярная масса, молярный объём, уравнение связи
Количество вещества, число Авогадро, молярная масса, молярный объём, уравнение связи Алкены
Алкены Презентация на тему Электронное и пространственное строение молекулы метана
Презентация на тему Электронное и пространственное строение молекулы метана  Циклоалканы. Физические свойства
Циклоалканы. Физические свойства Кислород
Кислород Синтетические органические соединения
Синтетические органические соединения Турнир Деда Мороза. Викторина по химии
Турнир Деда Мороза. Викторина по химии Презентация на тему Алмазы Индии
Презентация на тему Алмазы Индии  Алкены
Алкены Значимые личности в химии
Значимые личности в химии Стан електронів у атомі
Стан електронів у атомі