Слайд 3Распределение электронов по энергетическим уровням
+
N=1
N=2
N=3
N=4
N=5
N=6
N=7
ЭНЕРГИЯ Е УВЕЛИЧИВАЕТСЯ

Слайд 4Количество электронов на энергетических уровнях
N=2n2 N – номер уровня
n –

макс.число е
+
+
…
2e
8e
18е
32е
32е
N=1
N=2
N=3
N=4
N=5
Слайд 5 Электрон в атоме может находиться в любой точке пространства вокруг ядра,

однако вероятность его пребывания в разных местах атомного пространства различна.
Атомная орбиталь –
область вокруг ядра атома,
в которой наиболее вероятно
нахождение электрона.
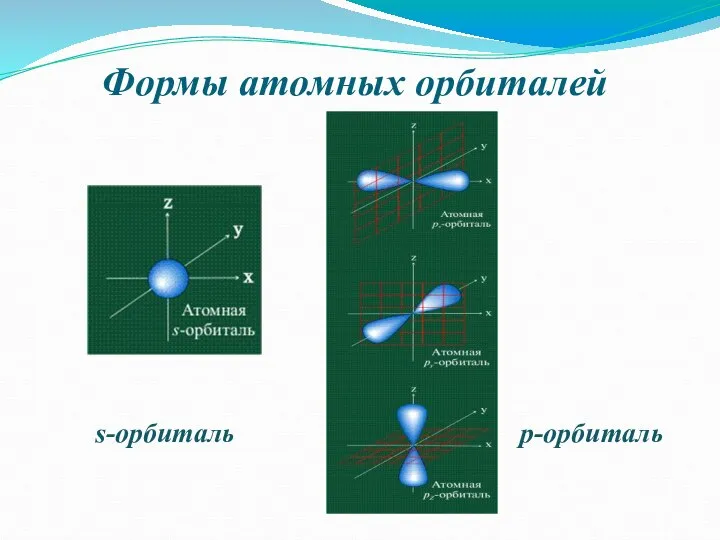
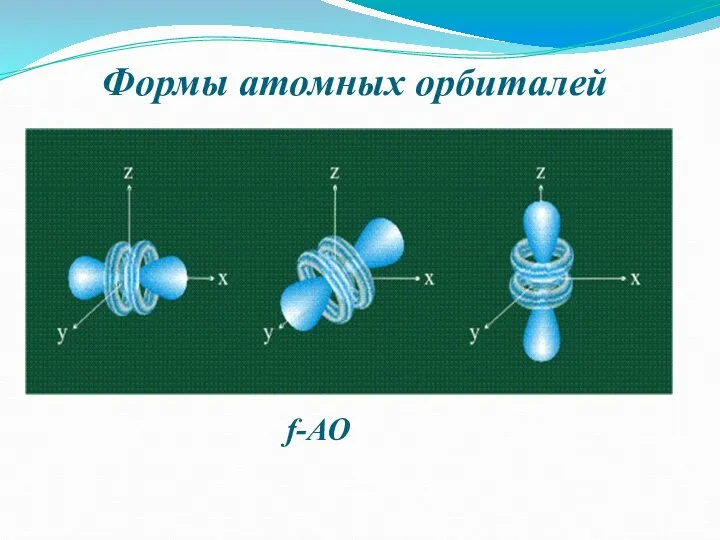
Слайд 7Формы атомных орбиталей
s-орбиталь
p-орбиталь
Слайд 10На одной орбитали могут находиться не более двух электронов, отличающихся друг от
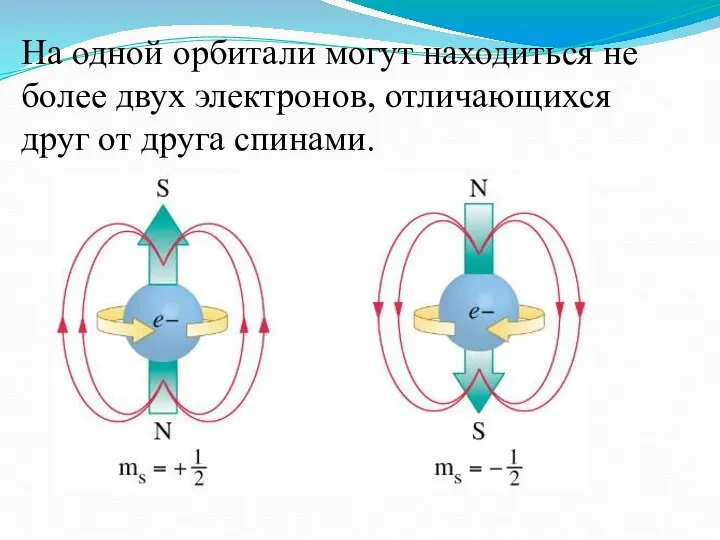
друга спинами.
Слайд 11 Принцип наименьшей энергии:
В атоме каждый электрон располагается так, чтобы его энергия была
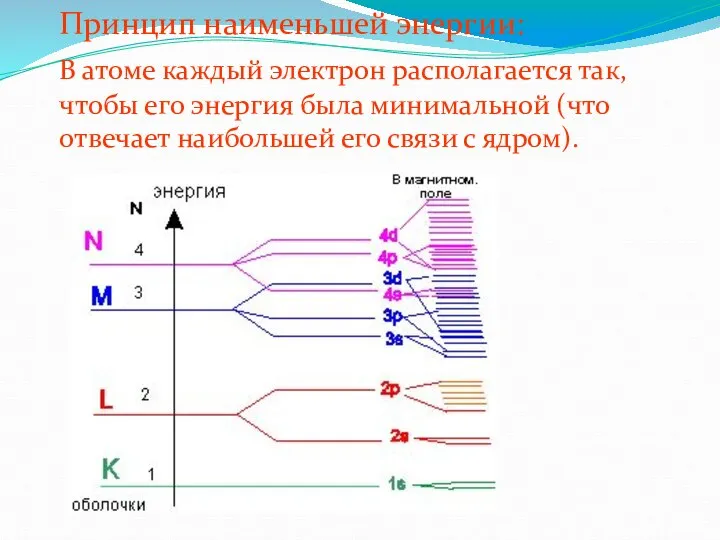
минимальной (что отвечает наибольшей его связи с ядром).
Слайд 12
+2 He )
2
1 S2
Пример движения электрона по
S-орбитали
+










 Производство серной кислоты
Производство серной кислоты Вода в природе. Состав, свойства и применение воды
Вода в природе. Состав, свойства и применение воды Бишофит - новый старый антигололедный реагент
Бишофит - новый старый антигололедный реагент Вода. Растворы
Вода. Растворы Закон сохранения массы и химические уравнения
Закон сохранения массы и химические уравнения Соли
Соли Нефть. Способы переработки нефти
Нефть. Способы переработки нефти Металлы побочных подгрупп
Металлы побочных подгрупп Модель химического образования на основе технологического подхода. Методическая система учителя химии
Модель химического образования на основе технологического подхода. Методическая система учителя химии Возможности окрашивания поверхности стекла путем высокотемпературной ионообменной обработки с выбранными реагентами
Возможности окрашивания поверхности стекла путем высокотемпературной ионообменной обработки с выбранными реагентами Химический элемент кислород
Химический элемент кислород Химическая география чудес природы
Химическая география чудес природы Материаловедение. Методы исследования в материаловедении (лекция 1)
Материаловедение. Методы исследования в материаловедении (лекция 1) Презентация по Химии "Схема получения моноизотопного кремния"
Презентация по Химии "Схема получения моноизотопного кремния"  Посвящение в химики
Посвящение в химики Наша стирка по-байкальски. Синтетические моющие средства (СМС¸ детергенты)
Наша стирка по-байкальски. Синтетические моющие средства (СМС¸ детергенты) Презентация на тему Неметаллы, особенности строения
Презентация на тему Неметаллы, особенности строения  Схема монооксигеназной цепи микросом
Схема монооксигеназной цепи микросом Общая характеристика оксидов
Общая характеристика оксидов Серная кислота
Серная кислота Основные понятия химии
Основные понятия химии Диссоциация веществ
Диссоциация веществ Химическая связь и ее типы
Химическая связь и ее типы Соли. Химические свойства
Соли. Химические свойства Соль. Добыча соли
Соль. Добыча соли Металлы. Атомы металлов
Металлы. Атомы металлов Природные источники углеводорода
Природные источники углеводорода Кислоты. Кислоты, вокруг нас
Кислоты. Кислоты, вокруг нас