Содержание
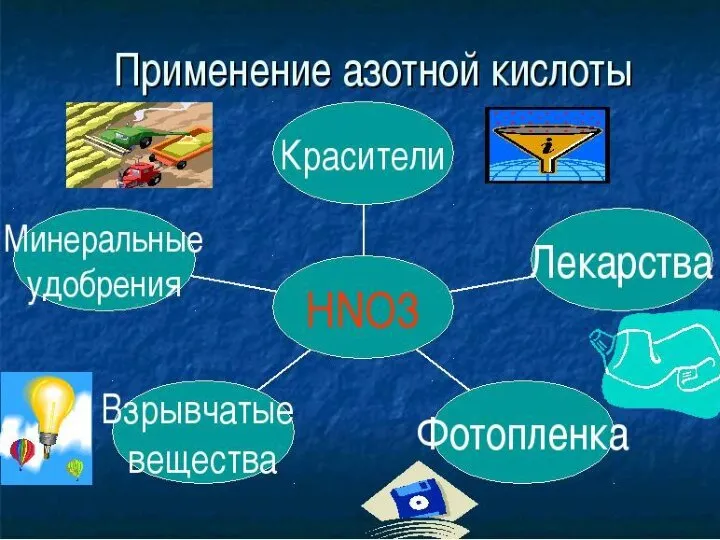
- 3. Её величество Азотная кислота
- 4. Строение Степень окисления азота в азотной кислоте равна +5. Связь – ковалентная полярная. Кристаллическая решетка –
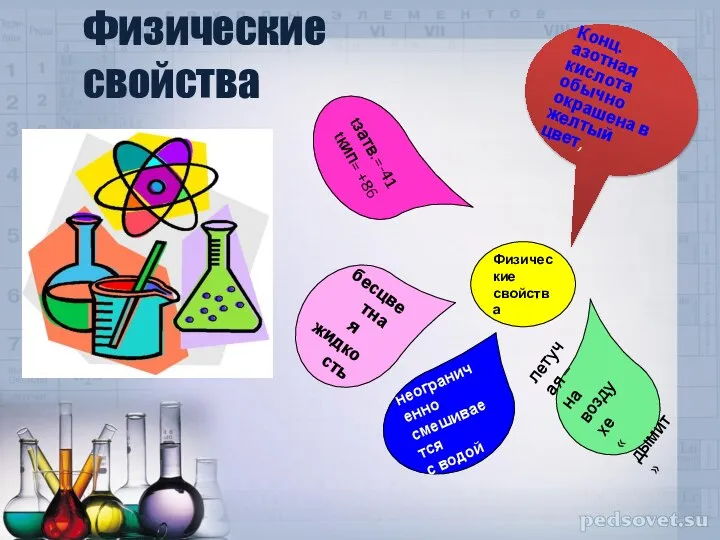
- 5. Физические свойства Физические свойства tзатв.=-41 tкип= +86 бесцветная жидкость неограниченно смешивается с водой летучая – на
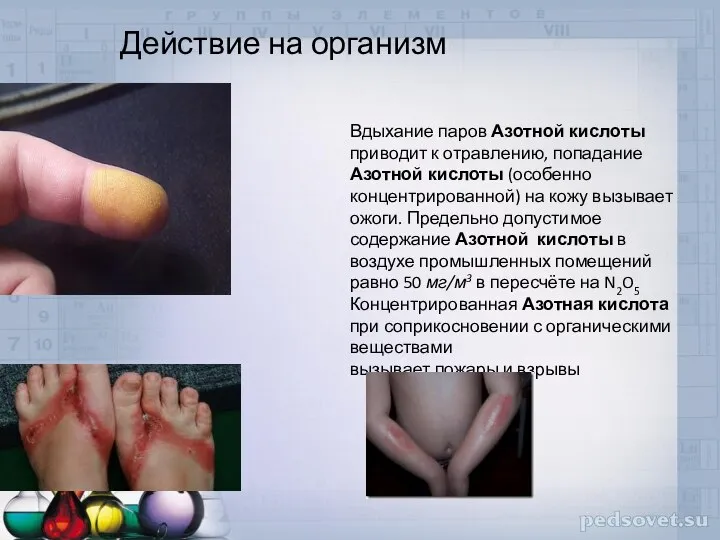
- 6. Действие на организм Вдыхание паров Азотной кислоты приводит к отравлению, попадание Азотной кислоты (особенно концентрированной) на
- 7. Исследования (задания по группам). 1 группа: провести реакцию раствора азотной кислоты и оксида меди (II), записать
- 8. Общие с другими кислотами: 1. Сильный электролит, хорошо диссоциируют на ионы HNO3 -> H+ +NO3- Изменяет
- 9. Взаимодействие с металлами: При взаимодействии с металлами образуются нитрат, вода и третий продукт по схеме: HNO3(р.)+Me(до
- 10. 4HN+5O3 + Hg0 = Hg+2(NO3)2 + 2N+4O2 + 2H2O N+5 + 1e → N+4 1 2
- 12. Проверь себя: Степень окисления азота в HNO3 а)-3 б)0 в)+5 г)+4 При хранении на свету HNO3
- 13. Ключ: 1 - в 2 - б 3 - а 4 - а 5 - б
- 14. Вывод: 1. Азотной кислоте характерны общие свойства кислот: реакция на индикатор, взаимодействие с оксидами металлов, гидроксидами,
- 15. Домашнее задание: §26 упр. 2,7 Творческие задания: способы получения азотной кислоты. Почему « царская водка» растворяет
- 17. Скачать презентацию











 Презентация на тему Ковалентная связь: полярная и неполярная
Презентация на тему Ковалентная связь: полярная и неполярная  Производство нитрата аммония (лекция 16)
Производство нитрата аммония (лекция 16) Презентация на тему В мире индикаторов - исследовательская работа
Презентация на тему В мире индикаторов - исследовательская работа  Современные подходы к преподаванию химии
Современные подходы к преподаванию химии Алюминий. Строение и свойства атома
Алюминий. Строение и свойства атома Жизнь и деятельность Д.И.Менделеева «Если не будешь знать имен, то умрет и познание вещей» К.Линей. Автор: Ватитова А.А. МОУ Еласов
Жизнь и деятельность Д.И.Менделеева «Если не будешь знать имен, то умрет и познание вещей» К.Линей. Автор: Ватитова А.А. МОУ Еласов Природные источники углеводородов
Природные источники углеводородов Химия вокруг нас. 10 класс
Химия вокруг нас. 10 класс Амины. Аминокислоты
Амины. Аминокислоты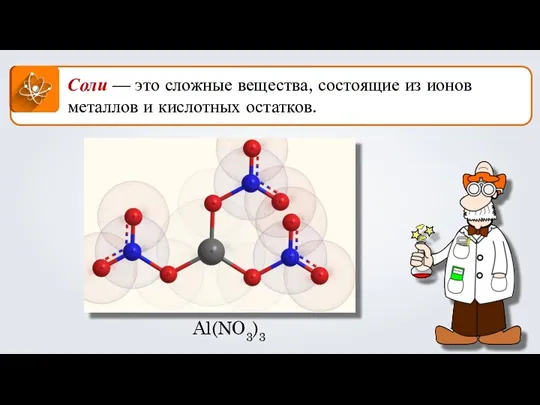 Соли. Формула соли
Соли. Формула соли Вода. Классы неорганических соединений. 8 класс
Вода. Классы неорганических соединений. 8 класс Ковалентная полярная связь
Ковалентная полярная связь Коллоидные системы Классификация. Получение. Очистка. Свойства. Устойчивость и коагуляция. Применение
Коллоидные системы Классификация. Получение. Очистка. Свойства. Устойчивость и коагуляция. Применение Основные соединения кальция и их применение – вчера, сегодня, завтра.
Основные соединения кальция и их применение – вчера, сегодня, завтра. Вуглеводи. Визначення вуглеводів
Вуглеводи. Визначення вуглеводів Алотропия углерода
Алотропия углерода ÐÐÐÐ ÐÐТÐÐРХÐÐÐЧÐСÐÐÐ¥ Ð ÐÐÐЦÐÐ
ÐÐÐÐ ÐÐТÐÐРХÐÐÐЧÐСÐÐÐ¥ Ð ÐÐÐЦÐÐ Изменения, происходящие с веществами Урок химии 8 класс Учитель химии МОУ «СОШ №7» г. Балаково Саратовская обл.
Изменения, происходящие с веществами Урок химии 8 класс Учитель химии МОУ «СОШ №7» г. Балаково Саратовская обл. Химический процесс: энергетика и равновесие
Химический процесс: энергетика и равновесие Презентация на тему Химическое равновесие
Презентация на тему Химическое равновесие 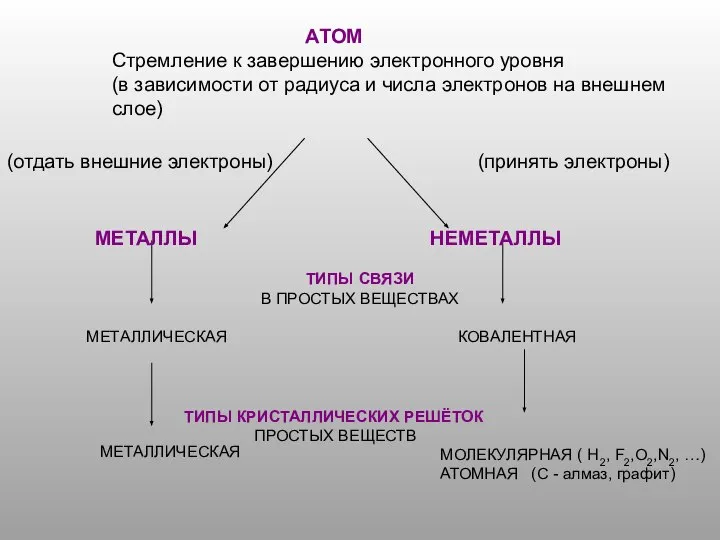 Атом. Стремление к завершению электронного уровня
Атом. Стремление к завершению электронного уровня Кислоты. Классификация кислот
Кислоты. Классификация кислот Коррозия металлов
Коррозия металлов Теория активированного комплекса
Теория активированного комплекса Л-1-5
Л-1-5 Презентация на тему Фенол и его свойства
Презентация на тему Фенол и его свойства  Процессы растворения твёрдых веществ
Процессы растворения твёрдых веществ Степень окисления. Бинарные соединения
Степень окисления. Бинарные соединения