Содержание
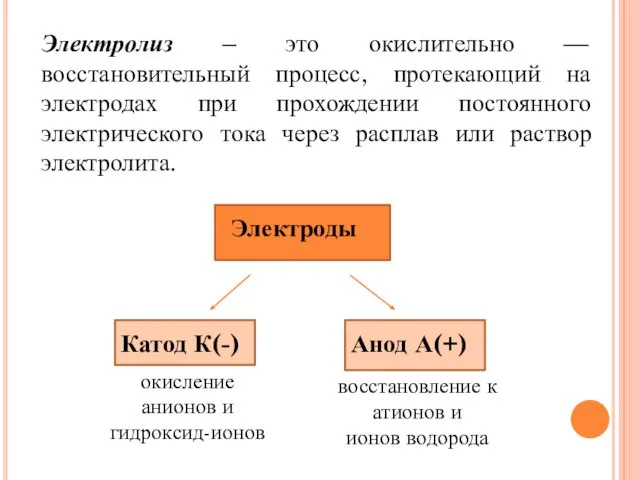
- 2. Электролиз – это окислительно — восстановительный процесс, протекающий на электродах при прохождении постоянного электрического тока через
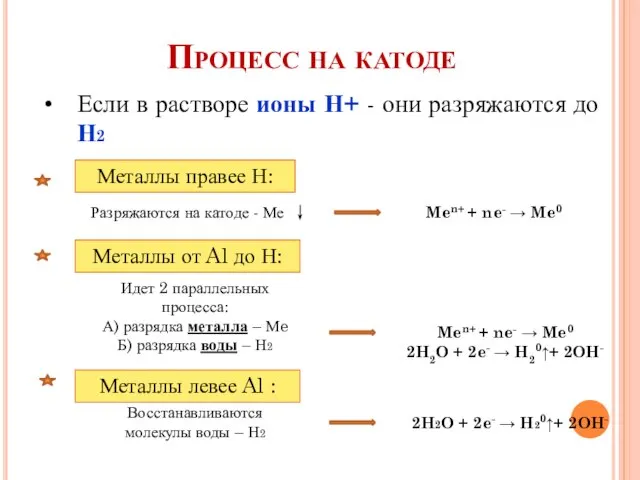
- 3. Процесс на катоде Если в растворе ионы Н+ - они разряжаются до Н2 Металлы правее Н:
- 4. Процесс на аноде если анод растворяется (железо, цинк, медь, серебро и все металлы, которые окисляются в
- 5. Анионы бескислородных кислот (кроме F-) Разряжаются до простого вещества: S2-, I-, Br-, СI- Анионы кислородсодержащих кислот
- 6. 1. Анод нерастворимый (например, графитовый) Суммарное уравнение: Учитывая присутствие ионов Na в растворе: Пример №1.
- 7. 2. Анод растворимый (например, медный) Если анод растворимый, то металл анода будет окисляться: Катионы Cu2+ в
- 8. При электролизе водного раствора хлорида лития (LiCL) на аноде в результате электролиза образуется: 1) хлор 2)
- 10. Скачать презентацию





 Фуллерены (шары Бакминстера)
Фуллерены (шары Бакминстера) Алюминий и его органические производные
Алюминий и его органические производные Презентация на тему Кристаллические решетки 9 класс
Презентация на тему Кристаллические решетки 9 класс  Энергетический обмен
Энергетический обмен Ионная связь
Ионная связь Свойства солей, оксидов, оснований
Свойства солей, оксидов, оснований Генетические ряды Fe2+ и Fе3+. Качественные реакции на Fе2+ и Fе3+
Генетические ряды Fe2+ и Fе3+. Качественные реакции на Fе2+ и Fе3+ Презентация на тему Йод
Презентация на тему Йод  Роль Хеуорса, Фишера, Лемье в изучении структуры углеводов
Роль Хеуорса, Фишера, Лемье в изучении структуры углеводов Конструкционные и специальные материалы холодильной техники
Конструкционные и специальные материалы холодильной техники Перициклические реакции
Перициклические реакции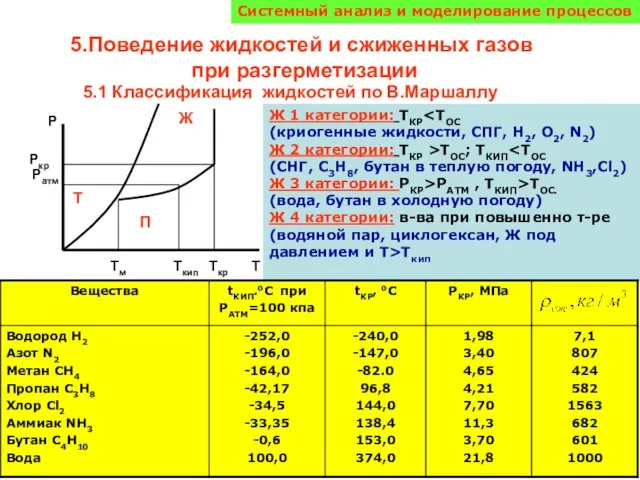 Поведение жидкостей и сжиженных газов при разгерметизации
Поведение жидкостей и сжиженных газов при разгерметизации Контроль качества лекарственных средств, производных карбоновых кислот и аминокислот
Контроль качества лекарственных средств, производных карбоновых кислот и аминокислот Получение армированных фотополимерных композиций
Получение армированных фотополимерных композиций Group 6 Cations
Group 6 Cations Русские ученые и топонимы в периодической системе химических элементов Д.И. Менделеева
Русские ученые и топонимы в периодической системе химических элементов Д.И. Менделеева Пищевые кислоты
Пищевые кислоты Предельные углеводороды. Алканы, насыщенные углеводороды, парафины, циклоалканы
Предельные углеводороды. Алканы, насыщенные углеводороды, парафины, циклоалканы Полиамиды (ПА)
Полиамиды (ПА) Окислители в пиросоставах
Окислители в пиросоставах Вебинар. Гидролиз солей
Вебинар. Гидролиз солей Совместимость материалов
Совместимость материалов Молярная масса вещества
Молярная масса вещества Композитные материалы
Композитные материалы Типы химической связи
Типы химической связи Презентация на тему Законы газового состояния вещества
Презентация на тему Законы газового состояния вещества  Development of the system of concepts on the topic redox reactions in the school course of inorganic chemistry
Development of the system of concepts on the topic redox reactions in the school course of inorganic chemistry Аммиак: состав, строение, свойства, применение
Аммиак: состав, строение, свойства, применение