Содержание
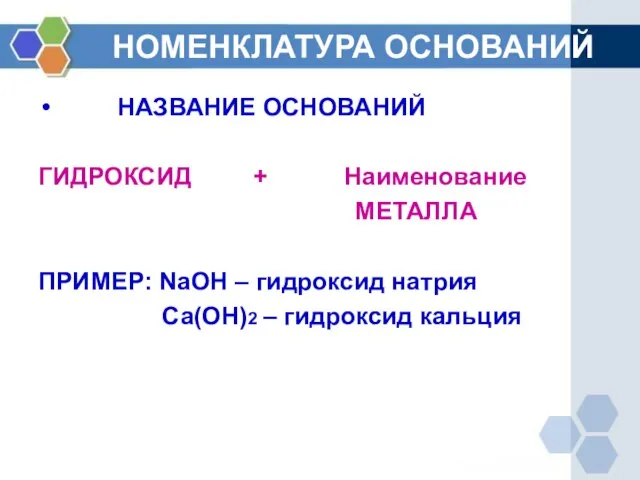
- 2. НОМЕНКЛАТУРА ОСНОВАНИЙ НАЗВАНИЕ ОСНОВАНИЙ ГИДРОКСИД + Наименование МЕТАЛЛА ПРИМЕР: NaOH – гидроксид натрия Ca(OH)2 – гидроксид
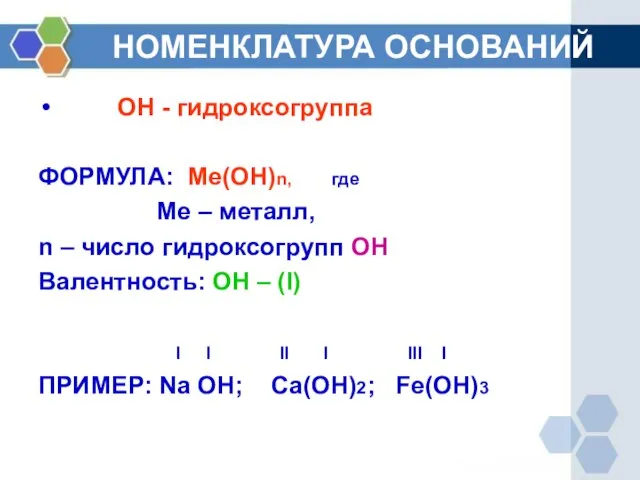
- 3. НОМЕНКЛАТУРА ОСНОВАНИЙ ОН - гидроксогруппа ФОРМУЛА: Ме(ОН)n, где Ме – металл, n – число гидроксогрупп ОН
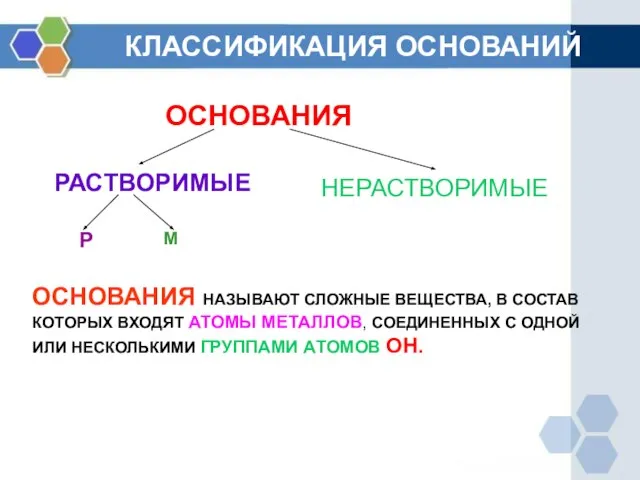
- 4. КЛАССИФИКАЦИЯ ОСНОВАНИЙ ОСНОВАНИЯ РАСТВОРИМЫЕ НЕРАСТВОРИМЫЕ Р М ОСНОВАНИЯ НАЗЫВАЮТ СЛОЖНЫЕ ВЕЩЕСТВА, В СОСТАВ КОТОРЫХ ВХОДЯТ АТОМЫ
- 5. НАПИСАТЬ ХИМИЧЕСКИЕ ФОРМУЛЫ ОСНОВАНИЙ 1)Гидроксид железа(III) 2)Гидроксид магния(II) 3) Гидроксид бария (II) 4) Гидроксид алюминия(III) 5)
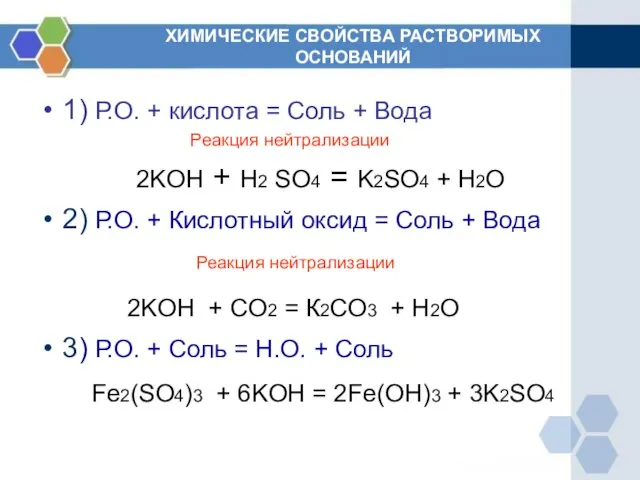
- 6. ХИМИЧЕСКИЕ СВОЙСТВА РАСТВОРИМЫХ ОСНОВАНИЙ 1) Р.О. + кислота = Соль + Вода Реакция нейтрализации 2KOH +
- 7. ХИМИЧЕСКИЕ СВОЙСТВА РАСТВОРИМЫХ ОСНОВАНИЙ 4) Действуют на индикаторы 5) при умеренном нагревании не разлагаются 6) разъедают
- 9. Скачать презентацию


 Строение атома
Строение атома Уравнение состояния
Уравнение состояния Общая характеристика металлов
Общая характеристика металлов Углеводороды. Предельные (насыщенные) углеводороды
Углеводороды. Предельные (насыщенные) углеводороды Водород
Водород ОВР в гетерогенных системах
ОВР в гетерогенных системах Каскадный синтез пептидов
Каскадный синтез пептидов Синтез.Малахит
Синтез.Малахит Презентация на тему: Подгруппа азота
Презентация на тему: Подгруппа азота Минералы
Минералы Серная кислота
Серная кислота Сложные эфиры
Сложные эфиры Своя игра. Химия и охрана почв
Своя игра. Химия и охрана почв АЛКИНЫ (ацетиленовые углеводороды)
АЛКИНЫ (ацетиленовые углеводороды) Связь между основными классами неорганических соединений
Связь между основными классами неорганических соединений Периодическая система Д.И. Менделеева
Периодическая система Д.И. Менделеева Уравнения химических реакций
Уравнения химических реакций Органическая химия
Органическая химия Исследование физико-химических свойств растворов сахарозы
Исследование физико-химических свойств растворов сахарозы Презентация на тему Фосфор. Соединения фосфора
Презентация на тему Фосфор. Соединения фосфора  Вычисление массовой доли химического элемента в веществе
Вычисление массовой доли химического элемента в веществе Бирюза. Характеристики минерала
Бирюза. Характеристики минерала Окислительно-восстановительные реакции (ОВР)
Окислительно-восстановительные реакции (ОВР) Простые вещества – металлы и неметаллы
Простые вещества – металлы и неметаллы Белки. Структуры белков
Белки. Структуры белков Сложные реакции
Сложные реакции Моделирование состава биоплёночного материала
Моделирование состава биоплёночного материала Химическое равновесие
Химическое равновесие