Содержание
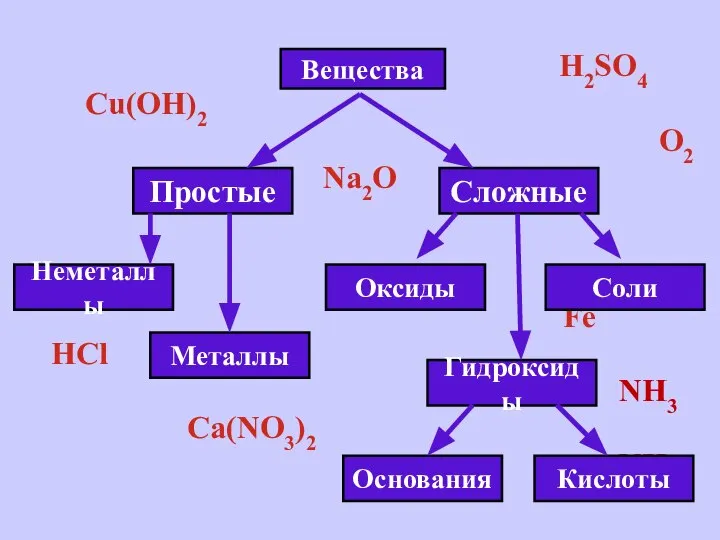
- 2. H2SO4 Cu(OH)2 O2 Na2O Fe HCl NH3 Ca(NO3)2 NH3 Вещества Простые Металлы Неметаллы Оксиды Основания Кислоты
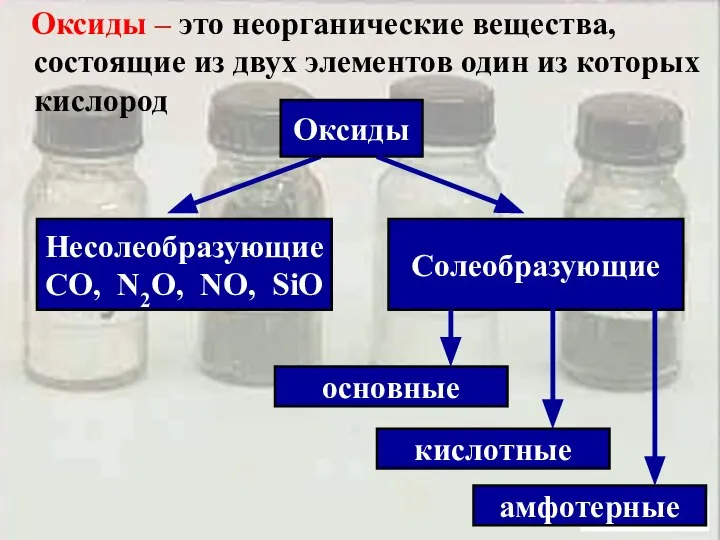
- 3. Солеобразующие основные кислотные Оксиды Несолеобразующие CO, N2O, NO, SiO амфотерные Оксиды – это неорганические вещества, состоящие
- 4. Основные оксиды образованы металлами со степенью окисления +1, +2: + -2 Na2O +2 -2 MgO Каждому
- 5. Основные оксиды взаимодействуют с кислотами, образуя соль и воду: - + - Na2O + 2HCl =
- 6. Кислотные оксиды образованы неметаллами и некоторыми металлами, если в оксиде они проявляют высшую валентность: SO2, CO2
- 7. Каждому кислотному оксиду соответствует кислота: CO2 – H2CO3 N2O5 – HNO3 SO2 – H2SO3 P2O5 –
- 8. Кислотные оксиды взаимодействуют с основаниями, образуя соль и воду: + 2- SO2 + 2NaOH = Na2SO3
- 9. Амфотерные оксиды образованы металлами со степенью окисления +3, +4, реже +2: ZnO, Al2O3, Fe2O3, Cr2O3 Амфотерным
- 10. Химические свойства оксидов
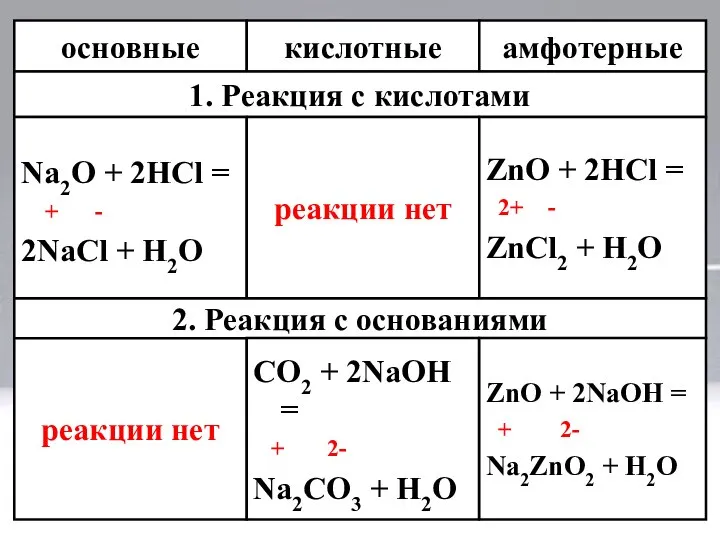
- 11. основные кислотные амфотерные 1. Реакция с кислотами Na2O + 2HCl = + - 2NaCl + H2O
- 13. Скачать презентацию







 Растворы. Определение
Растворы. Определение Особо чистые вещества. Занятие13
Особо чистые вещества. Занятие13 Общая характеристика нефти и газа
Общая характеристика нефти и газа Углеродные материалы. Основные понятия и определения. Области их применения
Углеродные материалы. Основные понятия и определения. Области их применения Проверочные работы по темам: Неметаллы. 9 класс
Проверочные работы по темам: Неметаллы. 9 класс Повторение пройденного
Повторение пройденного Сильные и слабые кислоты и основания
Сильные и слабые кислоты и основания Пептиды, белки. Лабораторное занятие
Пептиды, белки. Лабораторное занятие Кристаллы и аморфные тела
Кристаллы и аморфные тела Презентация на тему Жидкие кристаллы
Презентация на тему Жидкие кристаллы  Физическая химия, термодинамика
Физическая химия, термодинамика Периодический закон Д.И.Менделеева
Периодический закон Д.И.Менделеева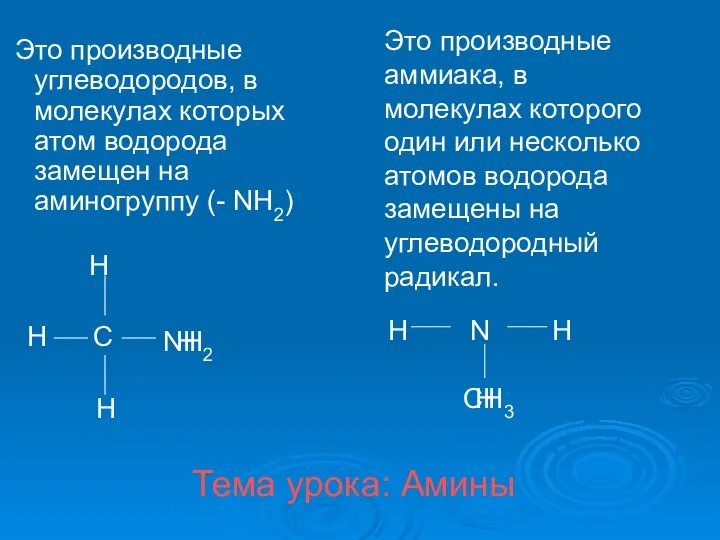 Амины. Классификация аминов
Амины. Классификация аминов Предмет органической химии. Теория химического строения органических веществ. 9 класс
Предмет органической химии. Теория химического строения органических веществ. 9 класс Химические равновесия в растворах. Константы равновесия при различном выборе стандартных состояний для участников реакции
Химические равновесия в растворах. Константы равновесия при различном выборе стандартных состояний для участников реакции Белки-1 2020
Белки-1 2020 Химические свойства металлов
Химические свойства металлов Химическая коррозия
Химическая коррозия Дигибридное скрещивание.Третий закон Г.Менделя.
Дигибридное скрещивание.Третий закон Г.Менделя. Металлы тоже воевали… 8 класс
Металлы тоже воевали… 8 класс Спирты
Спирты Повторение по теме: « Химическая связь. Строение вещества». Виды химических связей Типы кристаллических
Повторение по теме: « Химическая связь. Строение вещества». Виды химических связей Типы кристаллических Способы разделения смесей. Урок в 8 классе
Способы разделения смесей. Урок в 8 классе Сказка о братьях карбонатах
Сказка о братьях карбонатах Оксидті шикізаттан темір ұнтағын алу технологиясын жасау
Оксидті шикізаттан темір ұнтағын алу технологиясын жасау Сахароза (С12Н22О11)
Сахароза (С12Н22О11) Тест по неметаллам
Тест по неметаллам Строение комплексных соединений. Лекция 4
Строение комплексных соединений. Лекция 4