Содержание
- 2. Основные вопросы лекции: 1. Предмет изучения биоорганической химии 2. Классификация органических реакций. 2. Реакции SR алканов,
- 3. Биоорганическая химия изучает строение и свойства веществ, участвующих в процессах жизнедеятельности, в непосредственной связи с познанием
- 4. Субстрат – вещество, в котором происходит разрыв старых и образование новых связей с участием атома углерода.
- 5. Классификация реакций По направлению и конечному результату: Реакции присоединения – А; Реакции замещения – S; Реакции
- 6. Классификация реакций По характеру изменения связей в субстратах и реагентах: реакции радикальные (гомолитический тип разрыва связей)
- 7. Ионные реакции в зависимости от природы реагента: электрофильные нуклеофильные Классификация реакций
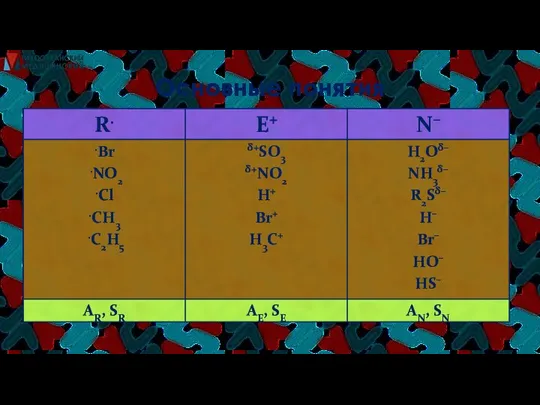
- 8. Основные понятия РАДИКАЛЫ(R.) – свободные атомы или частицы с неспаренным электроном (.CH3, Cl., Br .). ЭЛЕКТРОФИЛЫ
- 9. Основные понятия
- 10. Алканы CnH2n+2
- 11. Реакции радикального замещения (SR) – … … реакции замещения, в которых атаку осуществляют свободные радикалы —
- 12. Пример SR реакции 1)Инициирование реакции 2) Развитие цепи
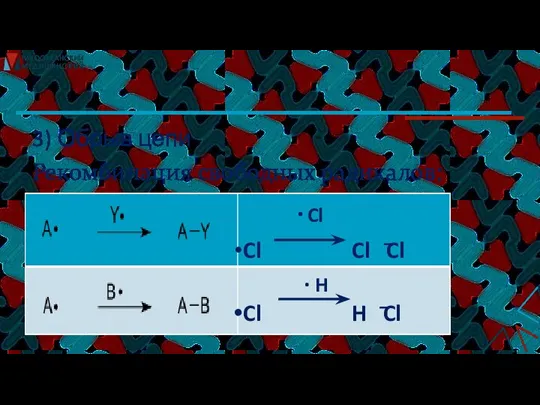
- 13. 3) Обрыв цепи Рекомбинация свободных радикалов:
- 14. Региоселективность реакций SR Реакция галогенирования (Br2, Cl2) протекающая по механизму радикального замещения (SR), характеризуется региоселективностью, т.е.
- 15. * Биологическая роль SR *Поражение кроветворных систем, кожных покровов, желез внутренней секреции, иммунной системы, мутации. *
- 16. Алкены CnH2n
- 17. Механизм реакций АE Реакция идет по механизму электрофильного присоединения (AE) Нижник Я.П. http://norgchem.professorjournal.ru
- 18. Реакции электрофильного присоединения (АЕ) — … … реакции, в которых атаку на начальной стадии осуществляет электрофил
- 19. М е х а н и з м р е а к ц и й АE
- 20. М е х а н и з м р е а к ц и й АE
- 21. Гидрогалогенирование (присоединение галогеноводородов) пропен 2-хлорпропан Реакции идут по механизму электрофильного присоединения (AE) CH2 = CH2 +
- 22. М е х а н и з м р е а к ц и й АE
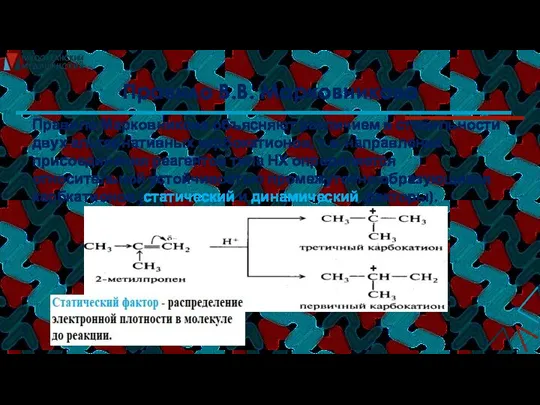
- 23. Правило В.В. Марковникова При присоединении веществ типа НХ (НCl, HBr, HOH) к нессиметричным алкенам, водород присоединяется
- 24. Правило Марковникова объясняют различием в стабильности двух альтернативных карбокатионов, т.е. направление присоединения реагентов типа НХ определяется
- 25. Относительная устойчивость карбкатионов определяется возможностью частичной делокализации положительного заряда в каждом из них (динамический фактор). Алкильные
- 26. Гидратация (присоединение воды) Реакция идет по механизму электрофильного присоединения (AE) в соответствии с правилом Марковникова. этилен
- 27. Механизм реакции гидратации алкенов (AE)
- 28. * Биороль реакций AE *Расщепление жиров в организме, ЖК, углеводов. *Процессы окисления в клетках ЖК липидов.
- 29. фумаровая кислота яблочная кислота Нижник Я.П. http://norgchem.professorjournal.ru Присоединение воды к двойной связи протекает в организме и
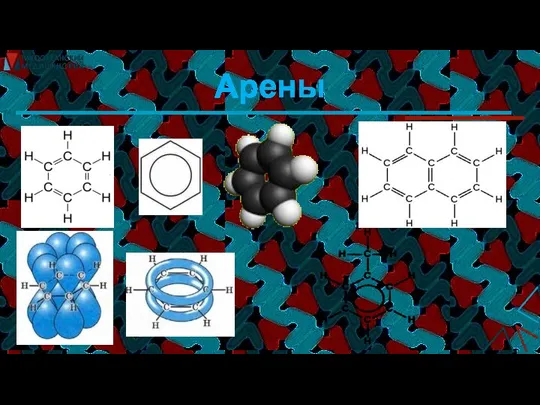
- 30. Арены
- 31. Основной тип реакции для аренов – SЕ (sp2 - гибридизованные атомы углерода), реагенты галогены Hal2 (Cl2
- 32. Реакции электрофильного замещения (SE) Атакующая частица — электрофил (положительно заряженная частица или частица с дефицитом ē).
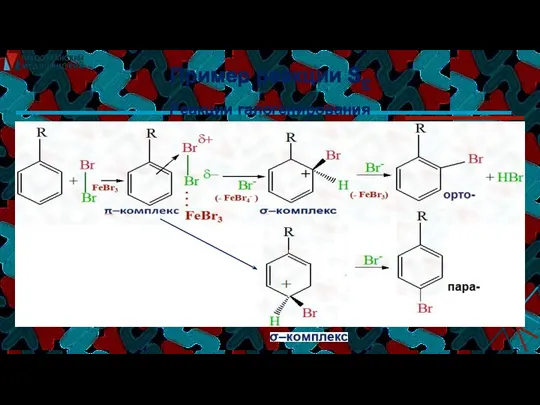
- 33. Пример реакции SE Реакции галогенирования
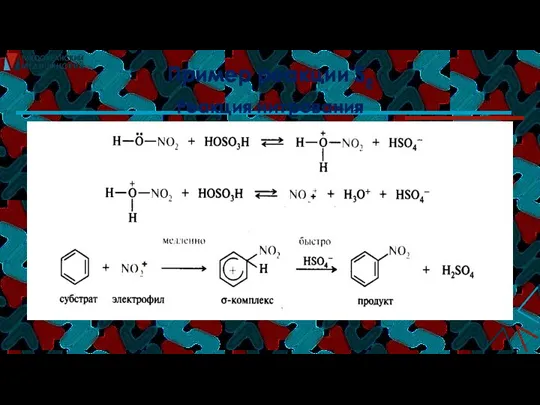
- 34. Пример реакции SE Реакция нитрования
- 35. Ориентирующее действие заместителя По ориентирующему и активирующему/дезактивирующему действию заместители можно разделить на 3 группы: Ориентанты первого
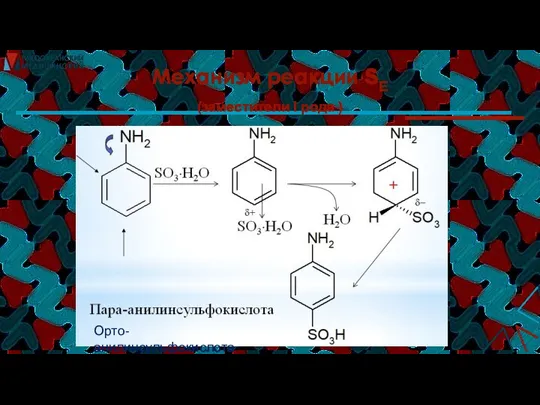
- 36. Механизм реакции SE (заместители I рода ) SE Орто-анилинсульфокислота
- 37. Пример реакции SE
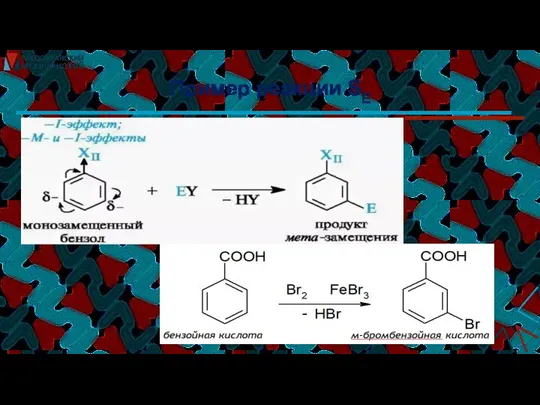
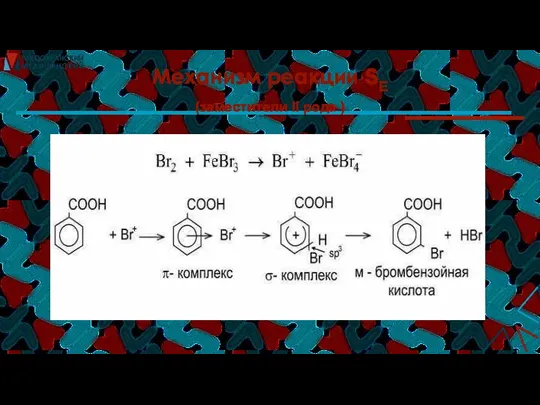
- 38. Механизм реакции SE (заместители II рода )
- 39. *Биологическая роль SE * Биосинтез ароматических гормонов и аминокислот. * Синтезы лекарственных препаратов: сульфаниламидов, салицилатов, антисептиков,
- 41. Скачать презентацию





























 Выращивание кристаллов
Выращивание кристаллов Презентация на тему Химические синонимы
Презентация на тему Химические синонимы  5 группа элементов
5 группа элементов Horľaviny. Horľavá látka
Horľaviny. Horľavá látka Презентация на тему Роль йода в организме
Презентация на тему Роль йода в организме 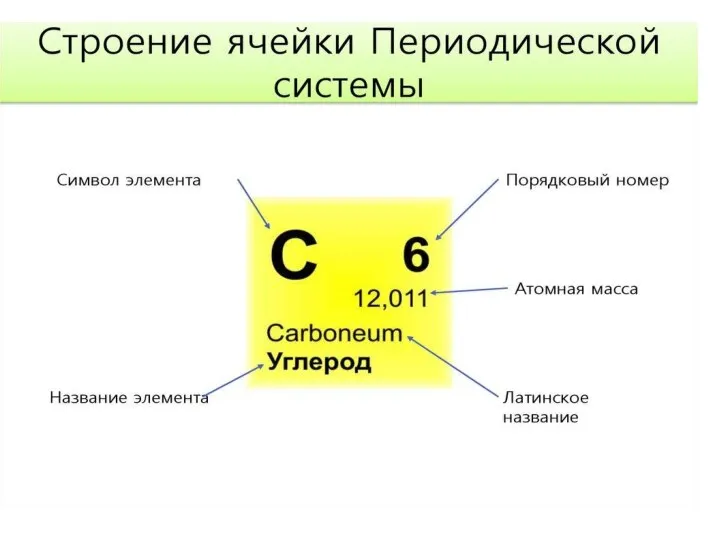 Строение ячейки периодической системы Менделеева
Строение ячейки периодической системы Менделеева Соли. Состав солей
Соли. Состав солей Разбор ДЗ. Титрование – общие моменты
Разбор ДЗ. Титрование – общие моменты Закон сохранения массы веществ. Уравнения химических реакций.
Закон сохранения массы веществ. Уравнения химических реакций. Комплексные соединения
Комплексные соединения Относительная атомная и молекулярная масса
Относительная атомная и молекулярная масса Алкены
Алкены Алюминий
Алюминий Теория электролитической диссоциации
Теория электролитической диссоциации Фотометрический анализ
Фотометрический анализ Углеродные материалы. Основные понятия и определения. Области их применения
Углеродные материалы. Основные понятия и определения. Области их применения Презентация на тему Строение атома и атомного ядра
Презентация на тему Строение атома и атомного ядра  Температурная зависимость скорости химической реакции
Температурная зависимость скорости химической реакции Драгоценные камни
Драгоценные камни Объёмный анализ
Объёмный анализ Непредельные углеводороды
Непредельные углеводороды Сера
Сера Оксиды. Классификация оксидов
Оксиды. Классификация оксидов Химия металлов. Влияние металлов на организм человека
Химия металлов. Влияние металлов на организм человека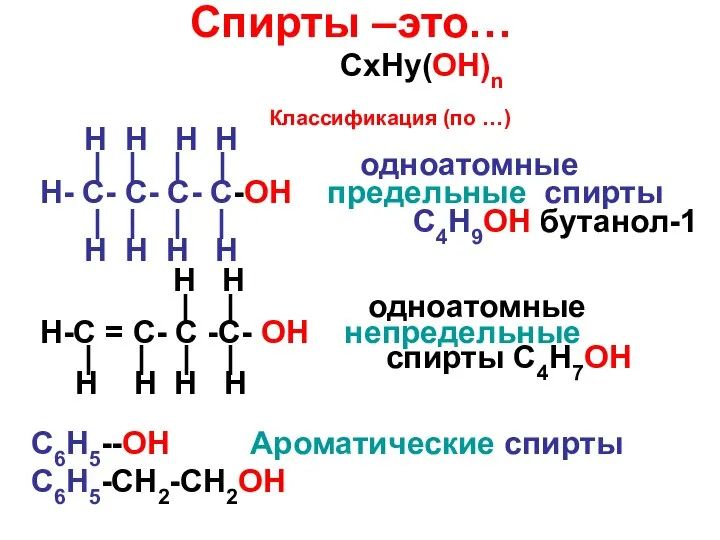 Спирты –это…
Спирты –это… Алюминийорганические соединения
Алюминийорганические соединения Презентация на тему Алмазы Индии
Презентация на тему Алмазы Индии  Химическая связь
Химическая связь