Слайд 2Цель работы
Рассмотреть работу ГЭ и объяснить
возникновение ГЭ при коррозии
контактных пар

металлов.
Слайд 3Теоретическое обоснование
Коррозия – самопроизвольный процесс
разрушения металла, вызываемого его
окислением.
Коррозия –

это взаимодействие металлов
с окружающей средой
Меt - nе- = Меtn+,
которое приводит к изменению свойств
материала. Процесс этот необратимый.
Слайд 4Электрохимическая коррозия
Большая часть коррозионных процессов
относится к электрохимическим, которые
протекают с участием

электрохимических
ячеек, подобных гальваническим
элементам и называемых коррозионными
элементами.
Слайд 5Электрохимическая коррозия
Механизм электрохимической коррозии,
определяемый разностью потенциалов
- пассивных (катод)
среда (окислитель)

+ nе- = продукты
- и активных (анод)
Меt - nе- = Меtn+
участков,
и сводится к работе гальванического
элемента.
Слайд 6Электрохимическая коррозия
Часто роль окислителя играет вода,
растворённый в воде кислород или, в

некоторых случаях, ионы водорода Н+
2 Н2О + 2 ē = Н2 + 2 -ОН,
О2+ 2 Н2О + 4 ē = 4 -ОН ,
2Н+ + 2 ē = Н2↑.
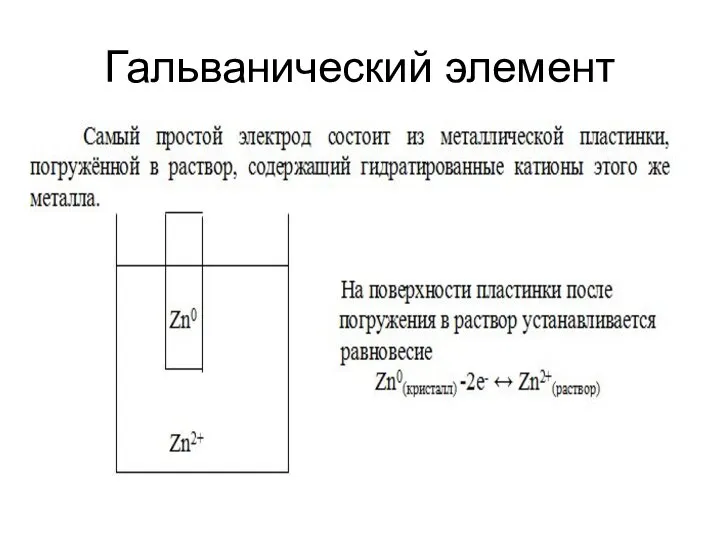
Слайд 8Гальванический элемент
В результате процесса окисления (прямой процесс) на пластинке появляется отрицательный

заряд, который увеличивается и к моменту равновесия становится величиной постоянной, выраженной как электрический потенциал (φ).
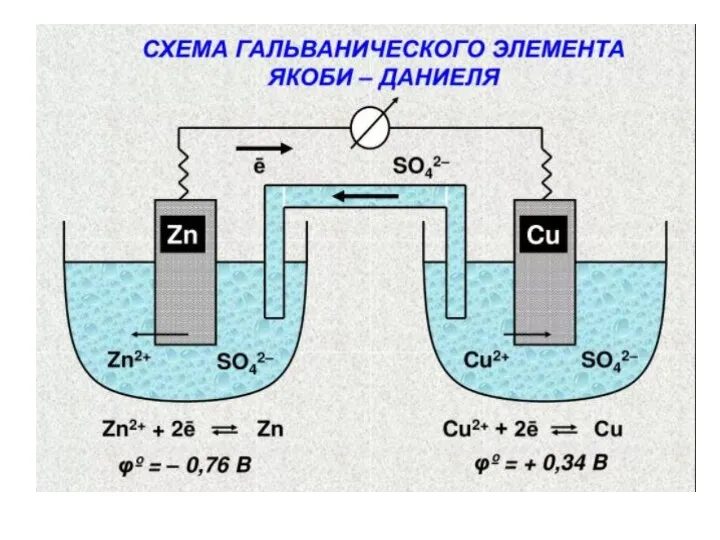
Слайд 9Гальванический элемент
ОВР может служить источником электрической энергии,
если она протекает в соответствующем

приборе –
гальваническом элементе, в котором реакция
окисления физически отделена от реакции
восстановления, а перенос электронов осуществляется
по внешней электрической цепи. Для того, чтобы цепь
была замкнута, используют «солевой мостик» -
внутренняя цепь, по которой осуществляется ионная
проводимость.
Гальванические элементы обычно обозначают
так
Zn0/Zn2+ // Сu2+/Сu0
Слайд 11Гальванический элемент
При работе гальванических элементов система с более высоким значением электродного

потенциала выступает в качестве окислителя (катод), а с более низким – восстановителя (анод).
Слайд 12Ход работы
Опыт 1. Гальванический элемент
Составляем схему ГЭ, записываем
уравнения электродных реакций и

общее
уравнение процесса.
Записываем вывод.
Слайд 13Опыт 2.
Возникновение ГЭ при контакте
металлов, находящихся в кислой среде.
https://yadi.sk/i/DQ1SoUYFvWx56w
Приготовить разбавленный

раствор серной кислоты.
Внести в пробирку с раствором цинковую гранулу.
Дождаться момента, когда гранула покроется
пузырьками газа. Внести в пробирку медную проволоку
и прикоснуться проволокой к поверхности гранулы
цинка. Отметить наблюдения.
Слайд 14Опыт 2.
Записать уравнения электродных
реакций. И общее уравнение реакции.
Составить схему гальванического

элемента.
Слайд 15Опыт 3
Электрохимическая коррозия.
https://yadi.sk/i/el52ujUWsL5dUQ
В разбавленные растворы серной
кислоты объёмом 2-3 мл добавить 1-2

раствора гексационоферрата (III) калия и
в каждую внести контактную пару
металлов Fe/Cu и Fe/Zn. Отметить
наблюдения. Сделать выводы.
Слайд 16Опыт 3
Записать уравнения электродных
процессов и общие уравнения реакций.
Составить схемы гальванических

элементов.













 Коррозия металлов и борьба с ней. Лабораторная работа
Коррозия металлов и борьба с ней. Лабораторная работа Создание из таблицы Менделеева и растворимости мини-справочник - шпаргалку
Создание из таблицы Менделеева и растворимости мини-справочник - шпаргалку Образование растворов ВМС
Образование растворов ВМС Комментарии к выполненным заданиям по темам Алканы и Алкены. 9 класс
Комментарии к выполненным заданиям по темам Алканы и Алкены. 9 класс Свойства растворов и их взаимодействие с газовой фазой
Свойства растворов и их взаимодействие с газовой фазой Plexiglas. Органическое стекло
Plexiglas. Органическое стекло Тайна алмазов
Тайна алмазов Степень окисления
Степень окисления Растворы. Типы растворов. Способы выражения концентрации растворов
Растворы. Типы растворов. Способы выражения концентрации растворов Непредельные углеводороды ряда этиленовых
Непредельные углеводороды ряда этиленовых Путешествие в мир кислот
Путешествие в мир кислот Prezentatsia_Microsoft_PowerPoint
Prezentatsia_Microsoft_PowerPoint Ферменттер.Ферменттердің құрылымы.Биохимиялық маңызы
Ферменттер.Ферменттердің құрылымы.Биохимиялық маңызы Кинетика и равновесие. Лекция №3
Кинетика и равновесие. Лекция №3 Строение металлов и их сплавов
Строение металлов и их сплавов По страницам истории российской химической науки
По страницам истории российской химической науки Химические реакции (игра)
Химические реакции (игра) Искусственные и синтетические полимеры
Искусственные и синтетические полимеры Реакции ионного обмена
Реакции ионного обмена Кремний. Германий, олово, свинец (Лекция № 6)
Кремний. Германий, олово, свинец (Лекция № 6) Получение гидроген хлорида
Получение гидроген хлорида Презентация на тему Хлороводород. Соляная кислота
Презентация на тему Хлороводород. Соляная кислота  Структура материалов
Структура материалов 175 – летию со дня рождения Дмитрия Ивановича Менделеева посвящается… АВТОР ПРЕЗЕНТАЦИИ: учитель химии МОУ СОШ №2 города Ртищево Саратовской области ПОПКОВА Е.Г.
175 – летию со дня рождения Дмитрия Ивановича Менделеева посвящается… АВТОР ПРЕЗЕНТАЦИИ: учитель химии МОУ СОШ №2 города Ртищево Саратовской области ПОПКОВА Е.Г. Непредельные углеводороды. Алкены
Непредельные углеводороды. Алкены Ионные уравнения реакций
Ионные уравнения реакций Соли, их классификация и свойства
Соли, их классификация и свойства Искусственные полимеры
Искусственные полимеры