Содержание
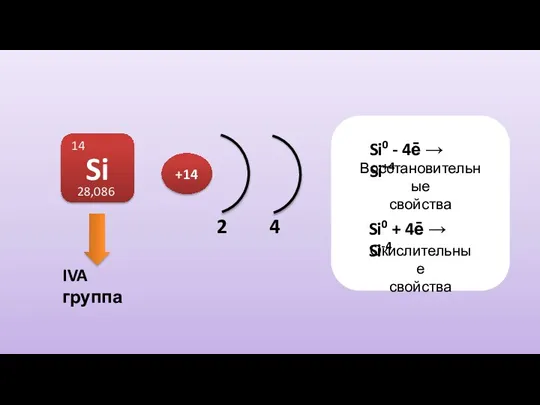
- 2. IVA группа Si 14 28,086 2 4 +14 Si0 - 4ē → Si+4 Восстановительные свойства Si0
- 3. SiO2 оксид кремния (IV) кремнезём горный хрусталь аметист агат топаз опал яшма халцедон сердолик
- 4. Природные силикаты – сложные вещества. Алюмосиликаты – силикаты, в состав которых входит алюминий. каолинит Al2O3 ·
- 5. Асбест используется для изготовления огнеупорных тканей.
- 6. Из разновидностей минералов на основе оксида кремния (IV) первобытные люди изготавливали орудия труда.
- 7. Оксид кремния (IV) у растений и животных
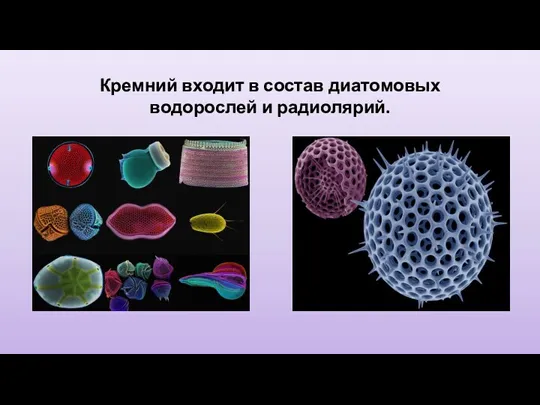
- 8. Кремний входит в состав диатомовых водорослей и радиолярий.
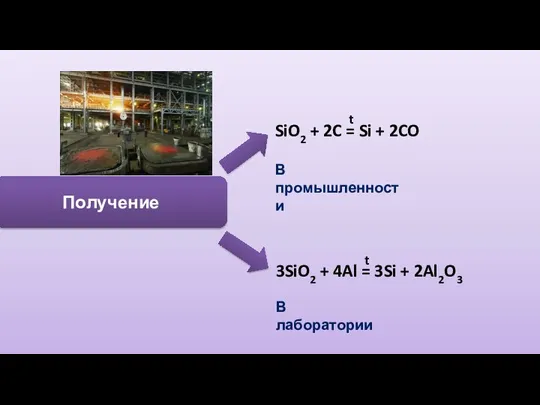
- 9. Получение SiO2 + 2C = Si + 2CO t 3SiO2 + 4Al = 3Si + 2Al2O3
- 10. Аллотропные модификации кремния Это бурый порошок. Аморфный кремний Твёрдое вещество тёмно-серого цвета с металлическим блеском. Он
- 11. Кремний является полупроводником. С повышением температуры его электропроводность увеличивается.
- 12. Реакция с кислородом Химические свойства кремния Si + O2 = SiO2 t оксид кремния (IV) 0
- 13. Реакции с металлами Химические свойства кремния t силицид магния 0 0 +2 -4 Реакция силицида с
- 14. Горение силана SiH4 + 2O2 = SiO2 + 2H2O t оксид кремния (IV) вода Реакция кремния
- 15. Получение кремния SiO2 + 2Mg = 2MgO + Si t SiO2 + 2С = Si +
- 17. Скачать презентацию











 Химические реакции в органической химии
Химические реакции в органической химии Графический диктант. Азот и Аммиак
Графический диктант. Азот и Аммиак Неньютоновская жидкость
Неньютоновская жидкость Язык естествознания. Химия
Язык естествознания. Химия Презентация на тему Химия и сельское хозяйство Пестициды
Презентация на тему Химия и сельское хозяйство Пестициды  Экстракция молибдена из азотнокислых растворов карбамоилметилфосфиноксидом, растворенным в высших спиртах
Экстракция молибдена из азотнокислых растворов карбамоилметилфосфиноксидом, растворенным в высших спиртах 12 принципов зелёной химии
12 принципов зелёной химии Алканы
Алканы Химическая связь. Строение вещества
Химическая связь. Строение вещества Диены. Понятие о диенах
Диены. Понятие о диенах Минералы и горные породы
Минералы и горные породы Типы химических реакций. 8 класс
Типы химических реакций. 8 класс Кварцевые пески
Кварцевые пески Вода как хладагент (R718)
Вода как хладагент (R718) Кроссворд по теме Металлы
Кроссворд по теме Металлы Оксиды
Оксиды Фосфорная кислота и ее свойства
Фосфорная кислота и ее свойства Щелочные металлы
Щелочные металлы Органическая химия
Органическая химия Периодическая система химических элементов. Периоды. Группы
Периодическая система химических элементов. Периоды. Группы Углерод 9 класс Подготовила учитель химии СШ№16 Самойлова Регина Львовна
Углерод 9 класс Подготовила учитель химии СШ№16 Самойлова Регина Львовна Кислород – основа жизни?
Кислород – основа жизни? Урок-путешествие по теме «Первоначальные химические понятия»
Урок-путешествие по теме «Первоначальные химические понятия» Метод высокоэффективной жидкостной хроматографии и тандемной масс-спектрометрии
Метод высокоэффективной жидкостной хроматографии и тандемной масс-спектрометрии Введение в органическую химию. Состав и структура органических веществ
Введение в органическую химию. Состав и структура органических веществ Многоатомные спирты
Многоатомные спирты Строение атома. Планетарная модель атома Резерфорда
Строение атома. Планетарная модель атома Резерфорда Презентация по Химии "Химическая номенклатура и филология"
Презентация по Химии "Химическая номенклатура и филология"