Содержание
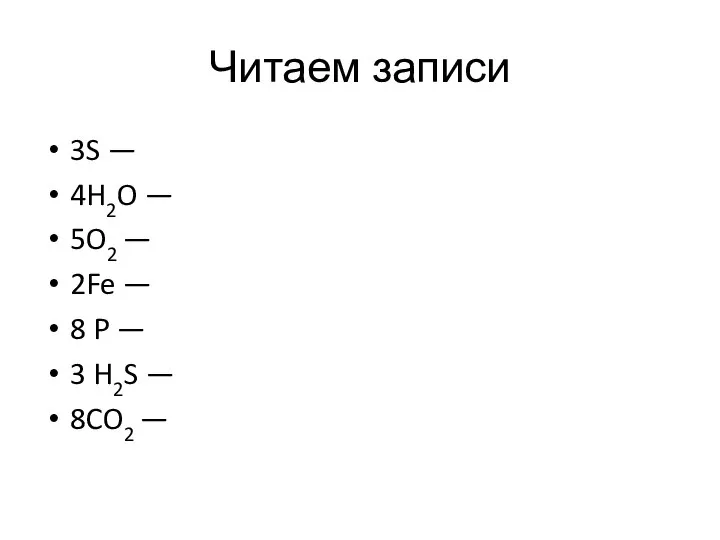
- 2. Читаем записи 3S — 4H2O — 5O2 — 2Fe — 8 P — 3 H2S —
- 3. Проверочная работа по теме «Относительная атомная масса»
- 4. 1. Запишите формулу Аш два эс о четыре Феррум хлор три Купрум цэ о три Литий
- 5. 2. Сколько простых и сложных веществ записаны формулами: Fe, NaNО3, S, О2, CuO, О3? 4 2
- 6. 3. Укажите формулы сложных веществ: 1)СuО; 2)Сu ; 3)СO2; 4)Н2 1 и 2 2 и 3
- 7. 4. Соотношение атомов серы и кислорода в молекуле сернистого газа равно 1:2. Найдите его формулу SO2
- 8. 5. Ar (относительная атомная масса) элемента фосфора равна 15 30 31 39
- 9. Что такое относительная молекулярная масса?
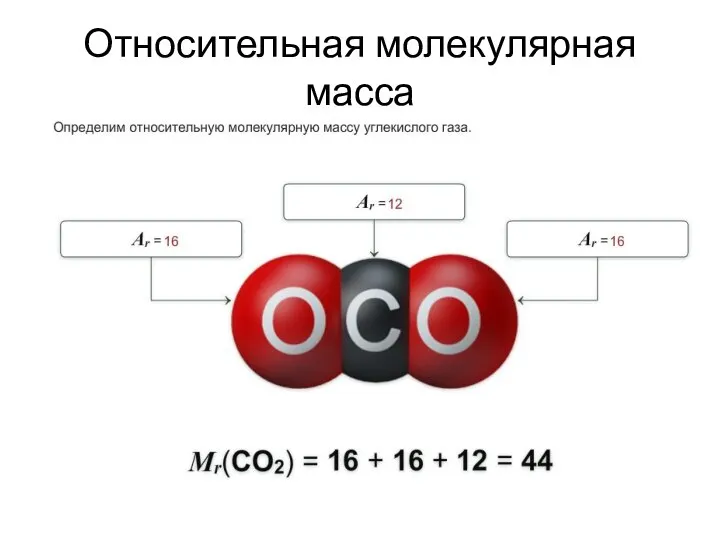
- 10. Относительная молекулярная масса
- 11. Относительная молекулярная масса
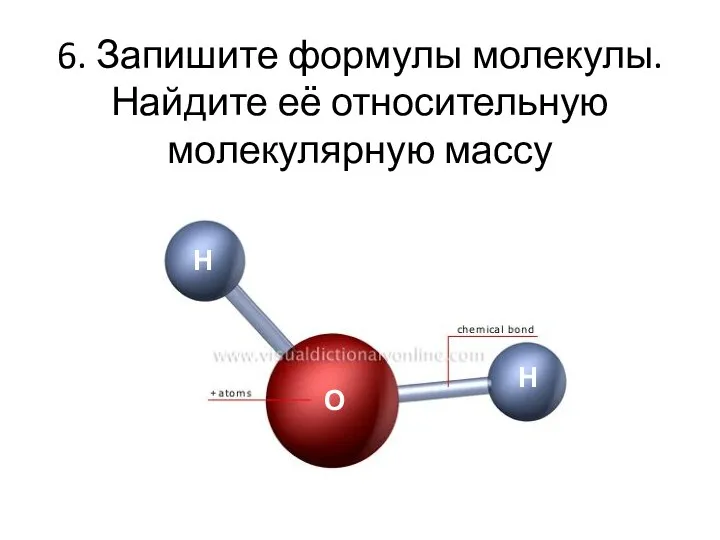
- 12. 6. Запишите формулы молекулы. Найдите её относительную молекулярную массу
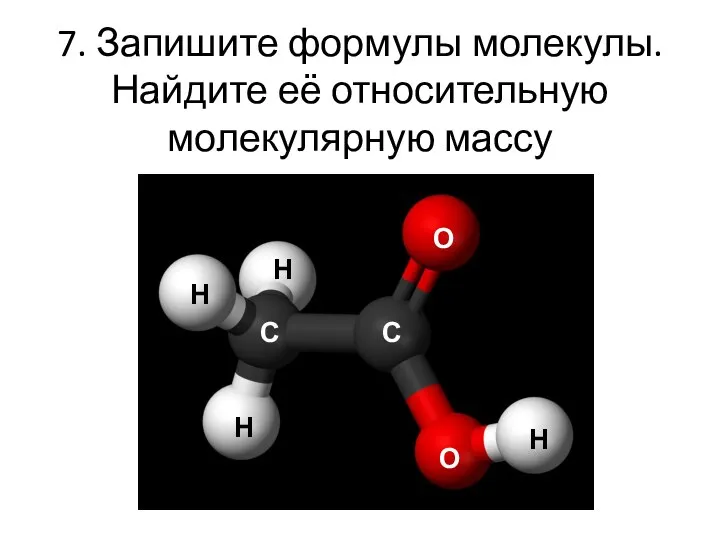
- 13. 7. Запишите формулы молекулы. Найдите её относительную молекулярную массу
- 14. Проверяем Ответы 1-H2SO4 2-FeCl3 3-CuCO3 4- LiOH 5- AlPO4 1 3 1 3 Mr (H2O) =
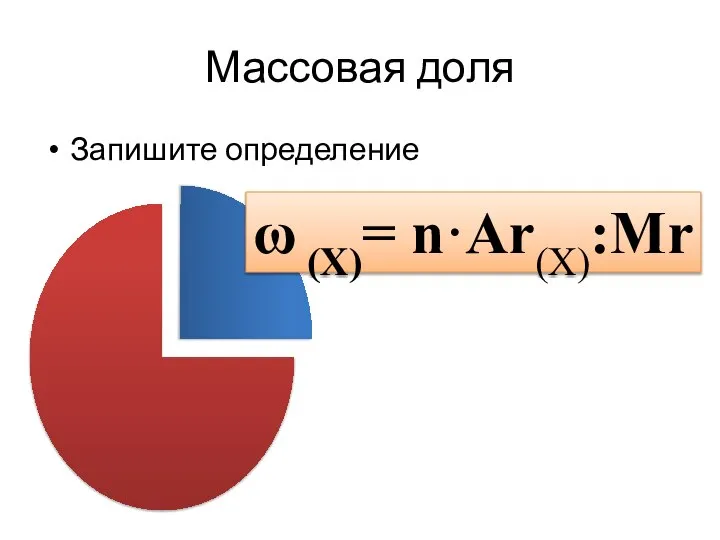
- 15. Массовая доля Запишите определение ω (X)= n·Ar(X):Mr
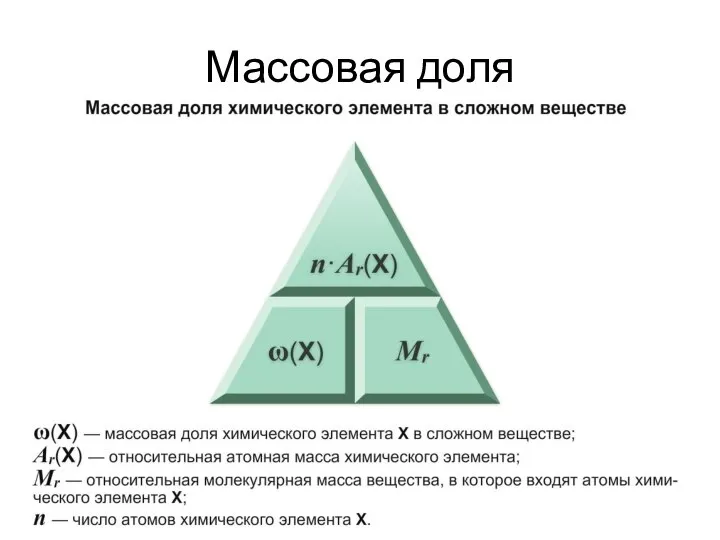
- 16. Массовая доля
- 17. Алгоритм расчета массовой доли элемента Рассчитать Mr (вещества); Аr (Э) умножить на индекс и разделить на
- 18. Например: Рассчитайте массовую долю кислорода в серной кислоте - H2SO4. Дано: Решение: H2SO4 Mr(H2SO4)=98 ω(О) =
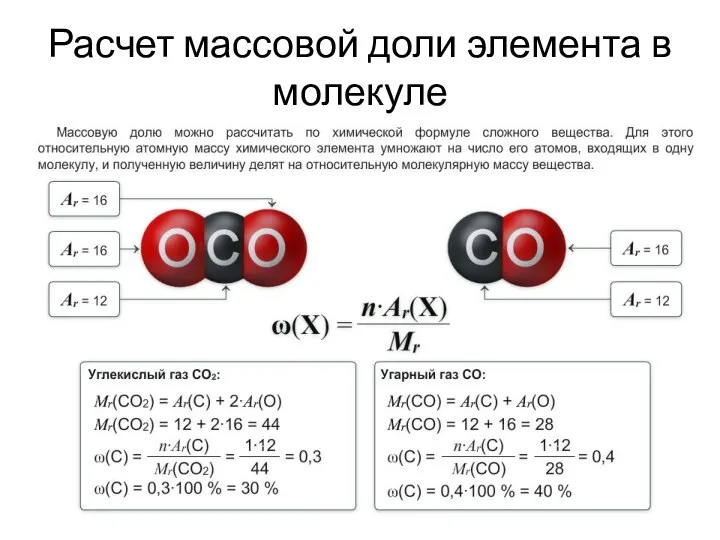
- 19. Расчет массовой доли элемента в молекуле
- 20. Решите расчетные задачи а) Вычислите массовую долю серы в сульфате натрия Na2SO4 б) Вычислите массовую долю
- 21. Решение а) Дано: Решение: Na2S04 Mr(Na2SО4)= 23 ∙ 2 +32 + 64= 142 ω(S) = x
- 22. б) Дано: Решение: Al I3 Mr (Al I3)= 27 + 127 ∙ 3 = 408 ω(l)
- 23. в) Дано: Решение: КСlOз Mr (КСlOз) = 39 + 35,5 + 16∙ 3 ω(Cl)= x %
- 25. Скачать презентацию















 20170625_otkrytyy_integrirovannyy_urok_himiya-geografiya
20170625_otkrytyy_integrirovannyy_urok_himiya-geografiya Лекция 1
Лекция 1 Теория химического строения органических веществ А.М. Бутлерова
Теория химического строения органических веществ А.М. Бутлерова Металлическая и водородная и химическая связь
Металлическая и водородная и химическая связь Бытовая химия
Бытовая химия Обсидиан
Обсидиан Предмет органической химии
Предмет органической химии Презентация на тему Выдающиеся русские ученые химики
Презентация на тему Выдающиеся русские ученые химики  Презентация на тему Оксиды углерода
Презентация на тему Оксиды углерода  Янтарь
Янтарь Нанокристаллические и аморфные металлы и сплавы
Нанокристаллические и аморфные металлы и сплавы Арены. Бензол
Арены. Бензол Азот N2
Азот N2 10_KISLOTNO_OSNOVNOE_TITROVANIE
10_KISLOTNO_OSNOVNOE_TITROVANIE Карбоновые кислоты
Карбоновые кислоты Известная и неизвестная вода
Известная и неизвестная вода Натрий, свойства атома, химические и физические свойства
Натрий, свойства атома, химические и физические свойства кислородосодерж. орг. соед. (1)
кислородосодерж. орг. соед. (1) Расчеты по уравнениям химических реакций
Расчеты по уравнениям химических реакций Стехиометрические законы химии
Стехиометрические законы химии Органическая химия: Жиры
Органическая химия: Жиры Классификация реакций. Теория-кинетика
Классификация реакций. Теория-кинетика Кислые горные породы
Кислые горные породы Соединения серы
Соединения серы Фотометрический анализ
Фотометрический анализ Создание из таблицы Менделеева и растворимости мини-справочник - шпаргалку
Создание из таблицы Менделеева и растворимости мини-справочник - шпаргалку Классификация аминокислот в зависимости от природы радикалов
Классификация аминокислот в зависимости от природы радикалов Конструкционные и специальные материалы холодильной техники
Конструкционные и специальные материалы холодильной техники