Содержание
- 2. Номенклатура порфиринов Применение порфиринов и их аналогов Порфирины в живых системах Синтез порфиринов Аналоги порфиринов Фотодинамическая
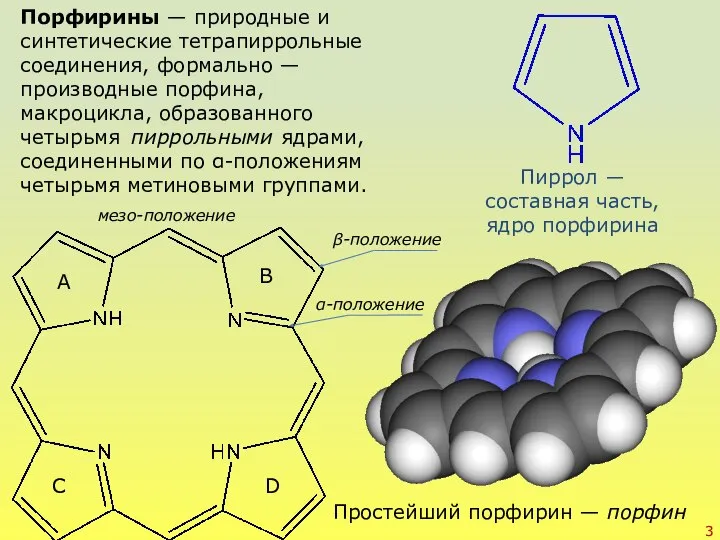
- 3. Порфирины — природные и синтетические тетрапиррольные соединения, формально — производные порфина, макроцикла, образованного четырьмя ядрами, соединенными
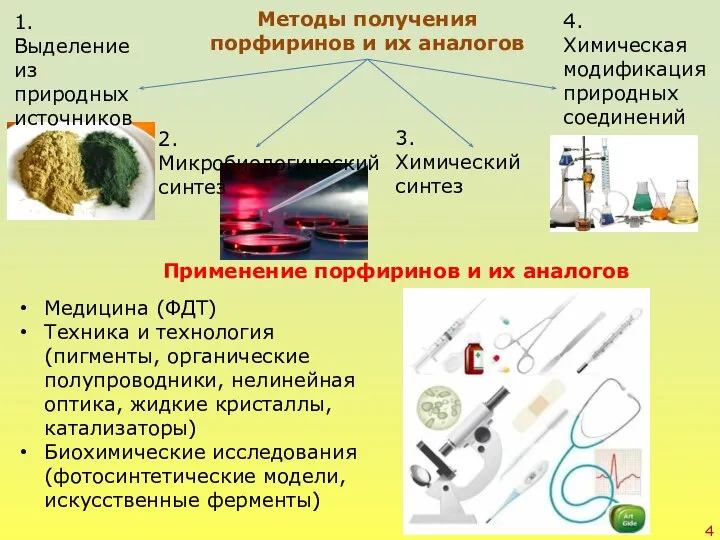
- 4. Методы получения порфиринов и их аналогов 1. Выделение из природных источников 2. Микробиологический синтез 3. Химический
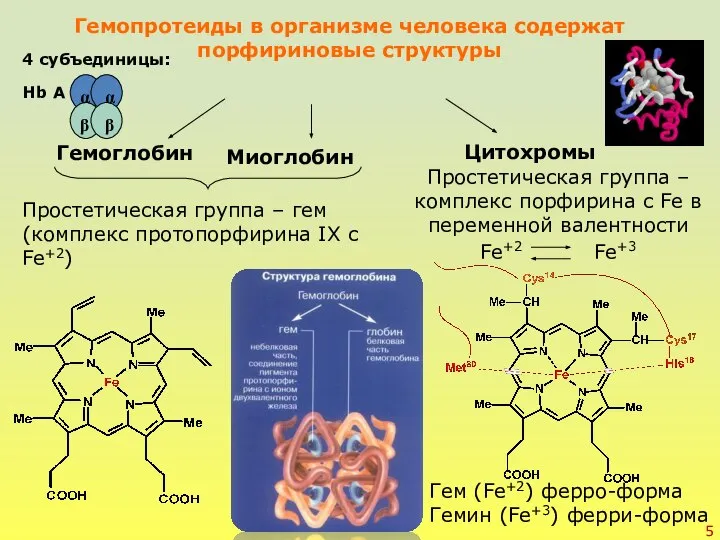
- 5. Гемопротеиды в организме человека содержат порфириновые структуры Простетическая группа – гем (комплекс протопорфирина IX с Fe+2)
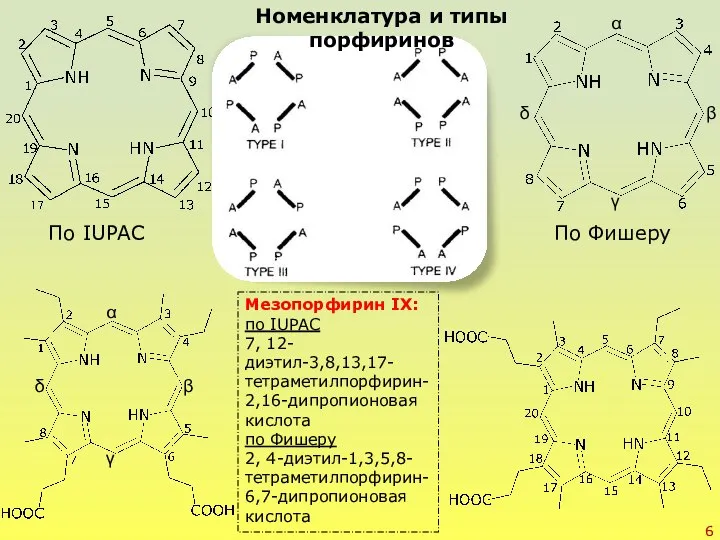
- 6. Номенклатура и типы порфиринов По Фишеру По IUPAC α β γ δ α β γ δ
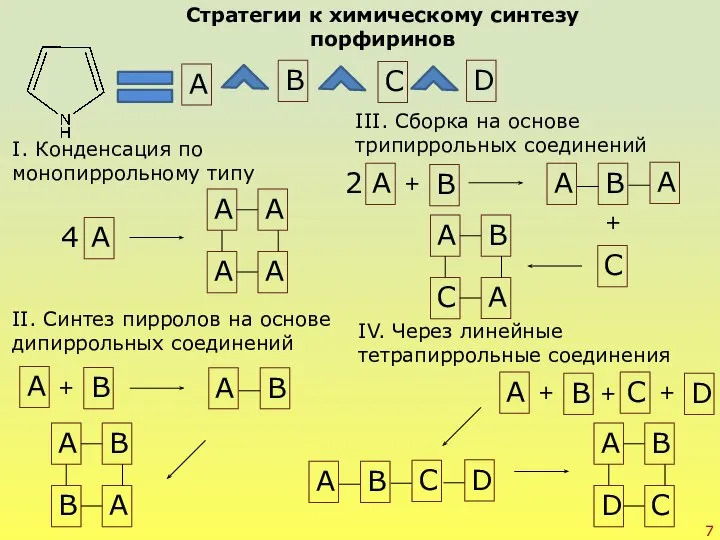
- 7. Стратегии к химическому синтезу порфиринов А B C D А 4 А А А А I.
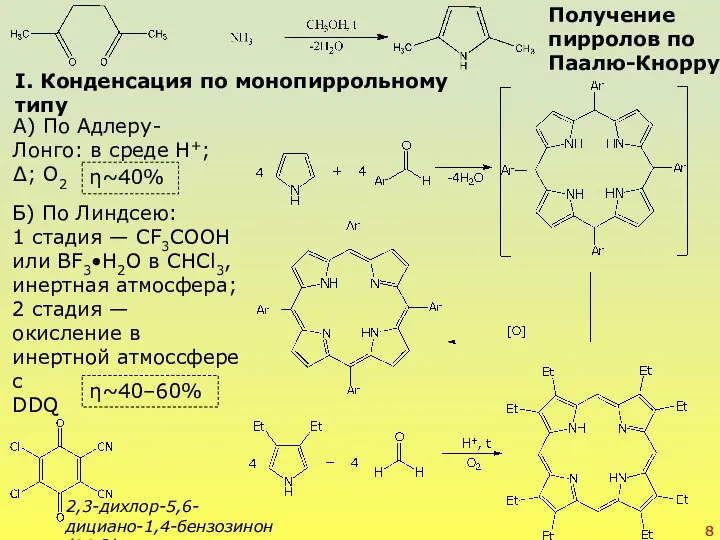
- 8. Получение пирролов по Паалю-Кнорру I. Конденсация по монопиррольному типу А) По Адлеру-Лонго: в среде H+; Δ;
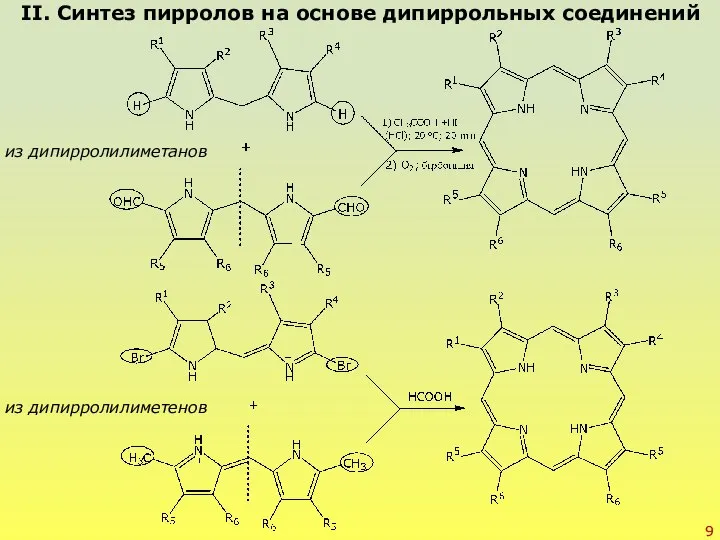
- 9. II. Синтез пирролов на основе дипиррольных соединений из дипирролилиметанов из дипирролилиметенов
- 10. III. Сборка на основе трипиррольных соединений Синтез из трипирранов по Сэсслеру (1987 г.) [3+1] 2
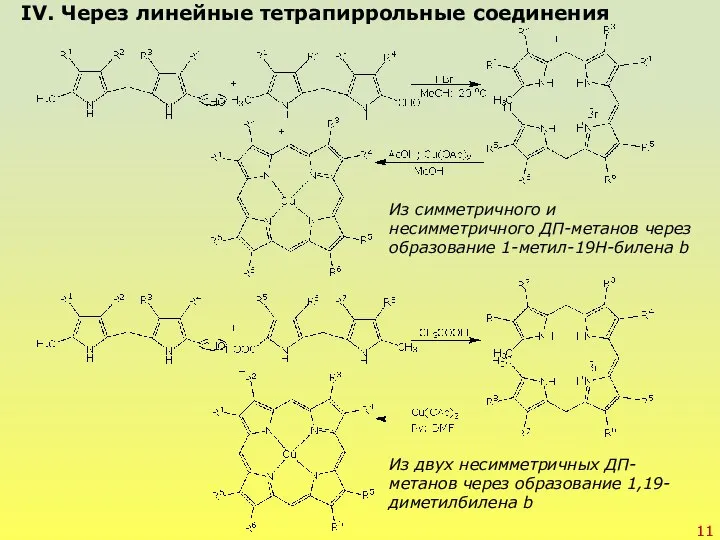
- 11. IV. Через линейные тетрапиррольные соединения Из симметричного и несимметричного ДП-метанов через образование 1-метил-19H-билена b Из двух
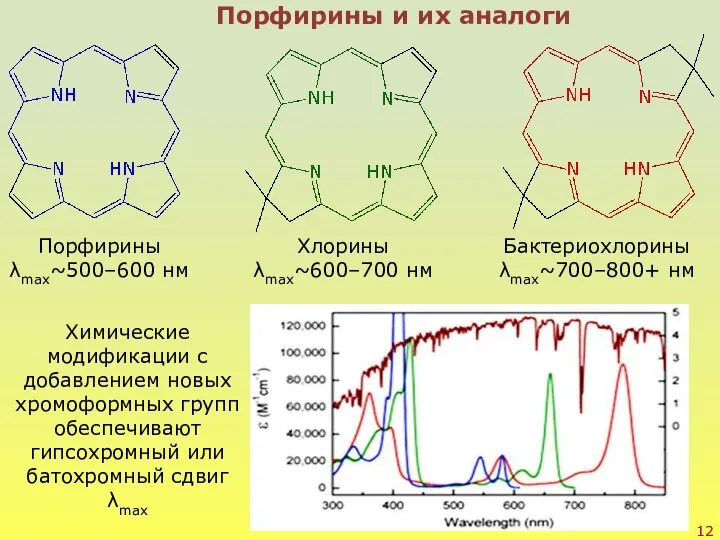
- 12. Порфирины и их аналоги Порфирины λmax~500–600 нм Хлорины λmax~600–700 нм Бактериохлорины λmax~700–800+ нм Химические модификации с
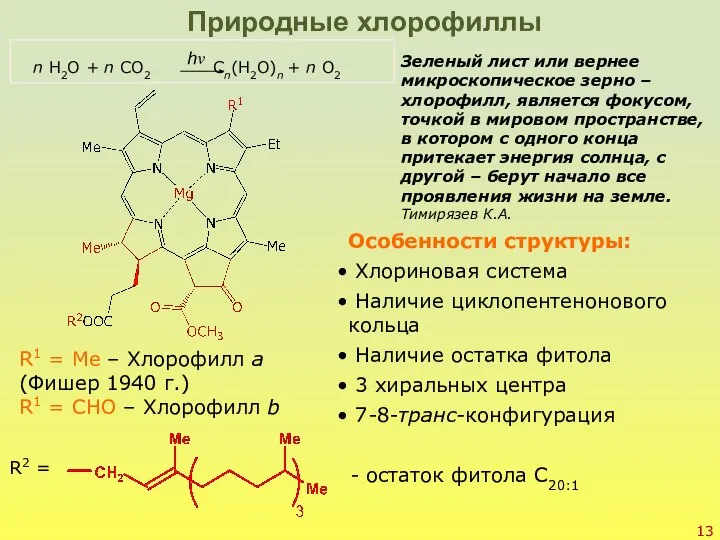
- 13. Природные хлорофиллы R1 = Me – Хлорофилл а (Фишер 1940 г.) R1 = CHO – Хлорофилл
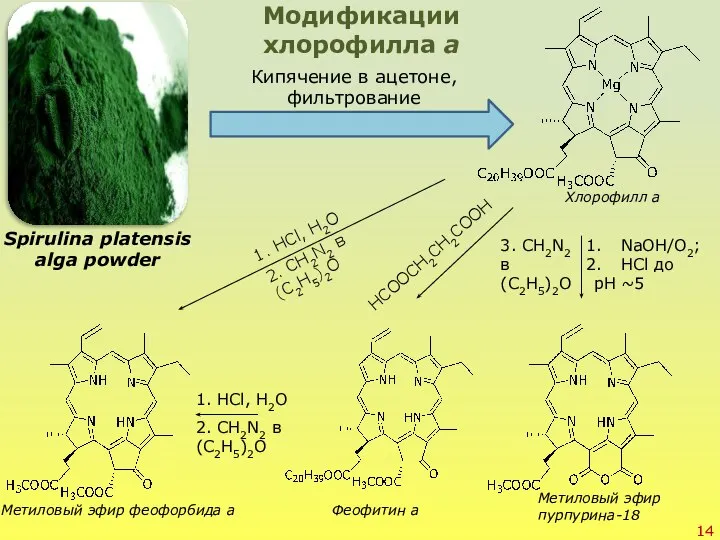
- 14. Spirulina platensis alga powder Кипячение в ацетоне, фильтрование Модификации хлорофилла а 1. HCl, H2O 2. CH2N2
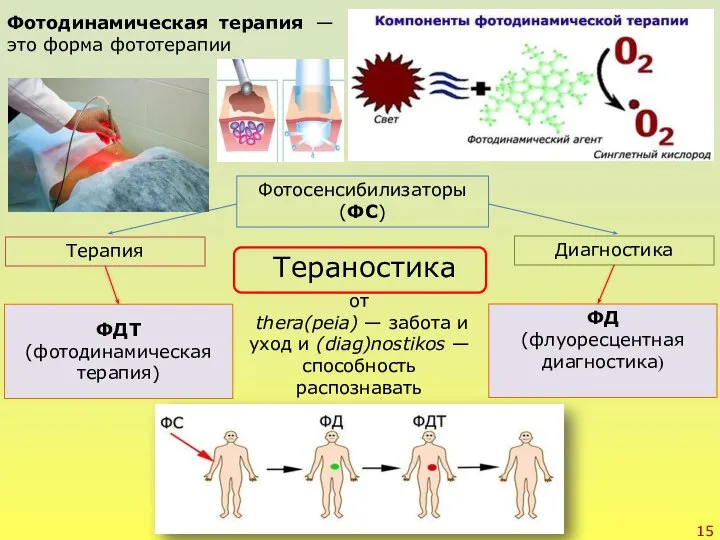
- 15. Фотосенсибилизаторы (ФС) Терапия Диагностика Тераностика ФДТ (фотодинамическая терапия) ФД (флуоресцентная диагностика) от thera(peia) — забота и
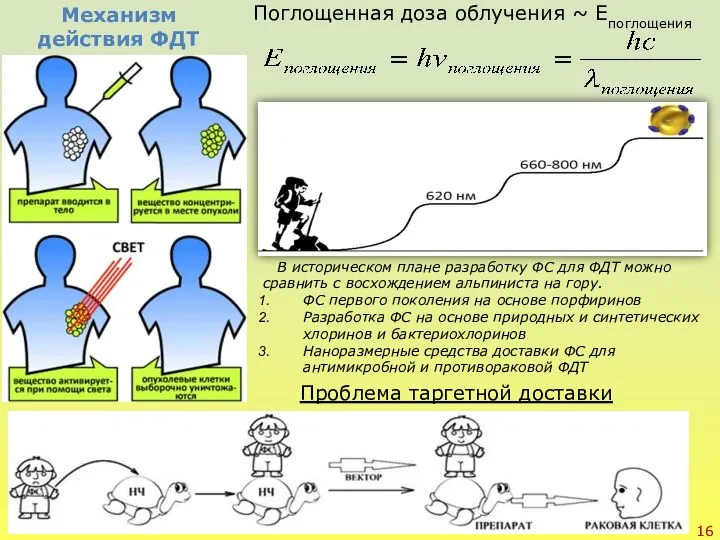
- 16. Проблема таргетной доставки Поглощенная доза облучения ~ Eпоглощения Механизм действия ФДТ В историческом плане разработку ФС
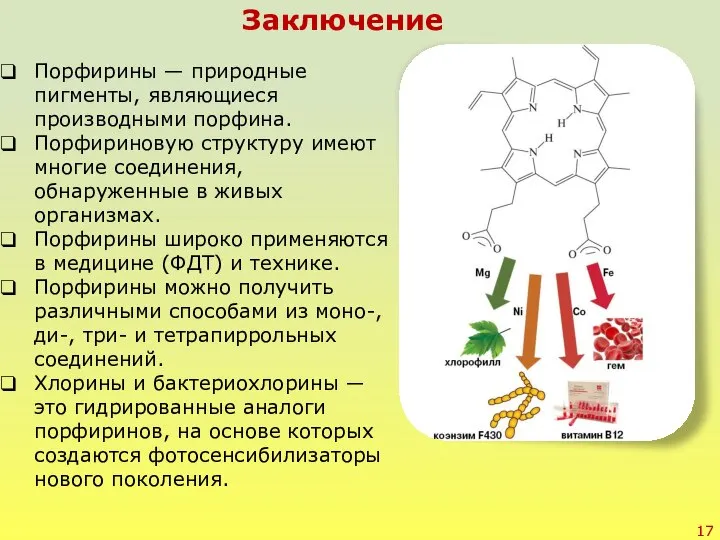
- 17. Заключение Порфирины — природные пигменты, являющиеся производными порфина. Порфириновую структуру имеют многие соединения, обнаруженные в живых
- 19. Скачать презентацию

![III. Сборка на основе трипиррольных соединений Синтез из трипирранов по Сэсслеру (1987 г.) [3+1] 2](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1132527/slide-9.jpg)
 Надмолекулярные структуры
Надмолекулярные структуры Углерод
Углерод Амины
Амины Витамины и их роль в жизни людей
Витамины и их роль в жизни людей Идеальная химическая лаборатория в школе
Идеальная химическая лаборатория в школе Классификация органических соединений. 10 класс
Классификация органических соединений. 10 класс Кремний и его соединения
Кремний и его соединения Мыло. Синтетические моющие средства
Мыло. Синтетические моющие средства Алкены
Алкены Сравнение свойств неорганических и органических веществ
Сравнение свойств неорганических и органических веществ Закалка без полиморфного превращения
Закалка без полиморфного превращения Неметаллические материалы
Неметаллические материалы Коллоидная химия
Коллоидная химия Применения химического анализа людьми в разных родах занятий
Применения химического анализа людьми в разных родах занятий Сплавы на основе магния и титана
Сплавы на основе магния и титана Приходченко ФЕР-2031
Приходченко ФЕР-2031 Бөлу процестерінің тиімділігін бағалау әдістерін таңдау және таңдау принциптері
Бөлу процестерінің тиімділігін бағалау әдістерін таңдау және таңдау принциптері Буферлік жүйелер мен ерітінділер туралы түсініктер, олардың құрамы және жіктелуі
Буферлік жүйелер мен ерітінділер туралы түсініктер, олардың құрамы және жіктелуі Физико-химические методы анализа. Лекция 4
Физико-химические методы анализа. Лекция 4 8-29 класс (1)
8-29 класс (1) Химия. Зачем она нужна? Дистанционный конкурс «Химия без лаборатории» Ученица 10 класса Климашина Василиса, ГОУСОШ № 464 – ЦАО, г. М
Химия. Зачем она нужна? Дистанционный конкурс «Химия без лаборатории» Ученица 10 класса Климашина Василиса, ГОУСОШ № 464 – ЦАО, г. М Экстракция и кристаллизация
Экстракция и кристаллизация Смолисто-асфальтеновые вещества
Смолисто-асфальтеновые вещества Homecredit Bank. Показатели и зоны роста
Homecredit Bank. Показатели и зоны роста Cиликат кальция
Cиликат кальция Альдегиды. Свойства альдегидов
Альдегиды. Свойства альдегидов Химическая коррозия
Химическая коррозия Химические структуры
Химические структуры