Слайд 2I. Строение молекул углекислого газа
Молекулы углекислого газа всегда состоят из двух атомов кислорода
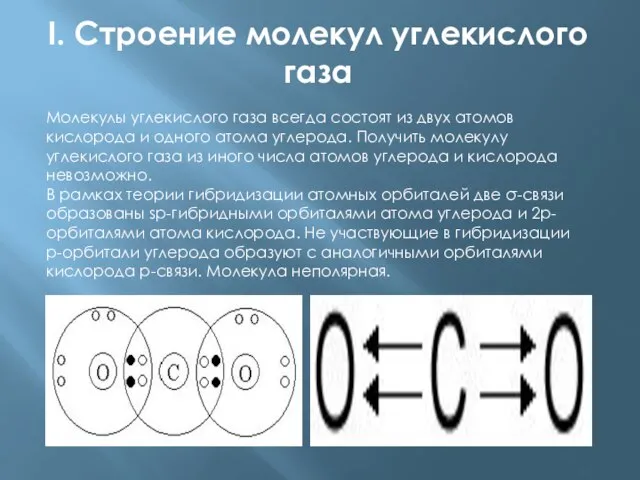
и одного атома углерода. Получить молекулу углекислого газа из иного числа атомов углерода и кислорода невозможно.
В рамках теории гибридизации атомных орбиталей две σ-связи образованы sp-гибридными орбиталями атома углерода и 2р-орбиталями атома кислорода. Не участвующие в гибридизации р-орбитали углерода образуют с аналогичными орбиталями кислорода p-связи. Молекула неполярная.
Слайд 3II.Открытие углекислого газа.
Углекислый газ был первым между всеми другими газами противопоставлен воздуху

под названием «дикий газ» алхимиком XVI века Вант Гельмонтом.
Открытием СО2 было положено начало новой отрасли химии – пневматохимии (химии газов).
Шотландский химик Джозеф Блэк (1728–1799) в 1754 году установил, что известковый минерал мрамор (карбонат кальция) при нагревании разлагается с выделением газа и образует негашеную известь (оксид кальция):
CaCO3CaO + CO2
Выделяющийся газ можно было вновь соединить с оксидом кальция и вновь получить карбонат кальция:
CaO + CO2CaCO3
Этот газ был идентичен открытому Ван Гельмонтом «дикому газу», но Блэк дал ему новое название – «связанный воздух» – так как этот газ можно было связать и вновь получить твердую субстанцию – карбонат кальция.
Несколько лет спустя Кавендиш обнаружил еще два характерных физических свойства углекислого газа – его высокую плотность и значительную растворимость в воде.
Слайд 4III. Физические свойства
Оксид углерода (IV) – углекислый газ, газ без цвета и

запаха, тяжелее воздуха, растворим в воде, при сильном охлаждении кристаллизуется в виде белой снегообразной массы – «сухого льда» . При атмосферном давлении он не плавится, а испаряется, температура сублимации -78 °С. Углекислый газ образуется при гниении и горении органических веществ. Содержится в воздухе и минеральных источниках, выделяется при дыхании животных и растений. Мало растворим в воде (1 объем углекислого газа в одном объеме воды при 15 °С) .
Слайд 5IV. Получение углекислого газа
Получение углекислого газа в промышленности:
Оксид углерода 2

горит в кислороде и на воздухе с выделением большого количества теплоты:
2СО+О2=2СО2
Таким же способом углекислый газ можно получать и в лаборатории.
Оксид углерода 2 является сильным восстановителем, поэтому в промышленности его используют для восстановления железных руд:
Fe2O3+3CO=2Fe+3CO2
В промышленности оксид углерода 4 получают при сжигании угля или при прокаливании известняка:
СаСО3=СаО+СО2
Получение углекислого газа в лаборатории:
В лаборатории СО2 получают действием кислот на соли угольной кислоты Н2СО3:
Na2CO3+H2SO4=Na2SO4+CO2+H2O
При действии кислот на карбонаты и их растворы происходит выделение диоксида углерода, вызывающего вспенивание раствора:
СаСО3+НCl=CaCl2+CO2+H2O
Слайд 6V. Распознание углекислого газа
Для обнаружения диоксида углерода можно провести следующую реакцию:
СаСО3+2HCl=CaCl2+CO2+H2O
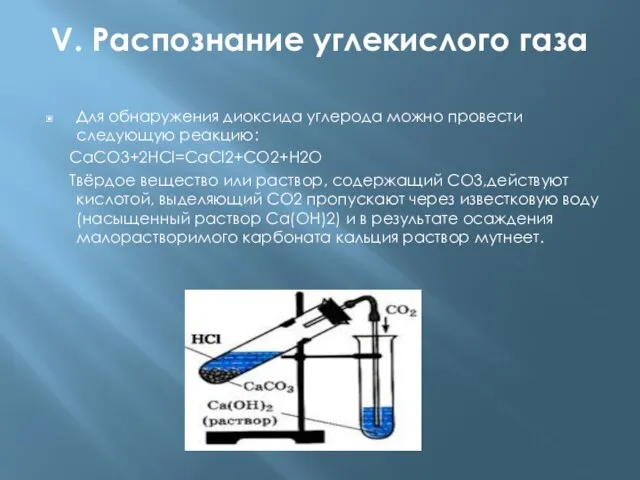
Твёрдое вещество или раствор, содержащий СО3,действуют кислотой, выделяющий СО2 пропускают через известковую воду (насыщенный раствор Са(ОН)2) и в результате осаждения малорастворимого карбоната кальция раствор мутнеет.
Слайд 7VI. Применение углекислого газа
Углекислый газ применяют во многих отраслях.
Например:
1.Химическая

отрасль;
2.Фармацевтика;
3.Пищевая отрасль;
4.Медицина;
5.Металлургическая отрасль;
6.Лабораторные исследования и анализ;
7.Целлюлозно-бумажная отрасль;
8.Электроника;
9.Охрана окружающей среды.
Слайд 8 VII. Нахождение в природе
Содержание углекислого газа в атмосфере относительно небольшое, около

0,03% (по объему). Углекислый газ, сосредоточенный в атмосфере, имеет массу 2200 биллионов тонн.
В 60 раз больше углекислого газа содержится в растворенном виде в морях и океанах.
В течение каждого года из атмосферы извлекается примерно 1/50 часть всего содержащегося в ней CO2 растительным покровом земного шара в процессе фотосинтеза, превращающего минеральные вещества в органические.
Основная масса углекислого газа в природе образуется в результате различных процессов разложения органических веществ. Углекислый газ выделяется при дыхании растений, животных, микроорганизмов. Непрерывно увеличивается количество углекислого газа, выделяемого различными производствами. Углекислый газ содержится в составе вулканических газов, выделяется он и из земли в вулканических местностях.
Вне земного шара оксид углерода (IV) обнаружен в атмосферах Марса и Венеры – планетах «земного типа».







 Ода стеклу и городу-герою Керчи
Ода стеклу и городу-герою Керчи Электролиз расплавов и растворов электролитов
Электролиз расплавов и растворов электролитов Азот. Физические свойства азота
Азот. Физические свойства азота Фуллерены (шары Бакминстера)
Фуллерены (шары Бакминстера) Многоатомные спирты
Многоатомные спирты Предельные углеводороды
Предельные углеводороды Гидролиз солей
Гидролиз солей Производство препарата Салициловая кислота, раствор для наружного применения спиртовой 2-х процентный
Производство препарата Салициловая кислота, раствор для наружного применения спиртовой 2-х процентный Свойства нефти
Свойства нефти Гидролиз солей
Гидролиз солей Аминокислоты. Химические и физические свойства
Аминокислоты. Химические и физические свойства Кристаллическое состояние воды - лёд
Кристаллическое состояние воды - лёд Презентация по Химии "Строение и физические свойства металлов"
Презентация по Химии "Строение и физические свойства металлов"  (+)-Plumisclerin A. Плюмисклин А
(+)-Plumisclerin A. Плюмисклин А Dereglarea metabolismului
Dereglarea metabolismului Наноматеріали. Тіт Лукрецій Кар
Наноматеріали. Тіт Лукрецій Кар Алкины, гомологический ряд алкинов. Электронное и пространственное строение алкинов на примере ацетилена (1)
Алкины, гомологический ряд алкинов. Электронное и пространственное строение алкинов на примере ацетилена (1) Презентация на тему Синтетические каучуки, строение, свойства, применение
Презентация на тему Синтетические каучуки, строение, свойства, применение  Гликоген. Синтез гликогена
Гликоген. Синтез гликогена Lektsia_4_Tochechnye_gruppy_simmetrii_Simvoly_Shenflisa
Lektsia_4_Tochechnye_gruppy_simmetrii_Simvoly_Shenflisa Классификация оганических соединений. 10 класс
Классификация оганических соединений. 10 класс ФБОУ- Раздольненская средняя общеобразовательная школа №19 Новосибирского района Новосибирской области
ФБОУ- Раздольненская средняя общеобразовательная школа №19 Новосибирского района Новосибирской области Значение углеводородов
Значение углеводородов Спирты
Спирты Наука ковала Победу. 1941-1945
Наука ковала Победу. 1941-1945 Презентация на тему Кристаллические решетки
Презентация на тему Кристаллические решетки  Опис технологічного процесу отримання смол бекелітових рідких марок
Опис технологічного процесу отримання смол бекелітових рідких марок Презентация на тему Жесткость воды
Презентация на тему Жесткость воды