Содержание
- 2. Строение и свойства атомов
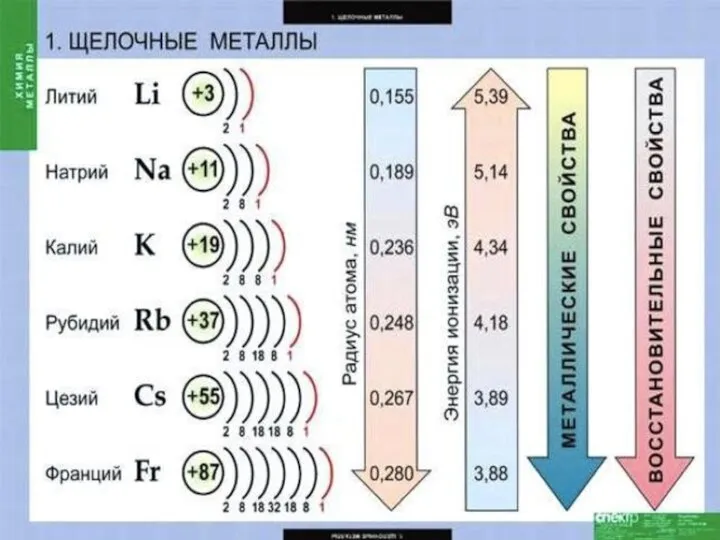
- 3. Щелочные металлы — это элементы главной подгруппы I группы : литий Li, натрий Nа, калий К,
- 5. На внешнем энергетическом уровне атомы этих элементов содержат по одному электрону, находящемуся на сравнительно большом удалении
- 6. Щелочные металлы - простые вещества
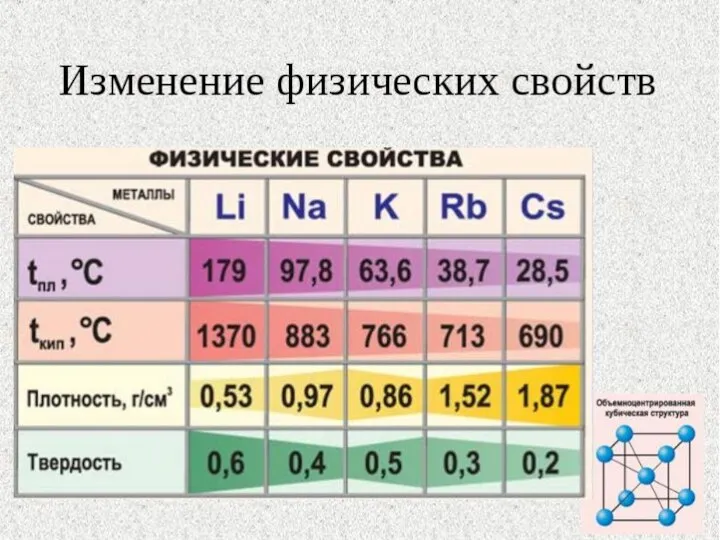
- 7. Серебристо-белые мягкие вещества (режутся ножом), с характерным блеском на свежесрезанной поверхности. Все они легкие и легкоплавкие,
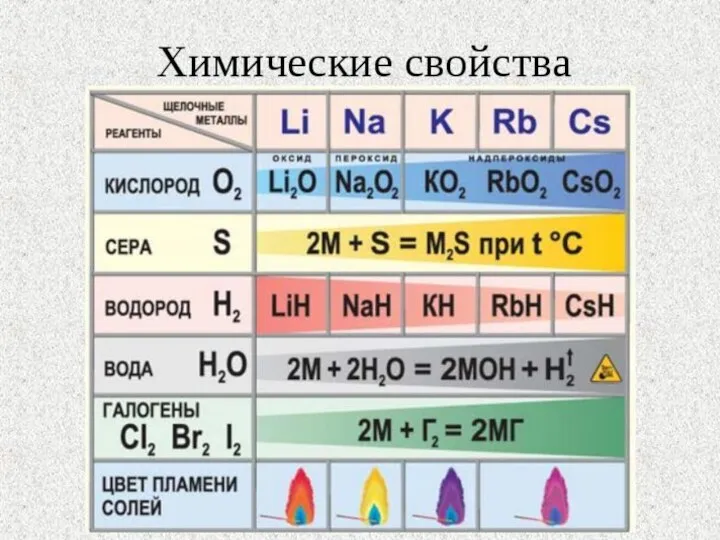
- 9. Химические свойства
- 10. Все щелочные металлы чрезвычайно активны, во всех химических реакциях проявляют восстановительные свойства, отдают свой единственный валентный
- 12. Взаимодействие с неметаллами
- 13. Щелочные металлы легко реагируют с кислородом, но каждый металл проявляет свою индивидуальность: оксид образует только литий:
- 14. Взаимодействие с водородом, серой, фосфором, углеродом, кремнием протекает при нагревании: с водородом образуются гидриды: 2Na +
- 15. С азотом легко реагирует только литий, реакция протекает при комнатной температуре с образованием нитрида лития: 6Li
- 16. Взаимодействие с водой
- 17. Все щелочные металлы реагируют с водой, литий реагирует спокойно, держась на поверхности воды, натрий часто воспламеняется,
- 18. Щелочные металлы способны реагировать с разбавленными кислотами с выделением водорода, однако реакция будет протекать неоднозначно, поскольку
- 19. Соединения щелочных металлов В свободном виде в природе щелочные металлы не встречаются из-за своей исключительно высокой
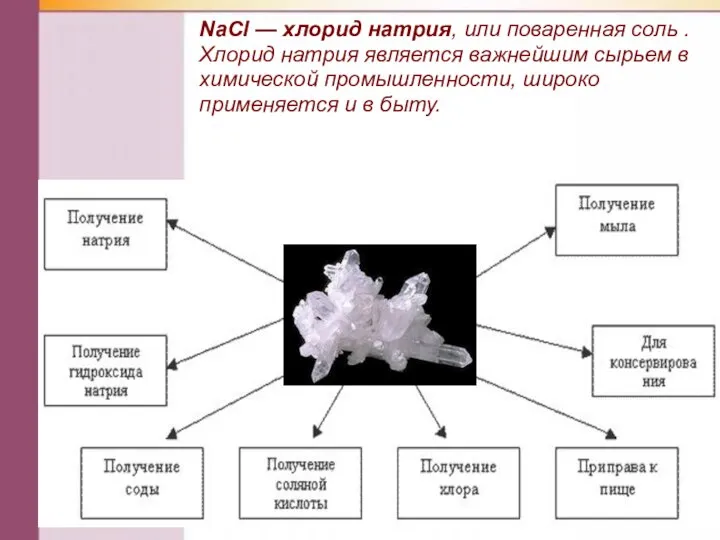
- 21. NаСl — хлорид натрия, или поваренная соль . Хлорид натрия является важнейшим сырьем в химической промышленности,
- 23. Скачать презентацию
















 Ароматерапия
Ароматерапия Фракционный состав нефти. Химический состав нефти
Фракционный состав нефти. Химический состав нефти Céramiques lesquelles choisi ?
Céramiques lesquelles choisi ? Арены. 10 класс
Арены. 10 класс Органическая химия. Введение
Органическая химия. Введение Технология получения полиуретанов
Технология получения полиуретанов Практико-ориентированные задачи по химии для студентов гуманитарных специальностей
Практико-ориентированные задачи по химии для студентов гуманитарных специальностей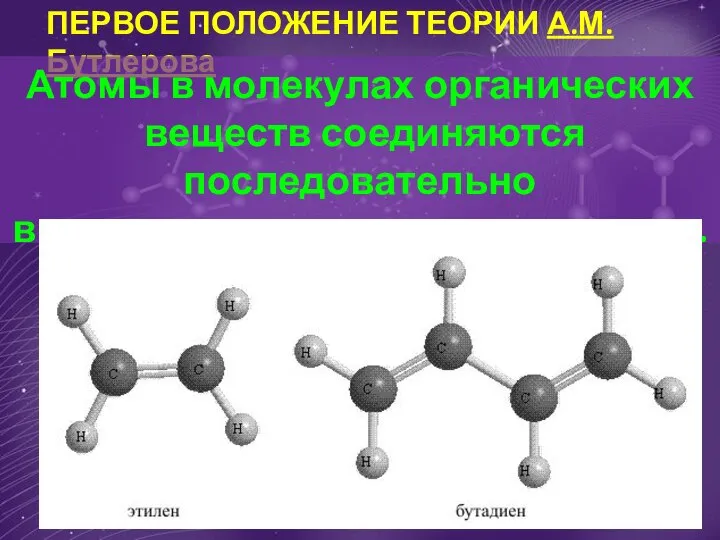 Первое положение теории А.М. Бутлерова Атомы в молекулах органических веществ соединяются последовательно
Первое положение теории А.М. Бутлерова Атомы в молекулах органических веществ соединяются последовательно Презентация на тему Бром
Презентация на тему Бром  Выращивание кристаллов соли и сахара в домашних условиях
Выращивание кристаллов соли и сахара в домашних условиях Презентация на тему Стронций
Презентация на тему Стронций  Алкены
Алкены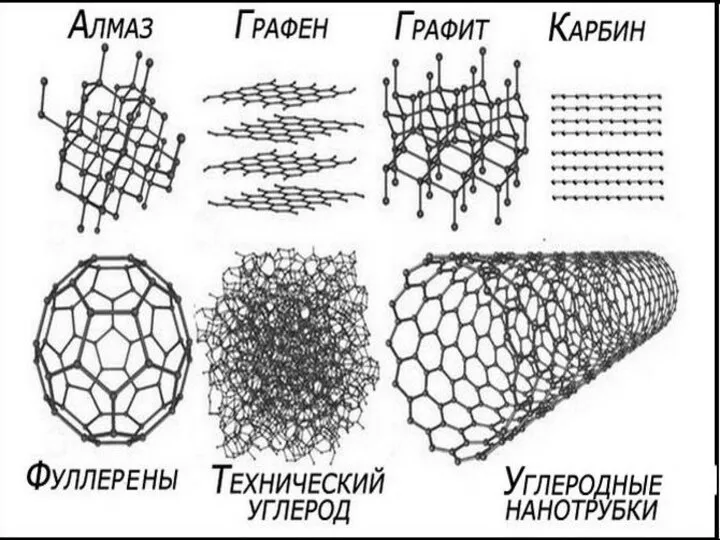 Углеродные нанотрубки
Углеродные нанотрубки Составление формул по валентности. Понятие
Составление формул по валентности. Понятие Положение металлов в периодической системе химических элементов
Положение металлов в периодической системе химических элементов Алканы
Алканы Учебное задание Расчет теплоты сгорания
Учебное задание Расчет теплоты сгорания Избыток, недостаток. Решение задач
Избыток, недостаток. Решение задач Кремний и его соединения
Кремний и его соединения Спирты и фенолы. (Лекция 6.1)
Спирты и фенолы. (Лекция 6.1) Валентность. Определение валентности элемента в оксиде
Валентность. Определение валентности элемента в оксиде Гемоглобин. Структура и свойства молекулы гемоглобина
Гемоглобин. Структура и свойства молекулы гемоглобина Какую воду мы пьем
Какую воду мы пьем Качественная реакция на многоатомные спирты
Качественная реакция на многоатомные спирты Олимпиада Ломоносов
Олимпиада Ломоносов Применение каучука
Применение каучука Презентация на тему Фолиевая кислота
Презентация на тему Фолиевая кислота  Химия в загадках
Химия в загадках