Содержание
- 2. Электролиты - вещества, диссоциирующие на ионы при взаимодействии с растворителем и сообщающие раствору способность проводить электрический
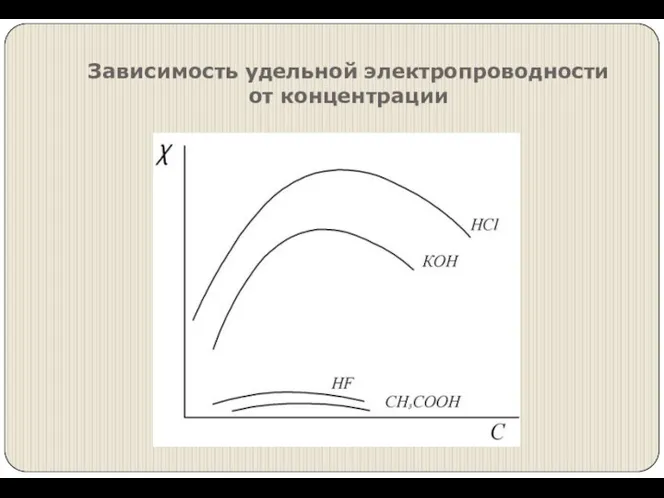
- 4. Зависимость удельной электропроводности от концентрации
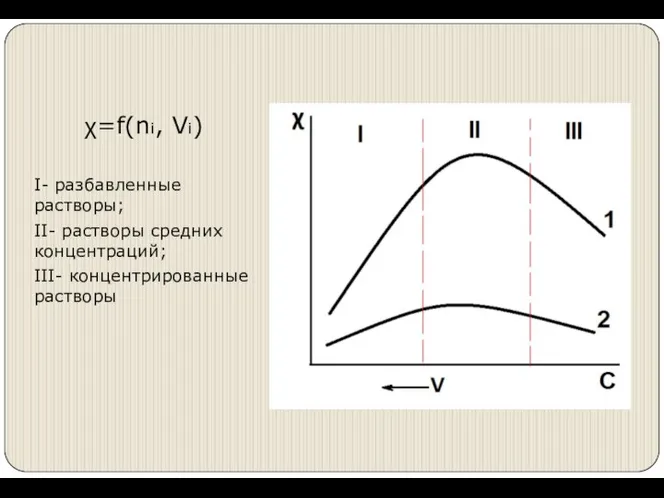
- 5. χ=f(ni, Vi) I- разбавленные растворы; II- растворы средних концентраций; III- концентрированные растворы
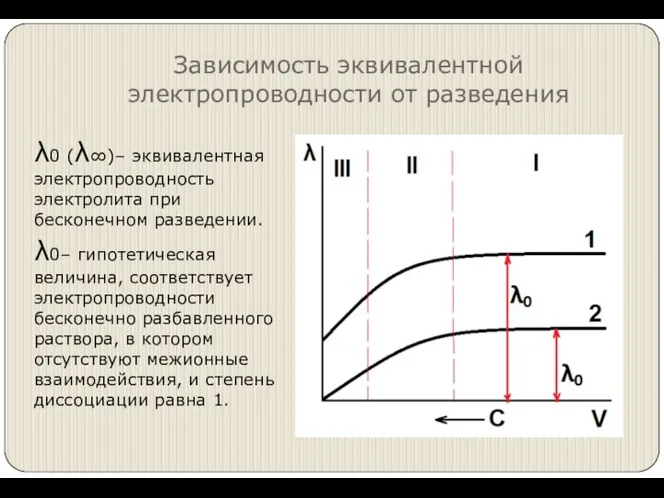
- 8. Зависимость эквивалентной электропроводности от разведения λ0 (λ∞)– эквивалентная электропроводность электролита при бесконечном разведении. λ0– гипотетическая величина,
- 10. При бесконечном разведении растворов кулоновские силы исчезают, величины ионных подвижностей стремятся к предельным значениям.
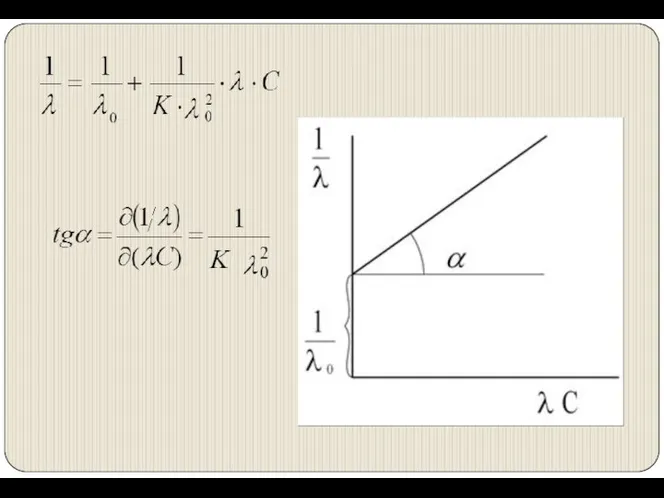
- 11. Зависимость электропроводности электролитов от концентрации при Т=const Разбавленные растворы сильных электролитов подчиняются закону Кольрауша: А –
- 12. Растворы слабых электролитов подчиняются закону разведения Оствальда.
- 15. Движение ионов в электрическом поле. Числа переноса ионов
- 19. Влияние природы электролита (иона и парного иона)
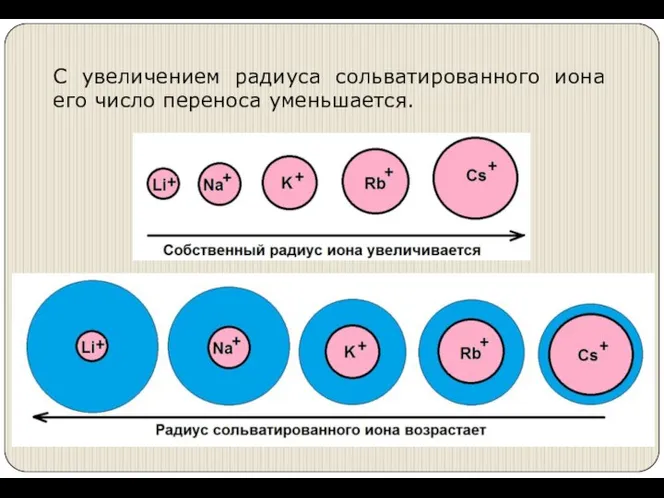
- 20. С увеличением радиуса сольватированного иона его число переноса уменьшается.
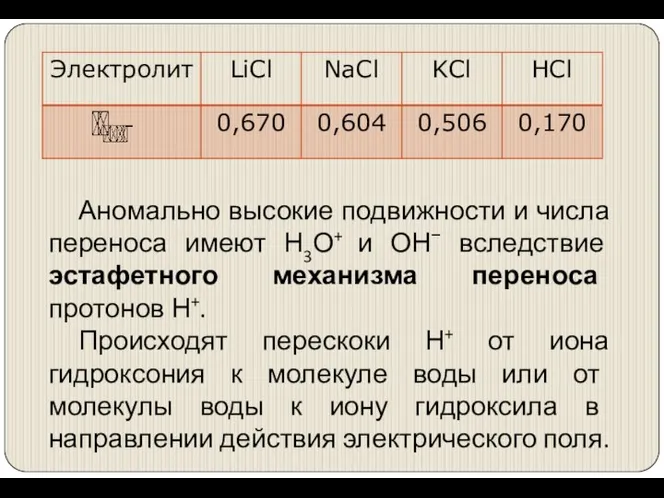
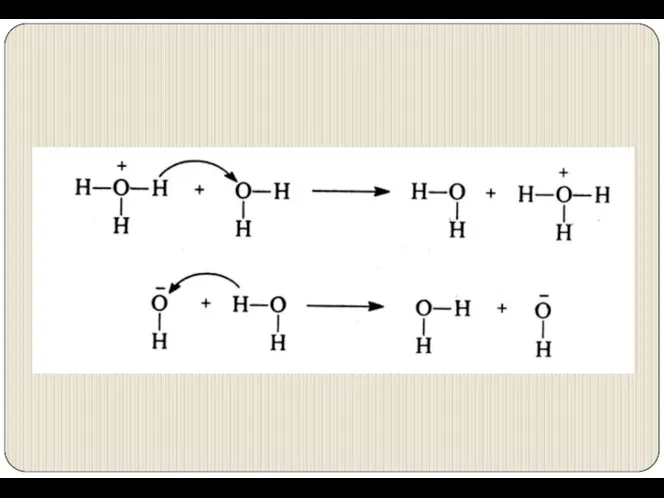
- 21. Аномально высокие подвижности и числа переноса имеют Н3О+ и ОН− вследствие эстафетного механизма переноса протонов Н+.
- 23. Влияние температуры. С ростом температуры снижается вязкость раствора; происходит десольватация ионов; числа переноса катиона и аниона
- 25. Скачать презентацию















 Химическая кинетика и равновесие
Химическая кинетика и равновесие Окислительно-восстановительные реакции, 9 класс
Окислительно-восстановительные реакции, 9 класс Твердые электролиты
Твердые электролиты Nanofibers of aluminum oxide
Nanofibers of aluminum oxide Введение в хроматографию. Хроматографические методы анализа
Введение в хроматографию. Хроматографические методы анализа Металлы
Металлы Составление формул оксидов, оснований, солей
Составление формул оксидов, оснований, солей 10 класс Алкадиены более совершенная (2)
10 класс Алкадиены более совершенная (2) Химическая связь
Химическая связь Презентация на тему Типы химических реакций (8 класс)
Презентация на тему Типы химических реакций (8 класс)  Экстракционное разделение радионуклидов
Экстракционное разделение радионуклидов Проточные реакторы непрерывного действия. (Лекция 5)
Проточные реакторы непрерывного действия. (Лекция 5) Алкены
Алкены Презентация на тему Альдегиды и их свойства
Презентация на тему Альдегиды и их свойства  Арены. Бензол
Арены. Бензол Изменения, происходящие с веществами
Изменения, происходящие с веществами Железо
Железо Диффузия и осмос
Диффузия и осмос Соли как производные кислот и оснований. Их состав и названия
Соли как производные кислот и оснований. Их состав и названия Занимательная химия Программу составил
Занимательная химия Программу составил  Строение атома
Строение атома Кислоты, их классификация и свойства
Кислоты, их классификация и свойства Соли. Классификация солей
Соли. Классификация солей Геохимический барьер
Геохимический барьер 5 Нефть. Нефтепереработка. Конверсия метана
5 Нефть. Нефтепереработка. Конверсия метана Ліпіди
Ліпіди Электролиз растворов и расплавов неорганических и органических электролитов
Электролиз растворов и расплавов неорганических и органических электролитов Строение и номенклатура карбонильных соединений
Строение и номенклатура карбонильных соединений