Слайд 2Системные васкулиты
это группа иммуновоспалительных заболеваний,
в основе патогенеза которых лежит иммуноопосредованное воспаление

стенок кровеносных сосудов
с развитием ишемических изменений в органах и тканях, кровоснабжаемых соответствующими сосудами.
Слайд 3Этиология
Этиология васкулитов остается НЕВЫЯСНЕННОЙ
1. Генетика
Имеются данные о возникновении СВ у членов одной

семьи.
Выявлена связь между носительством определенных антигенов главного комплекса гистосовместимости и развитием системных васкулитов.
Слайд 42. Инфекционные агенты
Вирусы гепатита А, В, С;
микобактерии туберкулеза и лепры;
вирусы Коксаки,
цитомегаловирус,
вирус простого герпеса,
бактериальные

инфекции (стрептококк, стафилококк, риккетсии, легионелла),
паразитарные (аскаридоз, стронгидоидоз, филяриатоз и др.)
грибковые инфекции.
Можно полагать, что данные инфекционные агенты выполняют триггерную роль в запуске иммуновоспалительного процесса в сосудистой стенке
Слайд 53. Воздействие внешних факторов
контакт с кремнием, металлами (бронза, латунь),
Курение
4. Васкулиты на фоне

других заболеваний
диффузных болезней соединительной ткани (ревматоидный артрит, системная красная волчанка, полимиозит и др.),
инфекционных заболеваний,
неопластических процессов,
при приеме некоторых лекарственных препаратов (антибиотики, хлортиазин, йод, стафилококковый анатоксин, противотифозная вакцина).
Слайд 6Патогенез
Ведущая роль - нарушения иммунной системы.
1) Воздействие этиологического фактора
2) Повреждение эндотелиоцитов
3) Формирование

антител к различным антигенам сосудистой стенки – эндотелиоцитам, коллагену, эластину, фосфолипидам клеточных мембран, плазменным и перинуклеарным антигенам лейкоцитов и др.
* Определенную роль в этом играет феномен молекулярной мимикрии, создающей условия для аутоиммунного повреждения не только чужеродных агентов, но и собственных тканей.
Среди большого количества аутоантител особое место занимают антинейтрофильные цитоплазматические антитела (АНЦА).
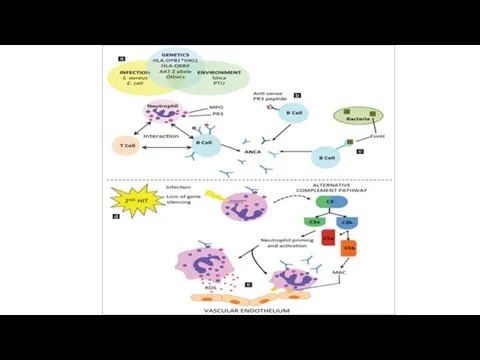
Слайд 7АНЦА
Это популяция аутоантител, реагирующих с различными ферментами цитоплазмы нейтрофилов, в первую очередь

с протеиназой-3 и миелопироксидазой.
Встречаются при АНЦА-ассоциированных васкулитах – гранулематозе Вегенера, микроскопическом полиартериите и синдроме Чарджа – Стросса.
1) Ферменты нейтрофилов экспрессируются на их мембранах (в результате чего они становятся доступными для АНЦА).
2) Взаимодействие аутоантител с антигенами при наличии соответствующего компонента комплемента
3) Формирование иммунных комплексов, которые в свою очередь фиксируются на базальных мембранах капилляров или сосудистой стенки различных паренхиматозных органов
4) Развития локального воспалительного процесса с тромбозом сосуда и ише- мией/некрозом тканей, которые кровоснабжались этим сосудом.
Слайд 9Классификация васкулитов по патогенезу

Слайд 10Классификация васкулитов по калибру пораженных сосудов

Слайд 11ГРАНУЛЕМАТОЗ С ПОЛИАНГИТОМ (ВЕГЕНЕРА)
Гранулематоз Вегенера (ГВ) – это системный гранулематозный васкулит с

поражением сосудов мелкого и среднего калибра.
Этиология и патогенез.
Этиологические факторы, вызывающие ГВ, неизвестны.
В основе - нарушения клеточного и гуморального звена иммунитета.
В сыворотке больных ГВ обнаруживают АНЦА, реагирующие с ферментами нейтрофилов (особенно с протеиназой-3).
Ферменты, освобождающиеся при дегрануляции нейтрофилов, обладают способностью повреждать базальную мембрану сосудов.
Слайд 12Клиническая картина
На первый план выступают поражения респираторного тракта и почек.
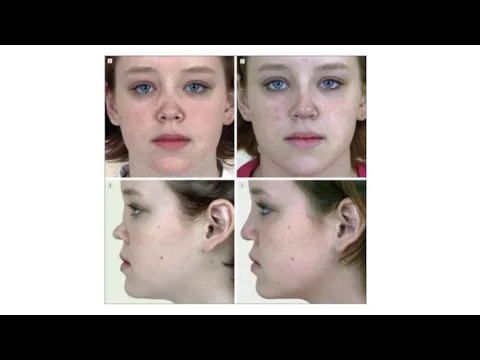
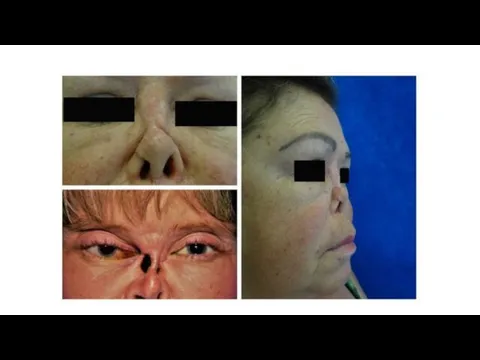
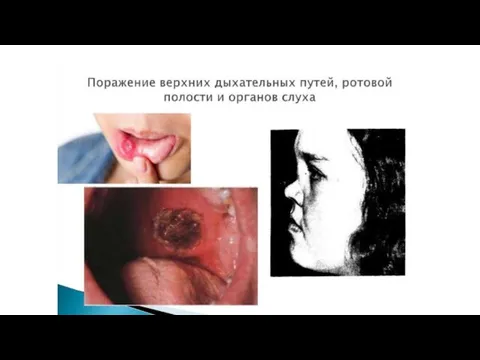
Последовательное поражение

верхних дыхательных путей с вовлечением придаточных пазух носа, перфорацией носовой перегородки и седловидной деформацией носа, поражение трахеи, гортани, легких, а также формирование быстропрогрессирующего гломерулонефрита.
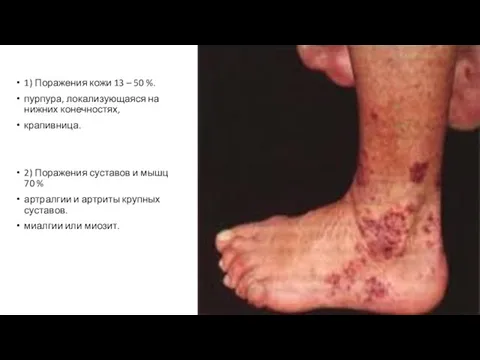
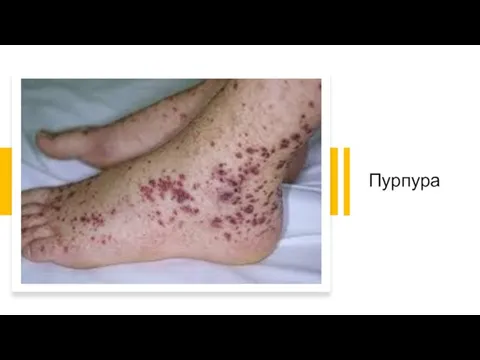
Слайд 141) Поражения кожи 13 – 50 %.
пурпура, локализующаяся на нижних конечностях,
крапивница.
2)
Поражения суставов и мышц 70 %
артралгии и артриты крупных суставов.
миалгии или миозит.
Слайд 153) Поражение сердечно-сосудистой системы. 40 %.
экссудативный перикардит,
коронарит, проявляющийся стенокардитическими болями,
миокардит, на фоне

которого могут развиваться тяжелые нарушения ритма и проводимости вплоть до AV-блокады
4) Поражение ЖКТ 40 %
боли в животе, перфорации и кровотечения.
эрозивный эзофагит.
поражения ротовой полости (гингивит)
Слайд 165) Поражение нервной системы
Со стороны ЦНС - ОНМК, субарахноидальные и субдуральные гематомы,

эпилепсия.
Периферическая полинейропатия и множественные мононевриты встречаются чаще
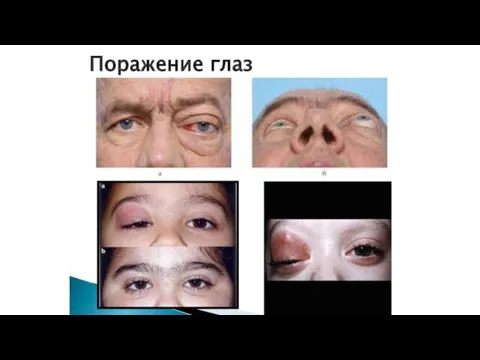
6) Поражение глаз 15 – 58 %
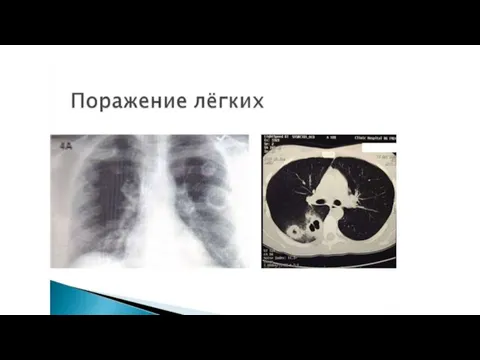
7) Поражение дыхательных путей. 70 %
хронический синусит
изъязвления слизистой носа с перфорацией или разрушением перегородки и образованием «седловидного носа»,
хронический ларинготрахеит, который может привести к стенозу трахеи и тяжелым нарушениям дыхания,
рецидивирующие инфильтраты в легких, склонные к распаду и формированию полостей.
Слайд 218) Поражение почек.
При ГВ часто встречается фокально-сегментарный гломерулонефрит 20 – 80 %
Возможно

развитие мембранозно-пролиферативного гломерулонефрита, инфарктов почек.
Слайд 23Лабораторные исследования
нормохромная анемия,
лейкоцитоз,
тромбоцитоз,
ускорение СОЭ.
Повышение СРБ
! Особое значение для диагностики ГВ имеют АНЦА к

протеиназе-3.
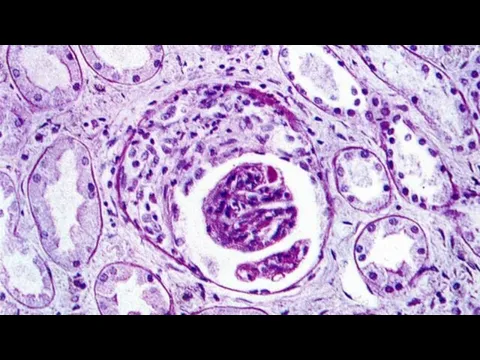
Слайд 24Морфологическое исследование
Важное значение для диагностики ГВ играет биопсия кожно-мышечного лоскута и/или почек.
Выявляется

деструктивно-продуктивный васкулит, полиморфно-клеточные гранулемы с наличием многоядерных гигантских клеток Лангханса, плазматических клеток, лимфоцитов, очаги фибриноидного некроза с деструкцией стенок артерий среднего и мелкого калибра, а также вен.
Слайд 25МИКРОСКОПИЧЕСКИЙ ПОЛИАНГИТ
Микроскопический полиангиит (МПА) -̆ некротизирующий системный васкулит с преимущественным поражением микроциркуляторного

русла (артериол, капилляров и венул), ассоциированный с антинейтрофильными цитоплазматическими антителами.
Мужчины болеют чаще, чем женщины
Средний возраст начала заболевания - 50 лет.
Слайд 26Этиология и патогенез МПА
Этиология не изучена.
Развитие некротизирующего васкулита и гломерулонефрита при МПА

обусловлено синтезом аутоантител к различным цитоплазматическим компонентам нейтрофилов (АНЦА).
При МПА данные антитела имеют высокую специфичность к миелопероксидазе (имеют перинуклеарное свечение) и реже реагируют с протеиназой-3 (цитоплазматическое свечение).
Слайд 27Клиника МПА
У 50% больных МПА проявляется в виде тяжёлого лёгочно-почечного синдрома.
1) Поражение

кожи. 40 - 60 %.
Пурпура нижних конечностях. Поражения кожи могут трансформироваться в язвы. Может наблюдаться крапивница.
2) Поражение суставов. 50 %.
Транзиторный артрит крупных суставов (локтевых, коленных, голеностопных).
3) Поражение мышц 50% характеризуется развитием миозита.
4) Поражения сердечно-сосудистой системы - коронарит, приводящий к развитию стенокардии и инфаркта миокарда.
Слайд 295) Поражения ЖКТ 40 %.
Боль в животе, диарея и тошнота.
При ФГДС обнаруживают

язвы различных отделов пищеварительного тракта, нередко осложняющиеся перфорацией и кровотечением.
6) Поражение периферической нервной системы в виде множественных невритов, которые обусловлены васкулитом эпиневральных сосудов.
7) Поражение глаз 20 %.
Эписклерит, склерит, кератит, увеит и васкулит сетчатки.
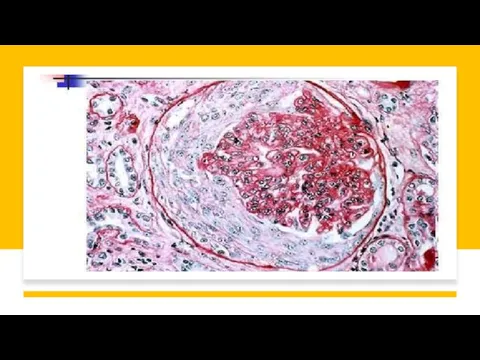
Слайд 308) Поражение почек типично для МПА 100 %.
Характеризуется развитием фокально-сегментарного гломерулонефрита (гломерулонефрита с полулуниями).

Экстракапиллярная пролиферация ведет к образованию полулун̆ин.
При МПА гломерулонефрит быстро осложняется формированием ХПН или нефротическим синдромом (отеки, гипопротеинемия, гиперпротеинурия, гиперхолестеринемия).
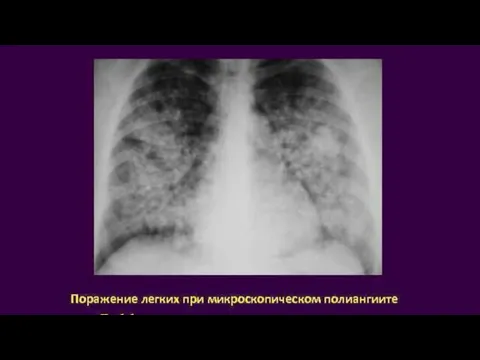
Слайд 339) Поражения легких 10 – 30 %.
Клинически проявляется кашлем, кровохарканьем, болями при

дыхании вследствие плеврита, одышкой.
При рентгеновском исследовании в легочной ткани выявляются инфильтраты, не имеющие склонности к распаду (в отличие от таковых при гранулематозных васкулитах).
При высокой клинико-иммунологической активности МПА могут развиваться альвеолярные кровотечения
Слайд 35Лабораторная диагностика
умеренная гипохромная анемия,
лейкоцитоз,
нейтрофилез,
ускорение СОЭ,
повышение СРБ,
снижение концентрации компонентов комплемента (С3 и С4).
При

поражении почек наблюдается повышение креатинина и мочевины, микрогематурия, протеинурия.
Повышение уровня АНЦА к миелопероксидазе, реже к протеиназе-3.
Слайд 36ЭОЗИНОФИЛЬНЫЙ ГРАНУЛЕМАТОЗ С ПОЛИАНГИТОМ (ЧЕРДЖА СТРОСС)
Синдром Чарджа – Стросса – эозинофильное, гранулематозное

воспаление респираторного тракта с некротизирующим васкулитом, поражающим сосуды мелкого и среднего калибра, часто сочетающееся с бронхиальной астмой и эозинофилией.
Синдромом Чарджа – Стросса чаще болеют мужчины в возрасте 30 – 45 лет.
Слайд 37Этиология и патогенез
В основе развития синдрома лежат нарушения клеточного и гуморального звена

иммунитета.
В сыворотке больных синдромом Чарджа – Стросса обнаруживают АНЦА, реагирующие с некоторыми ферментами нейтрофилов (особенно с миело- пероксидазой).
Слайд 38Клиническая картина
Можно выделить определенные фазы клинического течения заболевания.
1) Первая фаза характеризуется развитием

у больного бронхиальной астмы.
Зачастую астма становится рефрактерной к проводимой терапии. Бронхиальная астма может предшествовать симптомам васкулита и в течение длительного времени может оставаться единственным проявлением болезни.
Слайд 392) Во второй фазе болезни при обследовании часто обнаруживаются эозинофильные инфильтраты в

легких. Они развиваются асимметрично и рентгенологически предстают в виде диффузных или узловатых инфильтративных изменений.
Эозинофильный гастроэнтерит также наблюдается во второй фазе заболевания, проявляется болями в животе, тошнотой, рвотой, диареей и может осложняться желудочно-кишечными кровотечениями.
Из лабораторных изменений, характерных для этой фазы заболевания, следует отметить гиперэозинофилию (число эозинофилов составляет более 10 %).
Слайд 403) Третья фаза - клиническая картина васкулита
Поражение кожи - петехии, пурпура, подкожные узелки, зуд.
Патология

со стороны опорно-двигательного аппарата 20 – 50 % представляет собой артралгии или артриты.
Поражение ССС - миокардит, экссудативный перикардит
Поражение нервной системы - полиневриты с вовлечением в патологический процесс чувствительных и двигательных нервов. Со стороны ЦНС - ишемический или геморрагический инсульт.
Поражение почек часто проявляется очаговым гломерулонефритом, который редко приводит к развитию почечной недостаточности
Слайд 42Лабораторная диагностика АНЦА- СВ.
Основное значение имеет определение в сыворотке крови АНЦА методом

непрямой иммунофлуоресценции или с помощью иммуноферментного анализа с определением специфичности к протеиназе-3 (ПР-3) или миелопероксидазе (МПО).
Характерно увеличение СОЭ, концентрации СРБ, анемия, умеренный тромбоцитоз.
Клинические показания для определения АНЦА включают:
гломерулонефрит, особенно быстро прогрессирующий
кровохарканье/легочное кровотечение, особенно в сочетании с гломерулонефритом
кожный васкулит, сопровождающийся системными проявлениями
множественные очаги поражения легких при рентгенологическом исследовании
хроническое деструктивное поражение верхних дыхательных путей
затяжное течение синусита
множественный мононеврит
Слайд 43Гистологическое исследование при АНЦА- СВ.
Положительные данные биопсии играют большую роль в подтверждении

васкулита.
При биопсии слизистой носа у больных ГПА обнаруживают деструктивнопродуктивный васкулит и гигантоклеточные некротизирующие гранулёмы.
При биопсии кожно- мышечного лоскута у больных ЭГПА обнаруживают картину деструктивно- продуктивного васкулита с эозинофильной инфильтрацией.
Биопсия почки (c обязательным применением иммунолюминисцентной микроскопии) позволяет подтвердить диагноз АНЦА-ГН при наличии фибриноидного некроза капилляров клубочка и артериол, экстракапиллярного пролиферативного ГН с “полулуниями” в клубочках в сочетании с отсутствием иммунных депозитов в ткани почки.
Показаниями к диагностической биопсии почки являются:
нефропатия неясного генеза с протеинурией более 1 г/л, постоянной или рецидивирующей клубочковой гематурией;
острая или подострая почечная недостаточность с симптомами ГН или с системными проявлениями
Слайд 44Общие принципы лечения системных васкулитов
Основная цель фармакотерапии СВ направлена на подавление иммунопатологических

реакций, лежащих в основе заболевания.
Патогенетическую терапию подразделяют на три этапа:
индукция ремиссии коротким курсом агрессивной терапии;
поддержание ремиссии при помощи длительной (0,5- 2 года) терапии иммуносупрессантами;
лечение рецидивов.
Слайд 45Основные группы лекарственных препаратов:
1) Комбинированная терапия циклофосфамидом и ГК
2) Генно- инженерная анти-

В- клеточная терапия ритуксимабом
Плазмаферез
рекомендуется применять для лечения отдельных пациентов с БПГН в качестве процедуры, улучшающей прогноз в отношении функции почек. Сочетание стандартной патогенетической терапии и плазмафереза у больных СВ с тяжелым поражением почек снижает риск развития терминальной почечной недостаточности.
Слайд 463) Азатиоприн в сочетании с ГК
4) Лефлуномид
5) Метотрексат
6) Мофетила микофенолат
7) Нормальный иммуноглобулин

человека назначают в/в при тяжелом поражении почек, развитии геморрагического альвеолита, в случаях присоединения серьезных инфекционных осложнений.
Слайд 4710) Другие лекарственные средства
Антимикробные (триметоприм/ сульфаметоксазол) и противовирусные препараты могут иметь особое

значение в лечении больных СВ с доказанным участием инфекционных факторов в развитии заболевания.
Или для профилактики инфекционных осложнений на фоне терапии ГКС




































 Болезни, связанные с нехваткой химических элементов
Болезни, связанные с нехваткой химических элементов Мемристорный протез функционального отдела спинного мозга. Исследовательский проект
Мемристорный протез функционального отдела спинного мозга. Исследовательский проект Квест – игра, посвящённая всемирному дню борьбы со спидом Предупреждён - вооружён
Квест – игра, посвящённая всемирному дню борьбы со спидом Предупреждён - вооружён Оценка эффективности применения шелка по сравнению с викрилом для закрытия срединных брюшных разрезов
Оценка эффективности применения шелка по сравнению с викрилом для закрытия срединных брюшных разрезов ІХС: Інфаркт міокарда
ІХС: Інфаркт міокарда Доврачебная помощь при клинической смерти
Доврачебная помощь при клинической смерти Medical concern of a shoulder pain
Medical concern of a shoulder pain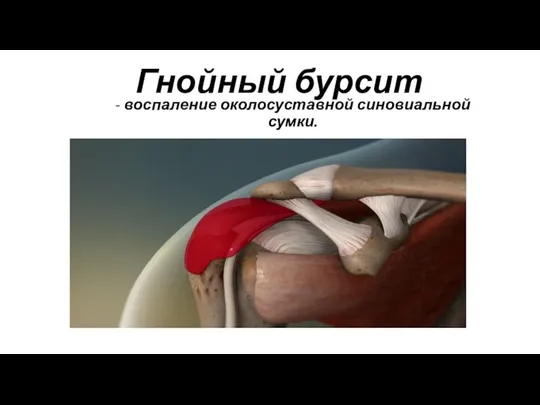 Гнойный бурсит
Гнойный бурсит Школа здоровья для беременных. Что произошло в моём организме? Лекция 2
Школа здоровья для беременных. Что произошло в моём организме? Лекция 2 Известные дерматологические школы мира и их вклад в развитие дисциплины
Известные дерматологические школы мира и их вклад в развитие дисциплины Высокомощностная брахитерапия в комплексном лечении раннего рака молочной железы
Высокомощностная брахитерапия в комплексном лечении раннего рака молочной железы Хирургическая обработка гнойного очага при оказании специализированной помощи в условиях мирного времени
Хирургическая обработка гнойного очага при оказании специализированной помощи в условиях мирного времени Мифы о здоровом образе жизни
Мифы о здоровом образе жизни Язва желудка. Язва двенадцатиперстной кишки
Язва желудка. Язва двенадцатиперстной кишки Лучевые поражения животных
Лучевые поражения животных Аллергические заболевания и их профилактика
Аллергические заболевания и их профилактика Сахарный диабет
Сахарный диабет Корь. Эпидемиология
Корь. Эпидемиология Перемещение больного
Перемещение больного Хвороби кролів
Хвороби кролів Методы исследования восприятия
Методы исследования восприятия Профилактика коронавируса
Профилактика коронавируса Умей предупреждать болезни
Умей предупреждать болезни Стоматологический препарат Сафорайд. Занятие 2
Стоматологический препарат Сафорайд. Занятие 2 ЗОЖ. Проблема здоровья дошкольников
ЗОЖ. Проблема здоровья дошкольников Проект памяти врачей-героев, погибших от коронавируса
Проект памяти врачей-героев, погибших от коронавируса Анатомия и физиология сердца (лекция 4)
Анатомия и физиология сердца (лекция 4) Организация обучения курсу БЖД на время карантина
Организация обучения курсу БЖД на время карантина