Содержание
- 2. История открытия Много веков назад арабы уже знали различные способы получения душистых веществ из растений и
- 3. Термин «эфир» впервые применил к синтетическим веществам Карл Вильгельм Шееле (1742-1786) в 1782 г. В труде
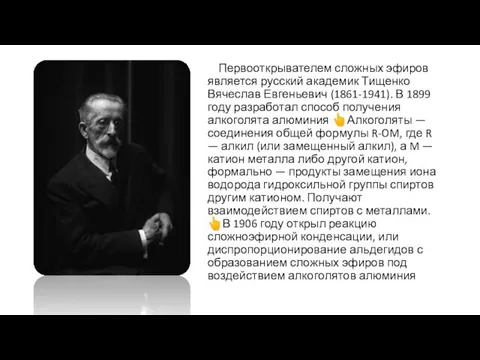
- 4. Первооткрывателем сложных эфиров является русский академик Тищенко Вячеслав Евгеньевич (1861-1941). В 1899 году разработал способ получения
- 5. Нахождение в природе Сложные эфиры входят в состав различных плодов, ягод, фруктов.(рис.3) Запах может определять только
- 6. Номенклатура и изомерия Среди функциональных производных карбоновых кислот особое место занимают сложные эфиры — соединения, представляющие
- 7. Часто сложные эфиры называют по тем остаткам кислот и спиртов, из которых они состоят. Так, рассмотренные
- 8. 2. Изомерия положения сложноэфирной группировки -СО-О-. Этот вид изомерии начинается со сложных эфиров, в молекулах которых
- 9. Классификация и состав сложных эфиров Когда число атомов С в исходных карбоновой кислоте и спирте не
- 10. Третья группа – жиры. В отличие от предыдущих двух групп на основе одноатомных спиртов ROH, все
- 11. Сложные эфиры Сложные эфиры (алкилалканоаты) — производные карбоновых кислот, в которых атом водорода карбоксильной группы замещен
- 12. Применение В пищевой промышленности В парфюмерной промышленности В медицине В производстве моющих средств Используют как растворители
- 14. Добыча в лаборатории Этерификация (от др.-греч. αἰθήρ — эфир и лат. facio — делаю) — реакция
- 16. Скачать презентацию












 Химические реакции
Химические реакции День химии
День химии Концентрированная серная кислота
Концентрированная серная кислота Азотистые основания. Нуклеотиды и нуклеозиды. ДНК и РНК
Азотистые основания. Нуклеотиды и нуклеозиды. ДНК и РНК Неметаллы азот
Неметаллы азот ЭОР в преподавании химии
ЭОР в преподавании химии Химическая связь
Химическая связь Молекулы и атомы. Относительная атомная масса
Молекулы и атомы. Относительная атомная масса Группа веществ, требующих особых методов изолирования. Характеристика соединений. Токсикологическое значение
Группа веществ, требующих особых методов изолирования. Характеристика соединений. Токсикологическое значение Соли Na2SO4
Соли Na2SO4 Презентация на тему Химическая связь
Презентация на тему Химическая связь  Производство аммиака
Производство аммиака Органическая химия. Введение
Органическая химия. Введение Коалесцирующие фильтры. Моделирование процесса разделения отходов углеводородов коалесцирующими фильтрами
Коалесцирующие фильтры. Моделирование процесса разделения отходов углеводородов коалесцирующими фильтрами Избранные главы органической стереохимии
Избранные главы органической стереохимии Кислоты с металлами
Кислоты с металлами Валентность химических элементов
Валентность химических элементов Тақырыпқа байланысты білімді жүйелеу
Тақырыпқа байланысты білімді жүйелеу Химическая география чудес природы
Химическая география чудес природы Ковалентная неполярная связь
Ковалентная неполярная связь Хим_10_30_Производство_аммиака
Хим_10_30_Производство_аммиака Органические цепочки
Органические цепочки Чистые вещества и смеси. Классификация веществ. Оксиды
Чистые вещества и смеси. Классификация веществ. Оксиды Физическая химия тугоплавких неметаллических и силикатных материалов (ТНСМ)
Физическая химия тугоплавких неметаллических и силикатных материалов (ТНСМ) Круговорот серы в природе
Круговорот серы в природе Презентация на тему Степень окисления 8 класс
Презентация на тему Степень окисления 8 класс  Ковалентная связь
Ковалентная связь Кислоты
Кислоты