Содержание
- 3. Твердое вещество Аморфное Кристаллическое смола стекло пластилин воск хлорид натрия сульфат меди
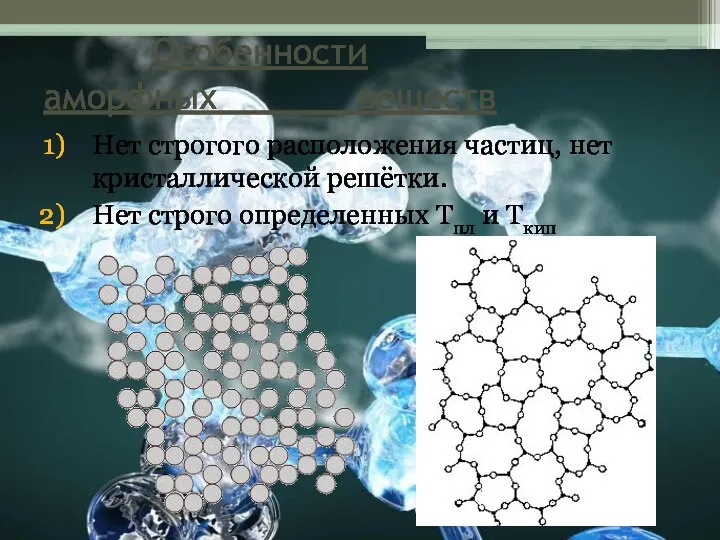
- 4. Особенности аморфных веществ Нет строгого расположения частиц, нет кристаллической решётки. Нет строго определенных Тпл и Ткип
- 5. Особенности кристаллических веществ Строгое расположение частиц, образующих кристаллическую решётку Строго определенные Тпл и Ткип Узлы кристаллической
- 6. Кристаллические решётки веществ-это упорядоченное расположение частиц (атомов, молекул, ионов) в строго определённых точках пространства. Точки размещения
- 7. Типы кристаллических решёток
- 9. Ионная кристаллическая решётка В узлах решётки ионы (+ и – заряженные), между которыми существует ионная сязь
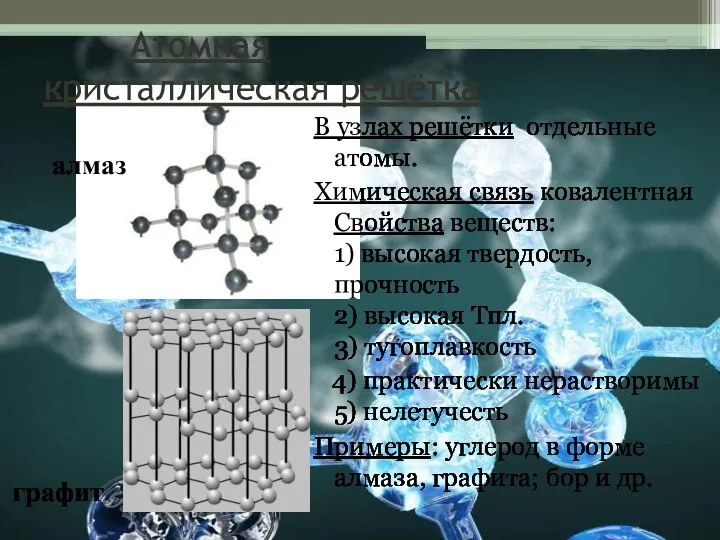
- 10. Атомная кристаллическая решётка В узлах решётки отдельные атомы. Химическая связь ковалентная Свойства веществ: 1) высокая твердость,
- 11. Свойства веществ: 1) малая твердость, прочность 2) низкие Тпл, Ткип, 3) при комнатной Т обычно жидкость
- 12. Молекулярная кристаллическая решетка В узлах решетки - молекулы Химическая связь Ковалентная неполярная (между частицами в узлах
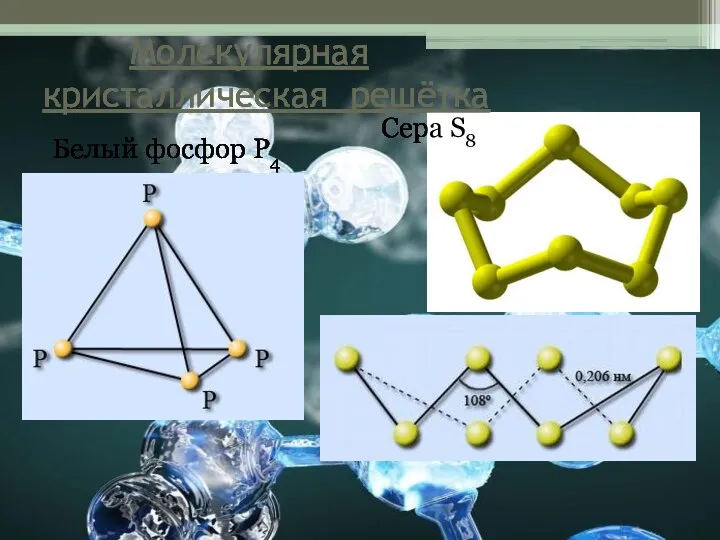
- 13. Молекулярная кристаллическая решётка Белый фосфор Р4 Сера S8
- 14. Металлическая кристаллическая решётка В узлах решётки атомы и ионы (+) Химическая связь металлическая Свойства веществ: 1)
- 16. Какой тип кристаллической решетки из рассмотренных выше не встречается в простых веществах? Какие кристаллические решетки характерны
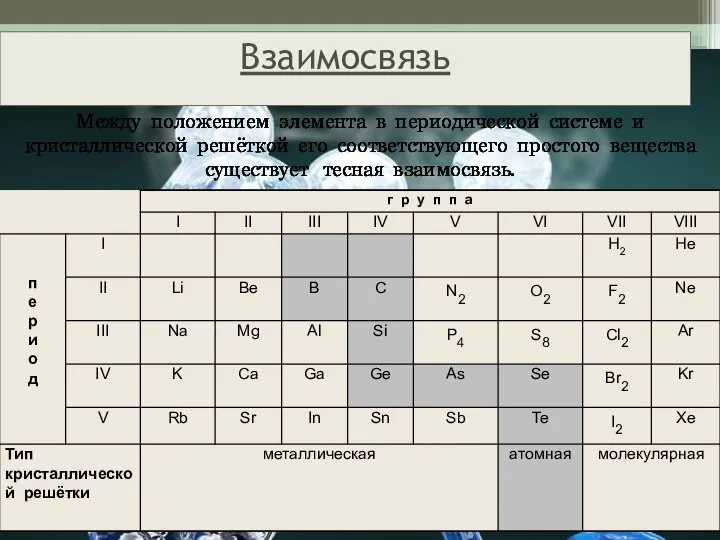
- 17. Между положением элемента в периодической системе и кристаллической решёткой его соответствующего простого вещества существует тесная взаимосвязь.
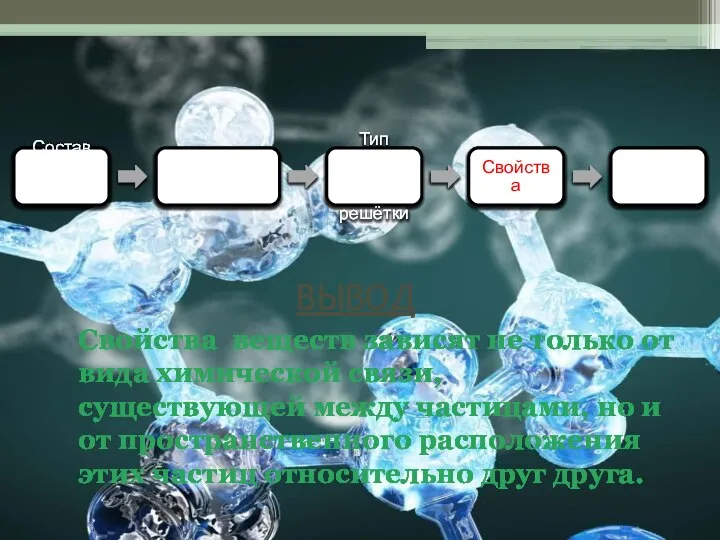
- 18. Состав вещества Вид химической связи Тип кристал-лической решётки Свойства Примене-ние ВЫВОД Свойства веществ зависят не только
- 19. 1. Немолекулярное строение имеет вещество, формула которого: А) Р4 Б) О3 В) C Г) I2 2.
- 21. Скачать презентацию












 Азот
Азот Синтетические моющие средства
Синтетические моющие средства Общие химические свойства металлов
Общие химические свойства металлов Презентация на тему Простые вещества - неметаллы
Презентация на тему Простые вещества - неметаллы  Электролитическая диссоциация
Электролитическая диссоциация Презентация на тему Алмазы
Презентация на тему Алмазы  Алмашу реакциясе
Алмашу реакциясе Химия нефти и газа
Химия нефти и газа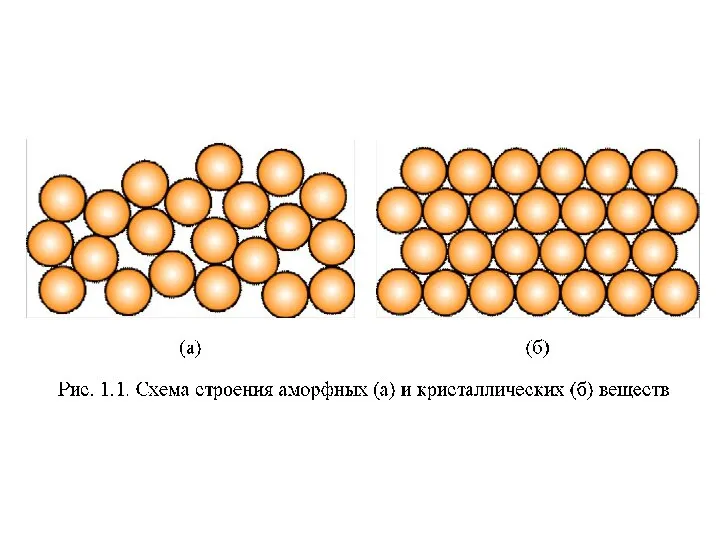 Материаловедение
Материаловедение Основания и их свойства
Основания и их свойства Энергосбережение в нашей жизни
Энергосбережение в нашей жизни Щелочные металлы — это элементы главной подгруппы I группы
Щелочные металлы — это элементы главной подгруппы I группы Физические опыты в домашней лаборатории
Физические опыты в домашней лаборатории Классификация углеводов: моносахариды, дисахариды, полисахариды. Химическая структура. Свойства и функция углеводов
Классификация углеводов: моносахариды, дисахариды, полисахариды. Химическая структура. Свойства и функция углеводов Презентация на тему Фолиевая кислота
Презентация на тему Фолиевая кислота  Решение турнира. 9 класс
Решение турнира. 9 класс Графит (С)
Графит (С) Ферментативные методы анализа
Ферментативные методы анализа Аммиак. Азот
Аммиак. Азот Элементоорганические мономеры (соединения)
Элементоорганические мономеры (соединения) Классификация органических веществ
Классификация органических веществ Химический состав клетки
Химический состав клетки Расчет физических свойств нефтепродуктов. Практическая работа 1
Расчет физических свойств нефтепродуктов. Практическая работа 1 Синтетический каучук
Синтетический каучук Алкены. Непредельные углеводороды
Алкены. Непредельные углеводороды L4_Aminoacids, peptides, proteins (2)
L4_Aminoacids, peptides, proteins (2) Алканы: состав, строение, изомерия, номенклатура, получение
Алканы: состав, строение, изомерия, номенклатура, получение Диаграммы состояния сплавов двухкомпонентных систем
Диаграммы состояния сплавов двухкомпонентных систем