Содержание
- 2. Что мы узнаем? Немного истории Положение железа в периодической системе: электронная формула Нахождение железа в природе
- 3. Немного истории «Железо» от санскритского «жель»-блестеть,пылать Метеориты Украшения,орудия труда Монеты
- 4. Положение железа в периодической системе: электронная формула 8 2 1s2 2 4s2 2s22p6 14 3s23p63d6 4,VIII,побочная
- 5. 2-ой по распространенности металл после Al (5,1%) Нахождение железа в природе Fe3O4 Магнетит Fe2O3 Гематит FeS2
- 6. Химические свойства железа: 1.Взаимодействие с простыми веществами(при t°). А) с галогенами: 2Fe + 3Cl2→2FeCl3 Б) с
- 7. Химические свойства железа: 2. Взаимодействие со сложными веществами: А) с кислотами (HCl ,разб.H2SO4) Fe +2 HCl
- 8. Качественные реакции на ионы Fe2+, Fe3+
- 9. Качественные реакции на ионы Fe2+, Fe3+
- 10. Качественные реакции на ионы Fe2+, Fe3+
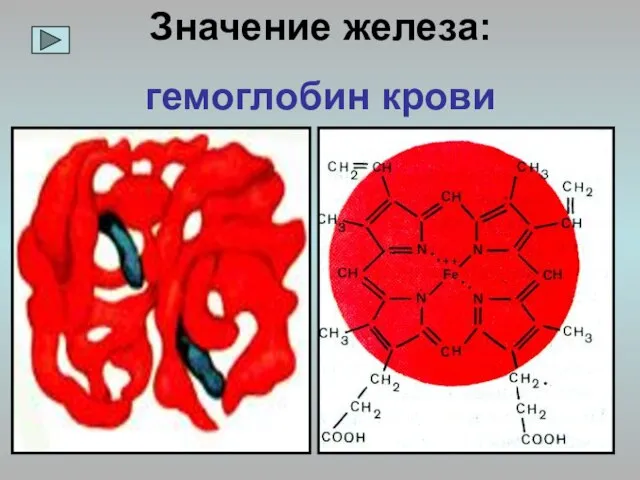
- 11. Значение железа: гемоглобин крови
- 12. Значение железа: шпинат мясо капуста яблоки
- 13. Памятник железу-Эйфелева башня
- 15. Скачать презентацию











 Оценка качества пищевой соли, реализуемой в розничной торговле
Оценка качества пищевой соли, реализуемой в розничной торговле Комментарии к выполненным заданиям по темам растворы и электролитическая диссоциация. 8 класс
Комментарии к выполненным заданиям по темам растворы и электролитическая диссоциация. 8 класс Алюминий и его органические производные
Алюминий и его органические производные Генетические ряды Fe2+ и Fе3+. Качественные реакции на Fе2+ и Fе3+
Генетические ряды Fe2+ и Fе3+. Качественные реакции на Fе2+ и Fе3+ Тосол. Гликолевые антифризы
Тосол. Гликолевые антифризы Способы очистки питьевой воды
Способы очистки питьевой воды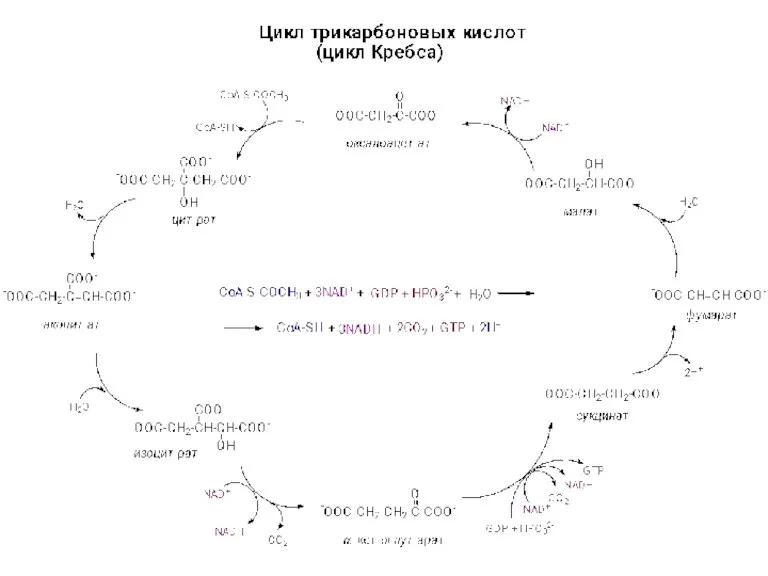 Цикл трикарбоновых кислот
Цикл трикарбоновых кислот Органические вещества
Органические вещества Железо как химический элемент
Железо как химический элемент Строение атома. Ядро и электронная оболочка
Строение атома. Ядро и электронная оболочка Классы неорганических соединений
Классы неорганических соединений Электронное и пространственное строение молекулы метана Учитель химии МБОУ СОШ № 9 МО ЩР станица Новощербиновская Степучева Ол
Электронное и пространственное строение молекулы метана Учитель химии МБОУ СОШ № 9 МО ЩР станица Новощербиновская Степучева Ол Сокровища соляных дворцов
Сокровища соляных дворцов Презентация по химии
Презентация по химии Общая характеристика металлов
Общая характеристика металлов Амины. Номенклатура аминов
Амины. Номенклатура аминов Алканы: состав, строение, изомерия, номенклатура, получение
Алканы: состав, строение, изомерия, номенклатура, получение Оксиды. Классификация, химические и физические свойства. Индивидуальные свойства
Оксиды. Классификация, химические и физические свойства. Индивидуальные свойства Изучение условий покрытий на основе Диатомита/ПАК и Каолина/ПАК
Изучение условий покрытий на основе Диатомита/ПАК и Каолина/ПАК Фотографии к исследовательской работе в рамках конкурса УРАЛХИМиЯ
Фотографии к исследовательской работе в рамках конкурса УРАЛХИМиЯ Магний и кальций
Магний и кальций Исследование структуры продуктов аммонолиза мезопористых магниетермических порошков тантала
Исследование структуры продуктов аммонолиза мезопористых магниетермических порошков тантала Термохимия. Термодинамические параметры
Термохимия. Термодинамические параметры Надмолекулярные структуры
Надмолекулярные структуры Химия. Наука о веществах
Химия. Наука о веществах Галогены и их соединения
Галогены и их соединения Воздействие нейропептидов семакс и PGP на содержание транскриптов гена в головном мозге крыс в условиях экспериментальной ишемии
Воздействие нейропептидов семакс и PGP на содержание транскриптов гена в головном мозге крыс в условиях экспериментальной ишемии Презентация на тему Путешествие по континенту Химия
Презентация на тему Путешествие по континенту Химия